Natrium hidroksida
Natrium hidroksida (NaOH), dikenali juga sebagai lai dan soda kaustik, ialah sejenis bes berlogam kaustik. Ia digunakan di dalam banyak industri, kebanyakannya sebagai satu bes kimia di dalam penghasilan pulpa and kertas, tekstil, air minuman, sabun dan detergen dan sebagai pencuci longkang. Penghasilan seluruh dunia pada tahun 1998 ialah sekitar 45 juta tan. Ia adalah bes yang biasa digunakan di dalam makmal kimia.

| |
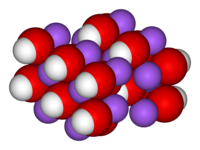
| |
| Nama | |
|---|---|
| Nama IUPAC
Sodium hydroxide
| |
| Nama lain
Soda kaustik
Lai | |
| Pengecam | |
Imej model 3D Jmol
|
|
| ChemSpider | |
| ECHA InfoCard | 100.013.805 |
| Nombor EC |
|
| Nombor E | E524 (pengawal keasidan pH & agen antikerakan) |
PubChem CID
|
|
| Nombor RTECS |
|
| Nombor PBB | 1823 |
CompTox Dashboard (EPA)
|
|
| |
| Sifat | |
| NaOH | |
| Jisim molar | 39.9971 g/mol |
| Rupa bentuk | pepejal putih, higroskopik |
| Ketumpatan | 1.04 g/cm3 |
| Takat lebur | 318 °C (604 °F; 591 K) |
| Takat didih | 1,388 °C (2,530 °F; 1,661 K) |
| 111 g/100 ml (20 °C) | |
| Keterlarutan dalam etanol | 13.9 g/100 mL |
| Keterlarutan dalam metanol | 23.8 g/100 mL |
| Keterlarutan dalam gliserol | larut |
| Keasidan (pKa) | ~13 |
Indeks biasan (nD)
|
1.412 |
| Bahaya | |
| Pengelasan EU | {{{value}}} |
| Frasa R | R35 |
| Frasa S | S1/2, S26, Templat:S37/39, S45 |
| NFPA 704 (berlian api) | |
| Takat kilat | Tidak mudah terbakar |
| Sebatian berkaitan | |
Anion lain
|
Natrium hidrosulfida Natrium amida |
Kation lain
|
Litium hidroksida Kalium hidroksida Rubidium hidroksida Sesium hidroksida |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| | |
| Rujukan kotak info | |
Natrium hidroksida asli berbentuk pepejal putih.
Zat ini ada dalam berbagai bentuk serpihan, butiran, kubus, dan balok dalam fase padat.
Natrium hidroksida adalah penyerap kelembaban. Reaksi soda api dengan air menghasilkan panas. Jika soda api dilarutkan dalam air, gelembung dan percikan akan dihasilkan.
Selain air, soda api bereaksi kuat dengan logam seperti aluminium, magnesium, seng, dan timbal. Reaksi soda api dengan logam menghasilkan gas hidrogen, yang dapat menyebabkan ledakan.
Reaktivitas zat ini dapat meluas ke jaringan hidup seperti kulit haiwan dan organ tubuh lainnya. Reaksi soda api dengan beberapa gula seperti maltosa, galaktosa dan fruktosa dapat menghasilkan karbon monoksida.
Catatan penting: soda kaustik tidak dapat digunakan tanpa mengikuti aturan keselamatan.[1]
Rujukan
suntingPautan luar
sunting- Media berkenaan Natrium hidroksida di Wikimedia Commons
