Saponificación

A saponificación é un proceso químico no que se forma xabón a partir de graxas. Na saponificación xeralmente faise reaccionar un hidróxido ou base ou álcali (normalmente hidróxido de sodio, NaOH) cun triglicérido. O triglicérido é un éster de tres ácidos graxos co glicerol, que é hidrolizado durante a saponificación liberando os seus ácidos graxos, que reaccionan co metal do hidróxido (sodio no noso exemplo), formando un sal entre o sodio e o ácido graxo ou carboxilato de sodio, que é o xabón. Na saponificación dos triglicéridos, ademais de xabón prodúcese glicerol libre.
Denomínanse substancias "saponificables" a aquelas que se poden converter en xabón.[1]. Os lípidos saponificables son aqueles que poden dar lugar a xabóns, porque son lípidos que conteñen ácidos graxos, tales como triglicéridos, fosfolípidos, esfingolípidos ou glicolípidos. Os lípidos insaponificables non poden orixinar xabóns, como por exemplo o colesterol (un esterol do grupo dos esteroides) ou o caroteno (un terpeno), xa que non conteñen ácidos graxos (os ésteres do colesterol si son saponificables, porque neles o grupo OH do colesterol está esterificado cun ácido graxo, que pode orixinar xabón).
Saponificación de triglicéridos
[editar | editar a fonte]As principais substancias que son saponificadas son os aceites vexetais e as graxas animais. Estas substancias lipídicas están formadas por triglicéridos, que son ésteres de glicerol con tres ácidos graxos diversos. Os triglicéridos poden ser convertidos en xabón nun proceso dun só paso (saponificación tradicional) ou de dous pasos (saponificación con vapor, que se explica nun capítulo máis abaixo).
No proceso tradicional dun paso, o triglicérido é tratado cunha base forte (como a sosa cáustica, NaOH), que acelera a rotura do enlace éster do triglicérido liberando os ácidos graxos, que forman o sal (carboxilato sódico, o xabón) e glicerol. Este proceso é o principal método industrial de producir glicerol. Se é necesario, os xabóns poden ser precipitados por con cloruro sódico saturado. O valor de saponificación é a cantidade de base requirida para saponificar unha graxa simple. Na fabricación dos xabóns os triglicéridos son moi purificados, pero outras saponificacións inclúen outras hidrólises básicas de triglicéridos non purificados, por exemplo a conversión das graxas de cadáveres en adipocera. Este proceso de formación de adipocera é máis frecuente cando a cantidade de tecido adiposo do cadáver é grande, e os axentes de descomposición do cadáver están ausentes ou son escasos, e o terreo do enterramento é especialmente alcalino, húmido e anaerobio.
Mecanismo da hidrólise básica
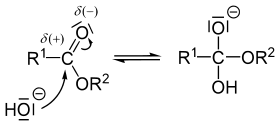
[editar | editar a fonte]O mecanismo da reacción por medio do cal os ésteres son escindidos pola base implica unha substitución ácida nucleofílica.[2] O anión hidróxido únese (ou "ataca") o grupo carbonilo do éster. O produto inmediato é un ortoéster:
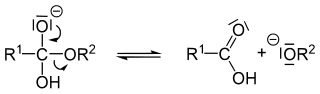
Nesta fase, o ortoéster pode facer dúas cousas: volver a formar o carbonilo orixinando ou ben o hidróxido ou ben o alcóxido. A primeira posibilidade orixina as substancias iniciais, polo que é improdutiva (pero explica que a saponificación é en realidade un equilibrio). Se o que se produce é a segunda posibilidade, libérase o alcóxido, que xera un ácido carboxílico (o ácido graxo):
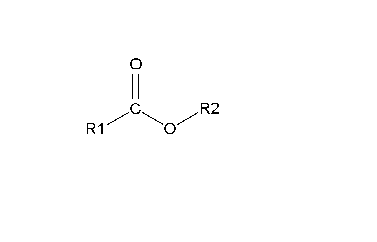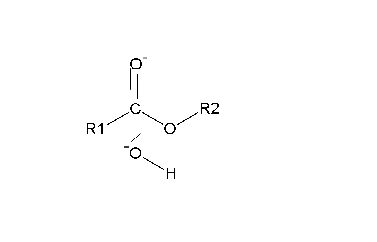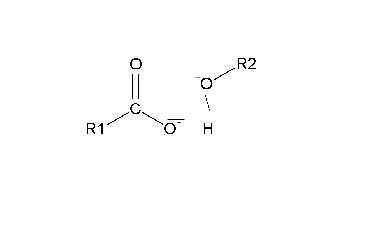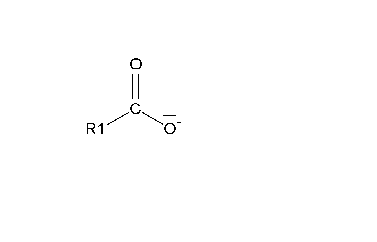
O alcóxido é máis básico ca a base conxugada do ácido carboxílico, e, por tanto, prodúcese unha rápida transferencia dun protón:
Nun procedemento clásico de laboratorio, o triglicérido trimiristina obtense primeiro extraéndoo da noz moscada (xénero Myristica) con dietil éter.[3] Despois, ten lugar a saponificación do ácido mirístico que contén con NaOH disolto en auga, orixinando o sal sódico do ácido. O ácido pode obterse engadindo ácido clorhídrico diluído.[4]
Hidrólise con vapor
[editar | editar a fonte]Os triglicéridos poden ser saponificados tamén nun proceso en dous pasos, que empeza coa hidrólise con vapor do triglicérido. Este proceso orixina o ácido carboxílico, non o seu sal, xunto con glicerol. Seguidamente, o ácido graxo neutralízase con álcali para dar o xabón. A vantaxe deste proceso en dous pasos é que se poden purificar os ácidos graxos, o que serve para producir xabóns de mellor calidade. A hidrólise con vapor ten lugar por un mecanismo similar ao da ruta catalizada por unha base, e implica o ataque dunha molécula de auga (non de hidróxido neste caso) ao carbonilo. O proceso é lento, polo que se require o vapor.
Aplicacións
[editar | editar a fonte]A saponificación é importante en moitas tecnoloxías e en moitos aspectos da vida diaria.
Xabóns duros e brandos
[editar | editar a fonte]Dependendo da natureza do álcali utilizado na súa produción, os xabóns teñen distintas propiedades. O hidróxido de sodio (NaOH) orixina "xabóns duros", e o hidróxido de potasio (KOH) orixina "xabóns brandos".
Xabóns de litio
[editar | editar a fonte]Os derivados de litio do 12-hidroxiestearato e varios outros ácidos carboxílicos son constituíntes importantes das graxas lubricantes. Nas graxas baseadas no litio, os carboxilatos de litio son espesantes. Os "xabóns complexos" tamén son moi utilizados; e son combinacións de xabóns metálicos, como os xabóns de litio e calcio.[5]
Extintores de lume
[editar | editar a fonte]Os incendios onde os combustibles son graxas para cociñar e aceites clasifícanse como lumes de tipo F (en Europa/Asia/Australia) ou de tipo K (nos Estados Unidos). Arden producindo maiores temperaturas ca outros líquidos inflamables, facendo que os extintores para lumes de clase B sexan ineficaces. Os líquidos inflamables teñen un punto de inflamabilidade inferior ao do aceite de cociñar. Este tipo de lumes deben ser extinguidos con extintores de "química húmida", que realizan a extinción por saponificación. O axente extintor converte rapidamente a substancia en combustión nun xabón non combustible. Este proceso é endotérmico, polo que absorbe enerxía térmica dos arredores, o que fai decrecer a temperatura dos arredores, ademais de apagar o lume.
Conservación de obras de arte
[editar | editar a fonte]
As pinturas ao óleo poden sufrir saponificación co tempo, orixinando un dano visible e deformación nas obras de arte, con formación de grumos e protrusións que dispersan a luz. A capa de fondo das capas de pintura ao óleo xeralmente contén metais pesados en pigmentos como chumbo branco, chumbo vermello ou cinc branco. Se eses metais pesados reaccionan cos ácidos graxos dos aceites da pintura que unen os pigmentos, poden formarse xabóns nunha capa de pintura profunda, que poden despois migrar a capas superiores ata chegaren á superficie da pintura.[6]
A saponificación nas pinturas ao óleo foi descrita por primeira vez en 1997.[7] Pénsase que é un fenómeno moi estendido, e foi observado en moitas obras pictóricas que datan desde o século XV ao XX, de moi diferentes orixes xeográficas, e pintadas sobre distintos soportes, como lenzo, papel, madeira, e cobre. Unha análise química pode poñer de manifesto se tivo lugar saponificación nas capas profundas dunha pintura antes de que aparezan signos visibles na superficie, mesmo en pinturas con séculos de antigüidade.[8]
O proceso de saponificación nas pinturas aínda non se coñece totalmente. A saponificación non ocorre sempre en todas as pinturas antigas, aínda que conteñan as materias necesarias para que se produza. Non se sabe que é o que desencadea o proceso, nin se pode ser detido unha vez comezado.[9] Actualmente, o único método de restauración que se pode aplicar é retocar a pintura.
Notas
[editar | editar a fonte]- ↑ K. Schumann, K. Siekmann “Soaps” in Ullmann’s Encyclopedia of Industrial Chemistry 2005, Wiley-VCH, Weinheim. doi 10.1002/14356007.a24_247
- ↑ John McMurry, Organic Chemistry (2nd Edition).
- ↑ Organic Syntheses 1:538 Link
- ↑ Organic Syntheses 1:379 Link
- ↑ Thorsten Bartels et al. "Lubricants and Lubrication" in Ullmann's Encyclopedia of Industrial Chemistry, 2005, Weinheim. doi 423 10.1002/14356007.a15 423
- ↑ Silvia A. Centeno and Dorothy Mahon, "The Chemistry of Aging in Oil Paintings: Metal Soaps and Visual Changes." The Metropolitan Museum of Art Bulletin’’, Summer 2009, pp. 12-19.
- ↑ Descubriuse en Holanda ao analizar o óleo de Rembrandt Lección de Anatomía do Dr. Nicolaes Tulp (1632). Ver Centeno, p. 14.
- ↑ Centeno, p. 16.
- ↑ Centeno, p. 19.
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]Ligazóns externas
[editar | editar a fonte]- Soapmaking at Bellaonline - Soapmaking articles, forum and supplier links.
- Soap Naturally Web and Mailing List - Resources for natural handmade soapmakers.
- Soap Recipe Corner - Soapmaking explained.
- About Candle and Soap Making Arquivado 21 de abril de 2011 en Wayback Machine. - Soap making at About.com
- Glossary for the Modern Soap Maker Arquivado 01 de febreiro de 2004 en Wayback Machine. - A collection of terms, definitions and acronyms for today's soap maker.
- The Handbook of Soap Manufacture - Libro de 1908.