Биохемија
Биокемија или биохемија је кемија живота, мост између биологије и кемије који проучава како комплексне хемијске реакције стварају живот. Биохемија је хибридни део хемије који конкретно проучава хемијске процесе у живим организмима.[1] Овај чланак дискутује само копнену биохемију, која почива на угљенику и води. Како сви облици живота које данас имамо на планети имају заједничко порекло, према томе имају и сличне биохемије, као што су генетска шифра и стереохемија многих биомолекула. Непознато је да ли су наизменичне биохемије уопште и могуће.[2][3]

Биохемија проучава структуру и функцију целуларних компоненти, као што су протеини, угљени хидрати, липиди, нуклеинске киселине и остали биомолекули. Иако постоји огроман број различитих биомолекула, они се често састоје од истих јединица које се понављају мономера, али који се понављају у различитим секвенцима. Недавно, биохемија је почела да се фокусира на проучавање реакција у којима су катализатори ензими, и на проучавање особина протеина.
Биохемија метаболизма ћелије и биохемија ендокриног система су два домена која су интезивно студирана. Друге области које спадају под појам биохемије су генетска шифра (ДНК, РНК), синтеза протеина, транспорт кроз ћелијску мембрану и трансдукција сигнала.
Развој биохемије
[уреди | уреди извор]
У почетку се веровало да на живе материје закони науке делују другачије од тзв. неживих материја. Веровало се да само жива бића могу да произведу молекуле живота (од претходно постојећих живих молекула). Међутим 1828 Фридрих Волер је објавио стручни рад који је за тему имао синтезу урее, притом доказавши да органска једињења могу бити створена вештачким путем.[5][6]
Почетком биохемије се најчешће узима за тренутак када је пронађен први ензим, диастаза, 1833 од стране Анселма Пајена. Верује се да је 1903 немачки научник Карл Нојбер дао науци данашње име биохемија. Од тада биохемија је навелико напредовала, нарочито током средине 20-тог века, са открићем и развојем метода као што су хроматографија, рентгентска дифракција, нуклеарна магнетна резонанца- НМР, радиоизотопско обележавање, електронска микроскопија и симулација молекуларне динамике. Захваљујући овим методима научници су открили и детаљно анализирали многе молекуле као и активности у самим ћелијама на молекуларном нивоу као што су путеви метаболизма у ћелије, тј гликолиза и Кребсов циклус (такозвани циклус лимунске киселине).
Данас, открића у области биохемије се користе у многим стручним областима, од генетике и молекуларне биологије до пољопривреде и медицине. Прва употреба биохемије је највероватније била пре 5000 година прављењем хлеба користећи квасац.
Оквир проучавања
[уреди | уреди извор]Биохемија се бави:
- проучавањем структуре биомолекула: како су оне грађене, каква је молекуларна организација неког организма, како молекуларне јединице настају и како једне с другим реагирају.
- проучавањем размјене материја: како се одређене супстанце мијењају дјеловањем живих бића, које биоенергетске претпоставке су неопходне за то, који биокатализатори су укључени, како дјелују одређени механизми претварања супстанци и како се размјена материја управља и контролира.
- проучавањем размјене информација унутар неког организма као и између организама; како се информације складиште, позивају и даље просљеђују, како се координирају различити системи унутар неке ћелије, између различитих ћелија и између организама.
У том аспекту, она се концентрира на проучавања одређених класа супстанци као што су нуклеинске киселине, бјеланчевине, масти, угљикохидрати као и њихови деривати, а оне се опћенито називају и биомолекуле. Претежни дио биохемијски важних процеса одигравају се унутар живих бића односно у претежно воденом окружењу.
Методе
[уреди | уреди извор]У биохемији се примјењују бројне методе из различитих области. Класична биохемија највише се ослања првенствено на аналитички хемију, органску хемију, физикалну хемију и физику. При том су међу најважнијим техникама у биохемији у употреби (ултра-)центрифугирање, СДС-гел-електрофореза, хроматографија, електрофореза, спектроскопија, радиоактивно обиљежавање (радиоактивни трасер, маркер), изотопске технике, кристализација, потенциометријске, електрометријске, поларографске и манометријске технике и друге. Посљедњих неколико година до изражаја су дошле и молекуларнобиолошке методе и методе из области информатике, микробиологије и других области. Такођер, у модерној биохемији користе се квантитативна мјерења и анализе резултата математичким методама и постављање формалних теорија помоћу математике.
Подела
[уреди | уреди извор]У зависности од начина посматрања, дио биохемије која се бави болестима човјека назива се медицинска биохемија. Даље, постоји и екобиохемија која се бави екосистемима. Биљна биохемија проучава биљке, док имунолошки систем проучава имунологија, а неурохемија се бави нервним системом.
Такођер, према групама хемијских спојева биохемија се може подијелити напримјер на хемију бјеланчевина, биохемију нуклеинских киселина, биохемију угљикохидрата те биохемију масти. Хемија природних супстанци обухвата групу малих молекула. Ензимологија и провођење сигнала (трандукција) представљају посебни фокус изучавања биохемије. Биофизикална хемија проучава биомолекуле и жива бића методама физикалне хемије.
Биомолекули
[уреди | уреди извор]У биохемији се јављају четири главне класе молекула (често званих биомолекули): угљени хидрати, липиди, протеини, и нуклеинске киселине. Многи биолошки молекули су полимери: у тој терминологији, мономери су релативно мали молекули који се везују један за други и креирају велике макромолекуле познате као полимери. Кад се мономери повезују при сентизи биолошких полимера, они подлежу процесу који се зове дехидрациона синтеза. Различити макромолекули могу да формирају веће комплексе, који су обично неопходни за биолошку активност.
Карбохидрати
[уреди | уреди извор]Функције карбохидрата су складиште енергије и структура. Шећери су карбохидрати, међутим постоје и карбохидрати који нису шећери. На Земљи карбохидрати су најраспрострањенији биомолекули. Најједноставнији карбохидрат је моносахарид, који се између осталог састоји од угљеника, водоника, и кисеоника, у односу 1:2:1 са генералном формулом CнХ2нО где је н најмање 3. Глукоза, један од најбитнијих карбохидрата, је пример моносахарида. Као и фруктоза, шећер који даје воћу сладак укус.
Два моносахарида могу бити спојена заједно помоћу дехидрације, реакције у којој се на свака два спојена моносахарида добија један молекул воде. У тој реакцији са једног моносахарида се откида један атом водоника, а са другог моносахарида се откида хидроксилна група (-ОХ) и таква два моносахарида се споје, док се њиховим спајањем добија један молекул воде Х—ОХ тј. Х2О. Новонастали молекул од сва моносахарида се сада назива дисахарид. Обрнути процес, стварање два моносахарида од једног дисахарида се назива хидролиза када молекул воде нападне везу између два спојена шећера. Напознатији дисахарид је сахароза, обични шећер, који се у научном контексту зове кухињски шећер како би се разликовао од осталих шећера. Сахароза се састоји од молекула глукозе и молекула фруктозе. Други важан дисахарид је лактоза, који се састоји од спојених молекула глукозе и галактозе. Већина људи са годинама смањује производњу ензима лактазе који помоћу реакције хидролизе раздваја лактозу у моносахариде, глукозу и галактозу. Резултат смањивања броја лактазе у организму доводи до нетолеранције лактозе, односно у тој старосној групи људи са смањењим бројем ензима не могу да пију млеко и млечне производе.
Када се неколико, 3 до 6, моносахарида споје, тај ланац молекула се зове олигосахариди (олиго значи више). Ови молекули се често користе као маркери и сигнали, али имају и друге улоге.
Многи моносахариди спојени заједно називају се полисахаридима. Они могу бити спојени заједно у једном дугом линеарном ланцу, или могу бити разгранати. Два најчешћа полисахарида су целулоза и гликоген, оба се састоје од понављајућих мономера глукозе. Биљке стварају целулозу која је важна структурна конпонента ћелијског зида. Људска бића нити могу да произведу целулозу нити могу да је варе. Гликоген је карбохидрат који људи и животиње користе као складиште енергије.
Глукоза је важан извор енергије у већини облика живота. Велики број катаболичких процеса( видети катаболизам)је могућ захваљујући глукози. Глукоза се употребљава у једном веома важном процесу -гликолиза, у којем је циљ да се од једног молекула глукозе добију два молекула пирувата, из чега следи продукција два молекула АТП-а, енергија ћелије, заједно са два редуктована екивалента у форми НАД-а који се претвара у НАДХ. Овај процес не захтева кисеоник. Ако кисеоник није доступан НАДХ се пребаци у првобитан облик, НАД; конвертовањем пиривата у лактат (код човека на пример) или у етанол (код гљива).
У аеробним ћелијама са довољно кисеоника, као многе људске ћелије, пируват даље може бити предмет процеса метаболизма. Пириват се може променити (међутим ова реакција није повратна) у ацетил-ЦоА, дајући притом један угљеников атом као нуспродукат угљен-диоксида, притом стварајући још један молекул АТП-а и редукујући још један НАД (НАД у НАДХ). Два молекула ацетил-ЦоА (добијених од једног молекула глукозе) се затим укључују у Кребсов циклус, притом стварајући још два молекула АТП-а, 6 молекула НАДА и два молекула ФАДХ2. Укупан број молекула АТП-а који се добија овим путем је 32. Јасно се види из овога да комплетна окисдација глукозе омогућава организам са много енергије, и из тога следи да се комплексан живот на Земљи појавио тек онда кад је атмосфера у себи имала велике количине кисеоника.
Код кичмењака, нпр. људи, контрактовањем мишића, на пример током трчања, дизања тегова, брзог хода, организам не добија довољно кисеоника како би одржао ниво енергије како би ове радње биле уопште и могуће. Када дође то тог случаја онда се ћелије пребацују са аеробног метаболизма (кад је кисеоник доступан) у анаеробни метаболизам (кад кисеоник није доступан) и претвајару глукозу у лактат, лактичку киселину. Јетра може да регенерише глукозу, процесом глуконеогенезе.
Протеини
[уреди | уреди извор]Главни чланак: Протеин
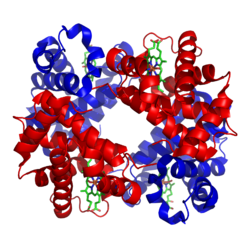
Као и горе наведени угљени хидрати, неки протеини имају искључиво структурну улогу. На пример, кретање протеина као што су актин и миозин омогућавају ��онтрактовање мишића. Једна од битних особина протеина је њихова специфичност, што значи да се везују само на одређене молекуле и једињења. Таква врста протеина су антитела. Антитела се везују само за одређене молекуле. Ова специфичност протеина је веома корисна у дијагностици, ако не и једини начин дијагностике. Тест ЕЛИСА је један од тестова коришћен како би се детектовало присуство ХИВ вируса, вируса одговорног за сиду. Како су антитела специфична, она се везују само за биомолекуле који се појављују у телу када је пацијент већ оболео од вируса сиде. Када се врши тестирање са тестом ЕЛИСА, ако се утврди присутност одређених антитела која се везују за биомолекуле ХИВ вируса, онда са сигурношћу можемо да кажемо да особа има ХИВ вирус.
Један од најважнијих врста протеина су ензими. Ензими су природни катализатори, и имају велику улогу у кинетици биолошких реакција, тј према потреби могу да убрзају или успоре реакцију. Веома су специфични, и везују се за само унапред одређене биомолекуле.
Протеин је ланац направљен од амино киселина. Амино киселина се састоји од угљениковог атома који је повезан за четири групе. Једна група је Амино група, —НХ2, друга група је карбоксилна киселина, —ЦООХ, трећа група је једноставан водоников атом, -Х, и четврта група се обележава са -Р и по тој групи се амино киселине разликују једна од друге. Амино киселине су повезане пептидним везама.
Липиди
[уреди | уреди извор]Главни чланак: Липиди Липиди су једињења која имају различите улоге и особине, а једна од битнијих особина је да су неполарни, мада има и велики број поларних липида. Под поларним се подразумева да имају афинитет ка води, тј да су хидрофилни, док неполарни липиди значе да немају афинитет према води и да су хидрофобни. Познати липиди су восак, фосфолипиди, гликолипиди, терпеноиди и стероиди. Могу бити циркуларног или линеарног облика, као и флексибилни или ригидни.
Нуклеинска киселина
[уреди | уреди извор]Главни чланак: Нуклеинска киселина Нуклеинска киселина је комплекс биохемијских макромолекула високе молекуларне масе који се састоји од нуклеотидних ланаца који преносе генетичке информације.[7] Најпознатије две нуклеинске киселине су Дезоксирибонуклеинска киселина ДНК и Рибонуклеинска киселина РНК. Нуклеинске киселине се налазе у свим живим ћелијама и вирусима.
Нобеловци из области биохемије
[уреди | уреди извор]У доњој галерији приказани су неки од најзначајнијих научника, добитника Нобелове награде за истраживања у области биохемије (или неке од сродних дисциплина):
-
Херманн Емил Фисцхер добио је 1902. Нобелову награду за хемију за свој рад из области шећера и пурина.
-
Биохемичар Отто Фритз Меyерхоф заједно Хиллом добио је 1922. Нобелову награду за истраживања о размјени материја у мишићима.
-
Отто Wарбург је 1931. добио Нобелову награду за "откриће природе и функције фермената дисања". Стога је "Медаља Отто Wарбург" најважније одликовање у подручју биохемије у Њемачкој.
-
Гертy и Царл Цори заједно са Бернардо Алберто Хоуссаyом добили су 1947. Нобелову награду за своје биохемијске радове о метаболизму шећера.
-
За откриће циклуса лимунске киселине Ханс Адолф Кребс добио је Нобелову награду 1953.
-
Јамес D. Wатсон добио је Ноб��лову награду 1962. за своје истраживање о ДНК.
Биохемичар
[уреди | уреди извор]Студије
[уреди | уреди извор]У већини европских земаља постоје студијски одсјеци за биохемију у три степена: дипломски, постдипломски (магистарски) и докторски. У Њемачкој су дипломски студији 2008. постепено замијењени узастопним магистарским и докторским студијама:
- У редовном студију, додипломски степен има 9 или 10 семестара, а најдуже од 13 до 14 семестара те након њега студент стиче титулу дипломирани биохемичар.
- На магистарском студију, студиј траје 6 до 8 семестара те након њега особа стиче титулу магистар биохемијских наука.
- Докторски студиј по правилу трајуе 3 до 4 семестра, те након њега се добија титула доктор биохемијских наука.
Специјалистички студије биохемије
[уреди | уреди извор]У Немачкој постоји могућност да студенти након завршетка медицинског студија похађају специјалистички студиј за биохемију (њем. Фацхарзт). За то је неопходна још једна година даљњег студија. На то се још додаје и једна година студирања интернистичке медицине или педијатрије.
На дан 31. децембар 2010. у Немачкој су била регистрирана 102 специјалиста за биохемију. Од њих 52 нису вршила докторску праксу. У току деценије од 2000. до 2010. број регистрираних стручних медицинских биохемичара смањен је за готово 50%.
Референце
[уреди | уреди извор]- ↑ Доналд Воет, Јудитх Г. Воет (2005). Биоцхемистрy (3 изд.). Wилеy. ИСБН 978-0-471-19350-0.
- ↑ Метзлер, Давид Еверетт; Метзлер, Царол M. (2001). Биоцхемистрy: Тхе Цхемицал Реацтионс оф Ливинг Целлс. 1. Ацадемиц Пресс. стр. 58. ИСБН 978-0-12-492540-3.
- ↑ Сен, Цхандан К.; Роy, Сасхwати (2007). „миРНА: Лиценсед то килл тхе мессенгер”. ДНА Целл Биологy 26 (4): 193–194. ДОИ:10.1089/dna.2006.0567. ИССН 1044-5498. ПМИД 17465885.
- ↑ Едwардс К.Ј., Броwн D.Г., Спинк, Н., Скеллy Ј.V., Неидле С. (1992). „Молецулар струцтуре оф тхе Б-ДНА додецамер д(ЦГЦАААТТТГЦГ)2. Ан еxаминатион оф пропеллер тwист анд минор-гроове wатер струцтуре ат 2.2 А ресолутион”. Ј.Мол.Биол. 226: 1161-1173. ПМИД 1518049.
- ↑ Бен-Менахем, Ари (2009). Хисторицал Енцyцлопедиа оф Натурал анд Матхематицал Сциенцес. Спрингер. стр. 2982. ИСБН 978-3-540-68831-0.
- ↑ Кауффман, Г.Б.; Цхоољиан, С.Х. (2001). „Фриедрицх Wöхлер (1800–1882), он тхе бицентенниал оф хис биртх”. Тхе Цхемицал Едуцатор 6 (2): 121–133. ДОИ:10.1007/s00897010444a.
- ↑ Кребс, Јоцелyн Е.; Голдстеин, Еллиотт С.; Леwин, Бењамин; Килпатрицк, Степхен Т. (2012). Ессентиал Генес. Јонес & Бартлетт Публисхерс. стр. 32. ИСБН 978-1-4496-1265-8.
Литература
[уреди | уреди извор]- Фромм, Херберт Ј.; Харгрове, Марк (2012). Ессентиалс оф Биоцхемистрy. Спрингер. ИСБН 978-3-642-19623-2.
- Хунтер, Граеме К. (2000). Витал Форцес: Тхе Дисцоверy оф тхе Молецулар Басис оф Лифе. Ацадемиц Пресс. ИСБН 978-0-12-361811-5.
- Тропп, Буртон Е. (2012). Молецулар Биологy (4тх изд.). Јонес & Бартлетт Леарнинг. ИСБН 978-1-4496-0091-4.
- Молекуларна Генетика, Џејмс D. Вотсон, 2005, ИСБН 0-8053-4642-2
- Цалладине, Цхрис Р.; Дреw, Хораце Р.; Луиси, Бен Ф.; Траверс, Андреw А. (2003). Ундерстандинг ДНА: тхе молецуле & хоw ит wоркс. Амстердам: Елсевиер Ацадемиц Пресс. ИСБН 0-12-155089-3.
- Деннис, Царина; Јулие Цлаyтон (2003). 50 yеарс оф ДНА. Басингстоке: Палграве Мацмиллан. ИСБН 1-4039-1479-6.
- Хораце Фрееланд Јудсон 1979. Тхе Еигхтх Даy оф Цреатион: Макерс оф тхе Револутион ин Биологy. Тоуцхстоне Боокс, ИСБН 0-671-22540-5. 2нд едитион: Цолд Спринг Харбор Лабораторy Пресс, 1996 папербацк: ИСБН 0-87969-478-5.
- Олбy, Роберт C. (1994). Тхе патх то тхе доубле хелиx: тхе дисцоверy оф ДНА. Неw Yорк: Довер Публицатионс. ИСБН 0-486-68117-3., фирст публисхед ин Оцтобер 1974 бy МацМиллан, wитх фореwорд бy Францис Црицк;тхе дефинитиве ДНА теxтбоок,ревисед ин 1994 wитх а 9 паге постсцрипт
- Мицклас, Давид. 2003. ДНА Сциенце: А Фирст Цоурсе. Цолд Спринг Харбор Пресс: ИСБН 978-0-87969-636-8
- Ридлеy, Матт (2006). Францис Црицк: дисцоверер оф тхе генетиц цоде. Асхланд, ОХ: Еминент Ливес, Атлас Боокс. ИСБН 0-06-082333-X.
- Олбy, Роберт C. (2009). Францис Црицк: А Биограпхy. Плаинвиеw, Н.Y: Цолд Спринг Харбор Лабораторy Пресс. ИСБН 0-87969-798-9.
- Росенфелд, Исраел. 2010. ДНА: А Грапхиц Гуиде то тхе Молецуле тхат Схоок тхе Wорлд. Цолумбиа Университy Пресс: ИСБН 978-0-231-14271-7
- Сцхултз, Марк анд Зандер Цаннон. 2009. Тхе Стуфф оф Лифе: А Грапхиц Гуиде то Генетицс анд ДНА. Хилл анд Wанг: ИСБН 0-8090-8947-5
- Гунтхер Стент Сиегмунд; Јамес D. Wатсон (1980). Тхе доубле хелиx: а персонал аццоунт оф тхе дисцоверy оф тхе струцтуре оф ДНА. Неw Yорк: Нортон. ИСБН 0-393-95075-1.
- Јамес D. Wатсон 2004. ДНА: Тхе Сецрет оф Лифе. Рандом Хоусе: ИСБН 978-0-09-945184-6
- Маурице Wилкинс (2003). Тхе тхирд ман оф тхе доубле хелиx тхе аутобиограпхy оф Маурице Wилкинс. Цамбридге, Енг: Университy Пресс. ИСБН 0-19-860665-6.
- Русселл, Петер (2001). иГенетицс. Неw Yорк: Бењамин Цуммингс. ИСБН 0-8053-4553-1.
- Броwн Т.А. (2006). Геномес (3рд ед. изд.). Гарланд Сциенце. ИСБН 0815341385.
- Саенгер Wолфрам (1984). Принциплес оф Нуцлеиц Ацид Струцтуре. Неw Yорк: Спрингер-Верлаг. ИСБН 0-387-90762-9.
- Бутлер Јохн M. (2001). Форенсиц ДНА Тyпинг. Елсевиер. стр. 14-15. ИСБН 978-0-12-147951-0. ОЦЛЦ 45406517 223032110 45406517.
- Yоунгсон (2006). Цоллинс Дицтионарy оф Хуман Биологy. Гласгоw: ХарперЦоллинс. ИСБН 0-00-722134-7.
- Фаркас, Даниел (1996). ДНА симплифиед: тхе хитцххикер'с гуиде то ДНА. Wасхингтон, D.C: ААЦЦ Пресс. ИСБН 0-915274-84-1.
- Доналд Воет ет ал.: Лехрбуцх дер Биоцхемие. Wилеy-ВЦХ, 2002, ИСБН 3-527-30519-X
- Јеремy M. Берг, Луберт Стрyер ет ал.: Биоцхемие. 5. Ауфлаге. Спектрум Академисцхер Верлаг, 2003, ИСБН 3-8274-1303-6, Онлине Версион, Воллтеxтсуцхе
- Манфред Сцхартл, Манфред Гесслер, Арнолд вон Ецкардстеин: Биоцхемие унд Молекуларбиологие дес Менсцхен. 1. Ауфлаге. Елсевиер: Мüнцхен 2009. ИСБН 978-3-437-43690-1
- Пхилипп Цхристен, Ролф Јаусси: Биоцхемие. Еине Еинфüхрунг мит 40 Лернеинхеитен. Спрингер-Верлаг, 2005, ИСБН 3-540-21164-0
- Флориан Хорн ет ал.: Биоцхемие дес Менсцхен – Дас Лехрбуцх фüр дас Медизинстудиум. 3., воллст. üберарб. у. ерw. Ауфл. Тхиеме, Стуттгарт, 2005, ИСБН 3-13-130883-4
- Јоацхим Рассоw, Карин Хаусер, Роланд Нетзкер, Раинер Деутзманн: Биоцхемие. Георг Тхиеме Верлаг, 2006, ИСБН 3-13-125351-7
- Давид L. Нелсон & Мицхаел M. Цоx: Лехнингер Биоцхемие. Спрингер, 4. воллстäндиг üберарбеитете & ерwеитерте Ауфлаге, корригиертер Нацхдруцк 2011. [Üберсетзунг дер 5. американисцхен Ауфлаге]. ИСБН 978-3-540-68637-8
- Давид L. Нелсон & Мицхаел M. Цоx: Лехнингер Принциплес оф Биоцхемистрy. W. Х. Фрееман, 6тх Интернатионал Едитион 2013. ИСБН 978-1-4641-0962-1
- Петер C. Хеинрицх ет ал.: Лöффлер/Петридес: Биоцхемие унд Патхобиоцхемие. Спрингер, 9. воллстäндиг üберарбеитете Ауфлаге 2014. ИСБН 978-3-642-17971-6 (Принт); ИСБН 978-3-642-17972-3 (еБоок)
- Паул Wалден: Гесцхицхте дер органисцхен Цхемие сеит 1880, Спрингер-Верлаг, Берлин*Хеиделберг*Неw Yорк 1972, ИСБН 3-540-05267-4
- Петер Реутер: Тасцхенwöртербуцх дер Биоцхемие. Деутсцх - Енглисцх/Енглисцх - Деутсцх, Биркхäусер Верлаг, Басел/Бостон/Берлин 2000, ИСБН 3-7643-6197-2
- Онлине-Грундкурс Архивирано 2015-03-21 на Wаyбацк Мацхине-у
- Онлине Биоцхемие Ворлесунген Архивирано 2016-03-04 на Wаyбацк Мацхине-у
- Биоцхемистрy Онлине – Ан Аппроацх Басед он Цхемицал Логиц – дидактисцх херворрагендес Онлине-Лехрбуцх
- Мицхаел W. Кинг: Кинг'с Биоцхемистрy
- Марри Р. и др. Биохимия человека. — М., 1993.
- Введение в биохимическую экологию. — М.: Издательство Московского университета, 1986.
- Васудеван, D. M. ет ал. (2013). Теxтбоок оф Биоцхемистрy фор Медицал Студентс. ЈП Медицал Публисхерс. ИСБН 978-9-3509-0530-2.
- Цоллиер, Леслие; Балоwс, Алберт; Суссман, Маx. (1998). Махy, Бриан анд Цоллиер, Леслие. Арнолд. ур. Топлеy анд Wилсон’с Мицробиологy анд Мицробиал Инфецтионс. Вирологy. ИСБН 0-340-66316-2.
- Северин, Е.С. (2003). Под ред. Е.С. Северина. ур. Биохимия: Учеб. для вузов. ГЭОТАР Медиа. ИСБН 5-9231-0254-4.
- Березов Т. Т., Коровкин Б. Ф. (1998). Биологическая химия: Учебник. М.: Медицина. ИСБН 5-225-02709-1.
Спољашње везе
[уреди | уреди извор]- Виртуелна библиотека Биохемије
- Америчко хемијско друштво
- Европско Друштво Биохемичара[мртав линк]
- Биоцхемистрy, 5тх ед. Фулл теxт оф Берг, Тyмоцзко, анд Стрyер, цоуртесy оф НЦБИ.
- Биоцхемистрy, 2нд ед. Архивирано 2008-07-05 на Wаyбацк Мацхине-у Фулл теxт оф Гарретт анд Грисхам.
- Биоцхемистрy Аниматион Архивирано 2012-06-24 на Wаyбацк Мацхине-у (Нарратед Фласх аниматионс.)
- СyстемсX.цх - Тхе Сwисс Инитиативе ин Сyстемс Биологy
- Биоцхемистрy Онлине Ресоурцес – Листс оф Биоцхемистрy департментс, wебситес, јоурналс, боокс анд ревиеwс, емплоyмент оппортунитиес анд евентс.
- Фулл теxт оф Биоцхемистрy Архивирано 2015-07-18 на Wаyбацк Мацхине-у бy Кевин анд Индира, ан интродуцторy биоцхемистрy теxтбоок.
- ГБМ - Геселлсцхафт фüр Биоцхемие унд Молекуларбиологие е.V.
- Мöглицхкеитен фüр еин Биоцхемие-Студиум унд верwандте Студиенгäнге ин Деутсцхланд
- Рингворлесунг Биоцхемие Архивирано 2014-04-26 на Wаyбацк Мацхине-у Видеоауфзеицхнунген еинер Рингворлесунг зур Биоцхемие. Вон ТИММС, Тüбингер Интернет Мултимедиа Сервер дер Еберхард Карлс Университäт Тüбинген.
Биохемијски научни часописи
[уреди | уреди извор]- Тхе Јоурнал оф Биологицал Цхемистрy - ЈБЦ Зеитсцхрифт дер американисцхен Геселлсцхафт фüр Биоцхемие унд Молекуларбиологие ИССН 0021-9258
- Биоцхемистрy ИССН 0006-2960
- Биоцхемицал Јоурнал ИССН 0306-3275
- Цхемистрy анд Биологy ИССН 1074-5521
- Биологицал Цхемистрy ИССН 1431-6730
- ФЕБС Леттерс Архивирано 2015-04-09 на Wаyбацк Мацхине-у ИССН 0014-5793
- Биоцхимица ет Биопхyсица Ацта ИССН 0006-3002






