Oganeson
118Og Oganeson | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Konfigurasi elektron oganeson | |||||||||||||
| Sifat umum | |||||||||||||
| Pengucapan | /oganèson/ | ||||||||||||
| Oganeson dalam tabel periodik | |||||||||||||
| |||||||||||||
| Nomor atom (Z) | 118 | ||||||||||||
| Golongan | golongan 18 | ||||||||||||
| Periode | periode 7 | ||||||||||||
| Blok | blok-p | ||||||||||||
| Kategori unsur | sebelumnya diperkirakan sebagai gas mulia, tetapi sekarang diprediksi berbentuk padatan reaktif yang tampak seperti logam, dan berupa semikonduktor (mungkin metaloid) atau logam miskin.[1][2] | ||||||||||||
| Nomor massa | [294] | ||||||||||||
| Konfigurasi elektron | [Rn] 5f14 6d10 7s2 7p6 (diprediksi)[3][4] | ||||||||||||
| Elektron per kelopak | 2, 8, 18, 32, 32, 18, 8 (diprediksi) | ||||||||||||
| Sifat fisik | |||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | padat (diprediksi)[5] | ||||||||||||
| Titik lebur | 325 ± 15 K (52 ± 15 °C, 125 ± 27 °F) (diprediksi)[5] | ||||||||||||
| Titik didih | 450 ± 10 K (177 ± 10 °C, 350 ± 18 °F) (diprediksi)[5] | ||||||||||||
| Kepadatan saat cair, pada t.l. | 6,6–7,4 g/cm3 (diprediksi)[5] | ||||||||||||
| Titik kritis | 439 K, 6,8 MPa (diekstrapolasi)[6] | ||||||||||||
| Kalor peleburan | 23,5 kJ/mol (diekstrapolasi)[6] | ||||||||||||
| Kalor penguapan | 19,4 kJ/mol (diekstrapolasi)[6] | ||||||||||||
| Sifat atom | |||||||||||||
| Bilangan oksidasi | (−1),[4] (0), (+1),[7] (+2),[8] (+4),[8] (+6)[4] (diprediksi) | ||||||||||||
| Energi ionisasi | ke-1: 860,1 kJ/mol (diprediksi)[9] ke-2: 1560 kJ/mol (diprediksi)[10] | ||||||||||||
| Jari-jari atom | empiris: 152 pm (diprediksi)[11] | ||||||||||||
| Jari-jari kovalen | 157 pm (diprediksi)[12] | ||||||||||||
| Lain-lain | |||||||||||||
| Kelimpahan alami | sintetis | ||||||||||||
| Struktur kristal | kubus berpusat muka (fcc) (diekstrapolasi)[13] | ||||||||||||
| Nomor CAS | 54144-19-3 | ||||||||||||
| Sejarah | |||||||||||||
| Penamaan | dari Yuri Oganessian | ||||||||||||
| Prediksi | Hans J. Thomsen (1895) | ||||||||||||
| Penemuan | Joint Institute for Nuclear Research dan Laboratorium Nasional Lawrence Livermore (2002) | ||||||||||||
| Isotop oganeson yang utama | |||||||||||||
| |||||||||||||
Oganesson adalah unsur kimia sintetis dengan simbol Og dan nomor atom 118. Unsur ini pertama kali disintesis pada tahun 2002 di Joint Institute for Nuclear Research (JINR) di Dubna, dekat Moskow, Rusia, oleh tim gabungan ilmuwan Rusia dan Amerika. Pada Desember 2015, ia diakui sebagai salah satu dari empat unsur baru oleh Joint Working Party dari badan ilmiah internasional IUPAC dan IUPAP. Unsur ini secara resmi dinamai pada 28 November 2016.[16][17] Nama ini menghormati fisikawan nuklir Yuri Oganessian, yang berperan penting dalam penemuan unsur-unsur terberat di tabel periodik. Ini adalah salah satu dari hanya dua unsur yang dinamai sesuai nama orang yang masih hidup pada saat penamaan, yang lainnya adalah seaborgium, dan satu-satunya unsur yang eponimnya masih hidup hingga 2024[update].[18][a]
Oganesson memiliki nomor atom dan massa atom tertinggi dari semua unsur yang diketahui hingga 2024[update]. Dalam tabel periodik unsur, ini adalah unsur p-block, anggota dari golongan 18 dan anggota terakhir dari periode 7. Isotopnya yang diketahui, oganesson-294, sangat radioaktif, dengan waktu paruh 0,7 ms dan, hingga 2020,[update] hanya lima atom yang berhasil diproduksi.[20] Hal ini sejauh ini mencegah studi eksperimental tentang kimianya. Karena efek relativistik, studi teoretis memprediksi bahwa unsur ini akan menjadi padat pada suhu ruangan, dan sangat reaktif,[20][3] tidak seperti anggota lain dari golongan 18 (gas mulia).
Sejarah
[sunting | sunting sumber]Spekulasi awal
[sunting | sunting sumber]Fisikawan Denmark Niels Bohr adalah orang pertama yang mempertimbangkan dengan serius kemungkinan sebuah unsur dengan nomor atom tinggi sebesar 118. Dalam catatannya pada tahun 1922, unsur ini akan berada di bawah radon dalam tabel periodik sebagai gas mulia ketujuh.[21] Setelah itu, Aristid von Grosse menulis sebuah artikel pada tahun 1965 yang memprediksi sifat-sifat yang kemungkinan dimiliki unsur 118 ini. Prediksi Bohr maupun van Grosse tergolong sangat spekulatif, karena cara sintesis unsur belum diketahui pada 1922, dan belum ada teori "pulau stabilitas" untuk unsur-unsur berat sampai tahun 1965. Unsur ini kelak disintesis pada 2002 (80 tahun setelah prediksi Bohr), dan saat itu sifat kimianya belum diselidiki sehingga tidak diketahui apakah ia benar bersifat seperti gas mulia seperti prediksi tersebut.[10]
Klaim penemuan yang tidak terkonfirmasi
[sunting | sunting sumber]Pada akhir 1998, fisikawan Polandia Robert Smolańczuk menulis perhitungan-perhitungan mengenai fusi inti-inti atom untuk sintesis atom super berat, termasuk oganeson.[22] Menurut hasil perhitungannya, ada kemungkinan oganeson dapat dibuat dengan menggabungkan timbal dengan kripton dalam kondisi yang dikendalikan secara ketat. Ia juga memprediksi bahwa peluang terjadinya reaksi ini akan hampir sama dengan peluang terjadinya reaksi fusi timbal dan kromium yang sebelumnya berhasil mensintesis unsur 106, seaborgium. Perhitungan ini bertentangan dengan prediksi-prediksi sebelumnya bahwa peluang reaksi fusi yang melibatkan timbal atau bismut akan menurun secara eksponensial jika nomor atom dari hasil reaksi fusi tersebut meningkat.[22]
Pada akhir 1998, para peneliti di Lawrence Berkeley National Laboratory menggunakan prediksi Smolańczuk dan melaporkan penemuan unsur livermorium dan oganeson dalam jurnal Physical Review Letters,[23] segera setelah hasil ini dilaporkan dalam jurnal Science.[24] Mereka melaporkan telah melakukan reaksi berikut
Namun, tahun berikutnya, mereka mencabut laporan tersebut karena hasil ini tidak dapat diulang, baik oleh peneliti di laboratorium lain, maupun ketika eksperimen itu diulang oleh laboratorium yang sama.[25] Pada bulan Juni 2002, direktur laboratorium tersebut mengakui bahwa data yang digunakan dalam laporan awal penemuan ini ternyata dipalsukan oleh penulis utama Victor Ninov.[26][27]
Laporan penemuan
[sunting | sunting sumber]Peluruhan pertama atom oganeson diamati pada tahun 2002 di Joint Institute for Nuclear Research (JINR) di Dubna, Rusia, oleh tim gabungan ilmuwan Rusia dan Amerika. Dipimpin oleh fisikawan nuklir Rusia Yuri Oganessian, tim tersebut melibatkan ilmuwan Amerika dari Lawrence Livermore National Laboratory, Kalifornia.[28] Pada tanggal 9 Oktober 2006, para peneliti mengumumkan[14] bahwa mereka secara tidak langsung telah mendeteksi secara total tiga (mungkin empat) inti oganeson-294 (satu atau dua pada tahun 2002[29] dan dua lagi pada tahun 2005) yang dihasilkan melalui tumbukan atom kalifornium-249 dan ion kalsium-48.[30][31][32][33][34]

Pada tahun 2011, IUPAC mengevaluasi hasil kerjasama peneliti Dubna dan Livermore pada tahun 2006 dan menyimpulkan: "Tiga peristiwa yang dilaporkan untuk isotop Z = 118 memiliki redundansi internal yang sangat baik, tetapi tanpa patokan kepada inti yang diketahui hal ini tidak memenuhi kriteria sebagai penemuan".[35]
Karena peluang reaksi fusi yang sangat kecil (penampang melintang fusi adalah ~0.3–0.6 pb atau ((3–6)×10−41 m2), percobaan ini memakan waktu empat bulan dan melibatkan dosis sinar sebesar 2,5×1019 ion kalsium yang harus ditembakan pada target kalifornium untuk menghasilkan peristiwa tercatat pertama yang diyakini sebagai sintesis oganeson.[36] Namun demikian, para peneliti sangat yakin bahwa hasilnya bukanlah positif palsu, karena kemungkinan deteksi seperti ini terjadi secara acak diperkirakan kurang dari 1:100.000.[37]
Pada percobaan-percobaan ini, peluruhan alfa dari tiga atom oganeson berhasil diamati. Ada juga yang mengatakan bahwa terjadi peluruhan dari satu atom lagi secara pembelahan spontan. Waktu paruh oganeson-294 sebesar 0,89 ms dan proses peluruhannya telah diketahui: 294Og meluruh 290Lv melalui peluruhan alfa. Karena hanya ada tiga inti, waktu paruh yang dihitung dari percobaan ini memiliki ketidakpastian yang besar, yaitu sebesar 0,89+1,07
−0,31 ms.[14]
Identifikasi inti atom ini sebagai 294Og diverifikasi dengan cara membuat inti 290Lv (yang diketahui merupakan hasil peluruhan 294Og) secara terpisah dengan cara membombardir 245Cm menggunakan ion 48Ca,
dan memeriksa bahwa peluruhan 290Lv yang dihasilkan dengan cara ini sesuai dengan rantai peluruhan inti atom294Og.[14] Hasil peluruhan ini sangat tidak stabil, meluruh dengan dengan waktu paruh 14 milidetik menjadi 286Fl, yang dapat mengalami pembelahan spontan atau peluruhan alfa menjadi 282Cn, yang akan kemudian mengalami pembelahan spontan.[14]
Dalam model penerowongan kuantum, waktu paruh 294Og sebelum terjadi peluruhan alfa diperkirakan 0,66+0,23
−0,18 ms[38] dengan nilai Q eksperimental yang diterbitkan pada tahun 2004[39] Perhitungan dengan nilai Q teoretis dari model makroskopis-mikroskopis Muntian-Hofman-Patyk-Sobiczewski memberikan hasil yang mirip tapi sedikit lebih rendah.[40]
Konfirmasi
[sunting | sunting sumber]Pada bulan Desember 2015, Kelompok Kerja Gabungan dari badan ilmiah internasional Persatuan Kimia Murni dan Terapan Internasional (IUPAC) dan Persatuan Fisika Murni dan Terapan Internasional (IUPAP) mengakui penemuan unsur oganeson dan menetapkan proyek kolaborasi Dubna dan Livermore sebagai penemunya.[41] Penetapan ini berdasarkan konfirmasi mengenai sifat-sifat 286Fl (cucu peluruhan dari 294Og), di Lawrence Berkeley National Laboratory, serta pengamatan rangkaian peluruhan 294Og lain oleh kelompok Dubna pada tahun 2012. Percobaan tersebut sebenarnya bertujuan mensintesis 294Ts melalui reaksi 249Bk(48Ca,3n), namun pendeknya waktu paruh 249Bk menyebabkan banyak inti tersebut meluruh menjadi 249Cf, sehingga sebagian hasil sintesis menjadi oganeson alih-alih semuanya menjadi tenesin.[42]
Dari 1 Oktober 2015 sampai 6 April 2016, tim Dubna melakukan percobaan serupa dengan menggunakan 48Ca untuk membombardir kalifornium dengan campuran isotop 249Cf, 250Cf, dan 251Cf, dengan tujuan menghasilkan isotop-isotop oganeson yang lebih berat yaitu 295Og dan 296Og. Digunakan dua tembakan berenergi 252 MeV dan 258 MeV. Hanya satu atom yang teramati pada 252 MeV, yang rantai peluruhannya cocok dengan yang sebelumnya diketahui dari 294Og (berakhir dengan pembelahan spontan 286Fl), dan tidak ada yang terlihat pada 258 MeV. Percobaan kemudian dihentikan, karena perekat dari bingkai sektor menutupi sasaran dan menghalangi residu penguapan untuk lolos ke alat pendeteksi. Tim Dubna berencana untuk mengulangi percobaan ini pada tahun 2017.[43]
Penamaan
[sunting | sunting sumber]
Dengan menggunakan tata nama Mendeleev untuk unsur tanpa nama yang belum ditemukan, oganeson kadang dikenal sebagai eka-radon (sebelum 1960an dikenal sebagai eka-emanasi, karena emanasi adalah nama lama radon).[13] Pada tahun 1979, IUPAC menggunakan nama sistematis ununoctium untuk unsur ini (yang saat itu belum ditemukan), dengan simbol Uuo,[44] dan menyarankan nama inilah yang dipakai hingga unsur ini ditemukan dan dikonfirmasi.[45] Meskipun nama ini banyak digunakan di komunitas kimia di semua tingkat, mulai dari kelas kimia hingga buku teks lanjutan, saran nama ini banyak diabaikan di kalangan ilmuwan di lapangan, yang menyebutnya "unsur 118", dengan simbol E118, (118), atau bahkan cukup 118.[4]
Sebelum pencabutan hasil percobaan pada tahun 2001, para periset dari Berkeley bermaksud memberi nama unsur ghiorsium (Gh), yang diambil dari Albert Ghiorso (salah satu pimpinan tim peneliti).[46]
Peneliti Rusia melaporkan sintesis mereka pada tahun 2006. Menurut rekomendasi IUPAC, penemu elemen baru memiliki hak untuk mengusulkan sebuah nama.[47] Pada tahun 2007, kepala institut Rusia tersebut menyatakan bahwa tim tersebut mempertimbangkan dua nama untuk elemen baru: flyorium, untuk menghormati Georgy Flyorov, pendiri laboratorium penelitian di Dubna; dan moskovium, sebagai pengakuan atas Oblast Moskow tempat Dubna berada.[48] Dia juga menyatakan bahwa meskipun unsur tersebut ditemukan melalu kerja sama dengan tim Amerika Serikat, yang menyediakan target kalifornium, unsur tersebut seharusnya diberi nama untuk menghormati Rusia karena Laboratorium Flerov di JINR adalah satu-satunya fasilitas di dunia yang dapat melakukan sintesis ini. Hasilnya,[49] nama-nama ini kemudian diusulkan untuk unsur 114 (flerovium) dan unsur 116 (moscovium).[50] Namun, akhirnya nama yang diajukan untuk unsur 116 malah livermorium,[51] dan nama moscovium kemudian diusulkan dan diterima untuk unsur 115 sebagai gantinya.[18]
Menurut tradisi, nama-nama semua gas mulia diakhiri dengan "-on", kecuali helium, yang tidak diketahui sebagai gas mulia saat ditemukan. Pedoman IUPAC yang berlaku pada saat diterimanya penemuan oganeson mengharuskan semua unsur baru diberi akhiran "ium, bahkan jika ternyata menjadi halogen (biasanya berakhir dengan " -in ") atau gas mulia (yang biasanya berakhir dengan "-on").[52] Nama sementara "ununoctium" mengikuti konvensi ini, tetapi sebuah rekomendasi IUPAC baru yang diterbitkan pada tahun 2016 menyarankan akhiran "-on" untuk unsur-unsur baru dari golongan 18 (VIIIA), terlepas dari apakah unsur-unsur tersebut ternyata memiliki sifat kimia seperti gas mulia.[53]
Pada bulan Juni 2016, IUPAC mengumumkan bahwa para penemu unsur 118 berencana untuk menamakannya oganeson (simbol: Og), untuk menghormati ahli fisika nuklir Rusia Yuri Oganessian, pelopor penelitian unsur-unsur super berat yang telah berkiprah selama 60 tahun sejak bidang tersebut baru dimulai. Tim Oganessian serta teknik yang diusulkannya adalah faktor penting dalam sintesis unsur 106 sampai 118.[54] Nama tersebut diresmikan pada tanggal 28 November 2016.[18] Oganessian kemudian menanggapi penamaan tersebut:[55]
Bagi saya, ini adalah sebuah kehormatan. Penemuan elemen 118 dilakukan oleh para ilmuwan di Joint Institute for Nuclear Research di Rusia dan di Lawrence Livermore National Laboratory di AS, dan rekan-rekan saya yang mengusulkan nama oganeson. Anak-anak dan cucu-cucu saya telah tinggal di AS selama berpuluh-puluh tahun, namun anak perempuan saya menulis kepada saya untuk mengatakan bahwa dia tidak bisa tidur pada malam setelah mendengar berita ini karena dia menangis.[55]
— Yuri Oganessian
Upacara penamaan moskovium, tenesin, dan oganeson diadakan pada 2 Maret 2017 di Akademi Ilmu Pengetahuan Rusia, Moskwa.[56]
Karakteristik
[sunting | sunting sumber]Kestabilan inti dan isotop
[sunting | sunting sumber]
Kestabilan inti sangat berkurang dengan bertambahnya nomor atom di atas 96 (nomor atom kurium, Cm). Semua isotop bernomor atom di atas 101 mengalami peluruhan radioaktif dengan waktu paruh dibawah 30 jam. Tidak ada unsur dengan nomor atom di atas 82 (timbal) memiliki isotop stabil.[57] Hal ini disebabkan terus meningkatnya gaya tolak Coulomb antara proton dalam inti-inti tersebut, sehingga gaya nuklir kuat tidak bisa lama menahan kecenderungan terjadinya pembelahan spontan. Jika hanya memperhitungkan faktor ini, seharusnya tidak mungkin ada unsur dengan jumlah proton (nomor atom) di atas 104. Namun penelitian yang dilakukan pada 1960an menunjukkan bahwa kulit nuklir dengan sekitar 114 proton dan 184 neutron dapat menanggulangi faktor ketidakstabilan di atas, sehingga muncullah konsep "pulau stabilitas" dalam fisika nuklir. Dalam "pulau" ini, inti-inti atom diperkirakan dapat memiliki waktu paruh mencapai ribuan bahkan jutaan tahun. Walaupun para ilmuwan belum mencapai pulau ini, keberadaan unsur-unsur superberat (termasuk oganeson) menunjukkan bahwa efek kestabilan ini nyata, dan inti-inti superberat yang sejauh ini ditemukan menunjukkan kenaikan waktu paruh yang eksponensial saat mendekati posisi "pulau" ini. Oganeson bersifat radioaktif dan memiliki waktu paruh yang sepertinya kurang dari satu milisekon. Namun, angka ini masih lebih tinggi dari beberapa prediksi,[38][58] sehingga menjadi salah satu bukti pendukung gagasan "pulau stabilitas" ini.[59]
Perhitungan menggunakan model penerowongan kuantum memprediksi keberadaan beberapa isotop kaya neutron dari oganeson yang memiliki waktu paruh alfa mendekati 1 ms.[60][61]
Perhitungan teoretis terhadap jalur sintetis maupun waktu paruh isotop-isotop lain menunjukkan kemungkinan isotop-isotop yang lebih stabil daripada 294Og, terutama 293Og, 295Og, 296Og, 297Og, 298Og, 300Og dan 302Og.[38][62] Dari isotop-isotop ini, peluang terbesar untuk mendapatkan isotop berumur lebih panjang agaknya ada pada 297Og,[38][62] dan penelitian oganeson di masa depan mungkin akan difokuskan pada isotop ini. Isotop-isotop yang lebih kaya neutron lagi, terutama isotop-isotop di sekitar 313Og, juga dapat menghasilkan inti berumur panjang.[63] Karena isotop-isotop berat berumur panjang ini akan sangat memudahkan penelitian kimia terhadap oganeson, tim Dubna berencana untuk melakukan percobaan selama paruh kedua tahun 2017 dengan menggunakan campuran isotop 249Cf, 250Cf, dan 251Cf yang ditembak dengan 48Ca, dengan tujuan sintesis isotop baru 295Og dan 296Og; lalu pada tahun 2020 direncanakan penelitian serupa untuk menghasilkan 297Og. Reaksi ini juga dapat menghasilkan 293Og dan putrinya 289Lv. Isotop 295Og dan 296Og juga dapat diproduksi melalui fusi inti 248Cm dengan tembakan 50Ti; reaksi ini direncanakan di JINR dan di RIKEN pada tahun 2017–2018.[43][64][65]
Perhitungan sifat atom dan fisik
[sunting | sunting sumber]Oganeson adalah anggota golongan 18 atau VIIIA, unsur-unsur tanpa elektron valensi. Anggota golongan 18 biasanya bersifat inert dalam reaksi-reaksi kimia yang umum (misalnya, pembakaran) karena kulit valensi terluarnya terisi penuh elektron. Hal ini menyebabkan energi minimum yang stabil, dengan elektron terluar yang terikat erat.[66] Oganeson diperkirakan memiliki sifat yang sama, dan kulit elektron terluarnya terisi penuh dengan elektron valensi berkonfigurasi 7s27p6.[3]
Akibatnya, beberapa peneliti memperkirakan oganeson memiliki sifat fisik dan kimia yang serupa dengan anggota golongan 18, terutama radon, gas mulia tepat berada di atas unsur ini dalam tabel periodik.[67] Mengikuti tren periodik, oganeson diperkirakan bersifat sedikit lebih reaktif daripada radon. Namun, perhitungan teoretis menunjukkan bahwa unsur ini bisa jadi jauh lebih reaktif. Selain itu, oganeson bahkan mungkin lebih reaktif daripada unsur flerovium dan kopernisium, yang berada di sebelah kiri oganeson dan di bawah unsur-unsur yang lebih reaktif yaitu timbal dan raksa.[3] Faktor yang menyebabkan kemungkinan ini adalah karena subkulit terluarnya, yaitu subkulit 7p, memiliki kestabilan energi yang lebih rendah dan jari-jari yang lebih besar.[3][b] Lebih tepatnya, interaksi spin–orbit antara elektron-elektron 7s yang inert dengan elektron-elektron 7p menyebabkan penutupan kulit kedua, dan penurunan yang signifikan dalam kestabilan kulit oganeson yang penuh.[3] Selain itu, perhitungan juga menunjukkan bahwa oganeson, tak seperti gas mulia lainnya, mengikat elektron dengan pelepasan energi–dengan kata lain, oganeson memiliki afinitas elektron yang bernilai positif,[68][69][c] disebabkan tingkat energi 8s yang terstabilkan secara relativistik dan tingkat energi 7p3/2 yang berkurang kestabilannya.[70]
Oganeson diperkirakan memiliki polarisabilitas terbesar dari semua elemen sebelum berada di tabel periodik, hampir dua kali lipat dari radon.[3] Dengan mengekstrapolasi dari gas mulia lainnya, diperkirakan oganeson memiliki titik didih antara 320 dan 380 K.[3] Ini sangat berbeda dengan nilai yang diperkirakan sebelumnya sebesar 263 K[71] atau 247 K.[72] Bahkan dengan ketidakpastian perhitungan yang besar, tampaknya sangat tidak mungkin oganeson akan menjadi gas di bawah kondisi standar,[3] dan karena kisaran cairan gas lainnya sangat sempit (antara 2 dan 9 kelvin), unsur ini seharusnya berbentuk padat pada kondisi standar. Jika oganeson membentuk gas pada kondisi standar, bagaimanapun, gas tersebut akan menjadi salah satu gas terpadat pada kondisi standar, bahkan jika gasnya monoatomik seperti gas mulia lainnya.
Karena polarisabilitasnya yang amat besar, oganeson diperkirakan memiliki energi ionisasi yang anehnya rendah (serupa dengan timbal yang energi ionisasinya sekitar 70% radon[7] dan jauh lebih kecil daripada flerovium[73]) dan fase terkondensasi pada keadaan standar.[3] Meskipun struktur kelopak pada inti dan awan elektron oganeson sangat dipengaruhi oleh efek relativistik: subkelopak elektron utama dan valensi dalam oganeson diperkirakan akan "terselimuti" oleh gas Fermi homogen dari elektron, akibat pemisahan orbit-orbit 7p yang sangat kuat dalam oganeson. Efek yang sama untuk nukleon, terutama neutron, adalah paling ringan pada kelopak neutron tertutup untuk inti 302Og dan sangat kuat pada inti hipotetis nukleotida tertutup superberat 472164, dengan 164 proton dan 308 neutron.[74]
Prediksi senyawa
[sunting | sunting sumber]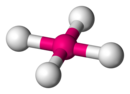
Tidak ada senyawa oganeson yang telah disintesis, namun perhitungan senyawa teoretis telah dilakukan sejak 1964.[13] Diharapkan bahwa jika energi ionisasi elemen cukup tinggi, akan sulit untuk mengoksidasi dan oleh karena itu, bilangan oksidasi yang paling umum adalah 0 (sama seperti gas mulia lainnya);[75] Namun, ini tampaknya tidak kasusnya.[10]
Perhitungan pada molekul diatomik Og2 menunjukkan interaksi ikatan kira-kira setara dengan yang dihitung untuk Hg2, dan energi disosiasi 6 kJ/mol, kira-kira 4 kalinya Rn2.[3] Tapi yang paling mencolok, setelah dihitung senyawa ini memiliki panjang ikatan yang lebih pendek 0,16 Å daripada Rn2, yang mengindikasikan adanya interaksi ikatan yang signifikan.[3] Di sisi lain, senyawa OgH+ menunjukkan energi disosiasi (afinitas proton oganeson) yang lebih kecil dari RnH+.[3]
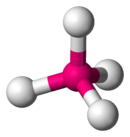
Ikatan antara oganeson dan hidrogen (OgH) diperkirakan sangat lemah dan dapat dianggap sebagai interaksi van der Waals murni dan bukan ikatan kimiawi yang sebenarnya.[7] Di sisi lain, dengan unsur yang sangat elektronegatif, oganeson tampaknya membentuk senyawa yang lebih stabil daripada kopernisium atau flerovium.[7] Keadaan oksidasi stabil +2 dan +4 diperkirakan di fluorida OgF2 dan OgF4.[76] Keadaan +6 akan kurang stabil karena ikatan kuat subkulit 7p1/2. Ini adalah hasil interaksi spin-orbit yang sama yang membuat oganeson biasanya tidak reaktif. Sebagai contoh, ditunjukkan bahwa reaksi oganeson dengan F2 untuk membentuk senyawa OgF2 akan melepaskan energi 106 kkal/mol dimana sekitar 46 kkal/mol berasal dari interaksi ini.[7] Sebagai perbandingan, interaksi spin-orbit untuk molekul serupa RnF2 adalah sekitar 10 kkal/mol dari energi pembentukan 49 kkal/mol.[7] Interaksi yang sama menstabilkan konfigurasi Td tetrahedral untuk OgF4, berbeda dari planar kuadrat D4h satu dari XeF4, yang diharapkan juga dimiliki oleh RnF4.[10] Ikatan Og-F paling mungkin bersifat ionik dan bukan kovalen, menghasilkan fluorida oganeson yang tidak mudah menguap.[8][77] OgF2 diprediksi akan ionik parsial karena sifat elektropositivitasnya yang tinggi.[78] Berbeda dengan gas mulia lainnya (kecuali mungkin xenon dan radon),[79][80] oganeson diperkirakan cukup elektropositif[78] untuk membentuk ikatan Og-Cl dengan klorin.[8]
Lihat pula
[sunting | sunting sumber]Catatan
[sunting | sunting sumber]- ^ Nama einsteinium dan fermium untuk unsur 99 dan 100 diusulkan saat nama mereka (Albert Einstein dan Enrico Fermi) masih hidup, tetapi tidak resmi sampai Einstein dan Fermi meninggal dunia.[19]
- ^ Kutipan sebenarnya adalah "Alasan untuk peningkatan aktivitas kimiawi unsur 118 yang relatif terhadap radon adalah destabilisasi energik dan perluasan radial dari kulit yang ditempati 7p3 / 2spinor."
- ^ Namun, koreksi elektrodinamika kuantum telah terbukti cukup signifikan. dalam mengurangi afinitas ini dengan mengurangi pengikatan anion Og – sebesar 9%, dengan demikian menegaskan pentingnya koreksi elemen superheavy ini. Lihat Pyykkö.
Referensi
[sunting | sunting sumber]- ^ Mewes, Jan-Michael; Smits, Odile Rosette; Jerabek, Paul; Schwerdtfeger, Peter (25 Juli 2019). "Oganesson is a Semiconductor: On the Relativistic Band‐Gap Narrowing in the Heaviest Noble‐Gas Solids". Angewandte Chemie. doi:10.1002/anie.201908327. Diakses tanggal 11 Agustus 2022.
- ^ Gong, Sheng; Wu, Wei; Wang, Fancy Qian; Liu, Jie; Zhao, Yu; Shen, Yiheng; Wang, Shuo; Sun, Qiang; Wang, Qian (8 Februari 2019). "Classifying superheavy elements by machine learning". Physical Review A. 99: 022110–1–7. doi:10.1103/PhysRevA.99.022110.
- ^ a b c d e f g h i j k l m Nash, Clinton S. (2005). "Atomic and Molecular Properties of Elements 112, 114, and 118". Journal of Physical Chemistry A. 109 (15): 3493–3500. doi:10.1021/jp050736o. PMID 16833687.
- ^ a b c d Hoffman, Darleane C.; Lee, Diana M.; Pershina, Valeria (2006). "Transactinides and the future elements". Dalam Morss; Edelstein, Norman M.; Fuger, Jean. The Chemistry of the Actinide and Transactinide Elements (edisi ke-3). Dordrecht, The Netherlands: Springer Science+Business Media. ISBN 978-1-4020-3555-5.
- ^ a b c d Smits, Odile; Mewes, Jan-Michael; Jerabek, Paul; Schwerdtfeger, Peter (2020). "Oganesson: A Noble Gas Element That Is Neither Noble Nor a Gas". Angew. Chem. Int. Ed. 59 (52): 23636–23640. doi:10.1002/anie.202011976. PMC 7814676
 . PMID 32959952.
. PMID 32959952.
- ^ a b c Eichler, R.; Eichler, B., Thermochemical Properties of the Elements Rn, 112, 114, and 118 (PDF), Paul Scherrer Institut, diakses tanggal 11 Agustus 2022
- ^ a b c d e f Han, Young-Kyu; Bae, Cheolbeom; Son, Sang-Kil; Lee, Yoon Sup (2000). "Spin–orbit effects on the transactinide p-block element monohydrides MH (M=element 113–118)". Journal of Chemical Physics. 112 (6): 2684. Bibcode:2000JChPh.112.2684H. doi:10.1063/1.480842.
- ^ a b c d Kaldor, Uzi; Wilson, Stephen (2003). Theoretical Chemistry and Physics of Heavy and Superheavy Elements. Springer. hlm. 105. ISBN 978-1402013713. Diakses tanggal 6 Agustus 2022.
- ^ Pershina, Valeria (30 November 2013). "Theoretical Chemistry of the Heaviest Elements". Dalam Schädel, Matthias; Shaughnessy, Dawn. The Chemistry of Superheavy Elements (edisi ke-2). Springer Science & Business Media. hlm. 154. ISBN 9783642374661.
- ^ a b c d Fricke, Burkhard (1975). "Superheavy elements: a prediction of their chemical and physical properties". Recent Impact of Physics on Inorganic Chemistry. 21: 89–144. doi:10.1007/BFb0116498. Diakses tanggal 11 Agustus 2022.
- ^ Oganesson, American Elements
- ^ Oganesson - Element information, properties and uses, Royal Chemical Society
- ^ a b c Grosse, A. V. (1965). "Some physical and chemical properties of element 118 (Eka-Em) and element 86 (Em)". Journal of Inorganic and Nuclear Chemistry. Elsevier Science Ltd. 27 (3): 509–19. doi:10.1016/0022-1902(65)80255-X.
- ^ a b c d e f Oganessian, Yu. Ts.; Utyonkov, V. K.; Lobanov, Yu. V.; Abdullin, F. Sh.; Polyakov, A. N.; Sagaidak, R. N.; Shirokovsky, I. V.; Tsyganov, Yu. S.; et al. (2006-10-09). "Synthesis of the isotopes of elements 118 and 116 in the 249Cf and 245Cm+48Ca fusion reactions". Physical Review C. 74 (4): 044602. Bibcode:2006PhRvC..74d4602O. doi:10.1103/PhysRevC.74.044602. Diakses tanggal 11 Agustus 2022.
- ^ Oganessian, Yuri Ts.; Rykaczewski, Krzysztof P. (August 2015). "A beachhead on the island of stability". Physics Today. 68 (8): 32–38. Bibcode:2015PhT....68h..32O. doi:10.1063/PT.3.2880. OSTI 1337838.
- ^ "IUPAC Announces the Names of the Elements 113, 115, 117, and 118". IUPAC. 30 November 2016. Diarsipkan dari versi asli tanggal 30 November 2016. Diakses tanggal 1 December 2015.
- ^ St. Fleur, Nicholas (1 December 2016). "Four New Names Officially Added to the Periodic Table of Elements"
 . The New York Times. Diakses tanggal 1 December 2016.
. The New York Times. Diakses tanggal 1 December 2016.
- ^ a b c "IUPAC Is Naming The Four New Elements Nihonium, Moscovium, Tennessine, And Oganesson". IUPAC. 8 June 2016. Diarsipkan dari versi asli tanggal 8 June 2016.
- ^ Hoffman, Ghiorso & Seaborg 2000, hlm. 187–189.
- ^ a b Smits, Odile R.; Mewes, Jan-Michael; Jerabek, Paul; Schwerdtfeger, Peter (2020). "Oganesson: A Noble Gas Element That Is Neither Noble Nor a Gas". Angewandte Chemie International Edition. 59 (52): 23636–23640. doi:10.1002/anie.202011976
 . PMC 7814676
. PMC 7814676  . PMID 32959952.
. PMID 32959952.
- ^ Leach, Mark R. "The INTERNET Database of Periodic Tables" (dalam bahasa Inggris). Diakses tanggal 8 Juli 2016.
- ^ a b Smolanczuk, R. (1999). "Production mechanism of superheavy nuclei in cold fusion reactions". Physical Review C (dalam bahasa Inggris). 59 (5): 2634–2639. Bibcode:1999PhRvC..59.2634S. doi:10.1103/PhysRevC.59.2634.
- ^ Ninov, Viktor (1999). "Observation of Superheavy Nuclei Produced in the Reaction of 86Kr with 208Pb". Physical Review Letters (dalam bahasa Inggris). 83 (6): 1104–1107. Bibcode:1999PhRvL..83.1104N. doi:10.1103/PhysRevLett.83.1104. (Dicabut)
- ^ Service, R. F. (1999). "Berkeley Crew Bags Element 118". Science (dalam bahasa Inggris). 284 (5421): 1751. doi:10.1126/science.284.5421.1751.
- ^ Public Affairs Department (21 Juli 2001). "Results of element 118 experiment retracted" (dalam bahasa Inggris). Berkeley Lab. Diakses tanggal 18 Januari 2008.
- ^ Dalton, R. (2002). "Misconduct: The stars who fell to Earth". Nature (dalam bahasa Inggris). 420 (6917): 728–729. Bibcode:2002Natur.420..728D. doi:10.1038/420728a. PMID 12490902.
- ^ Element 118 disappears two years after it was discovered Diarsipkan 2007-10-12 di Wayback Machine.. Physicsworld.com. Diakses pada 2 April 2012.
- ^ Oganessian, Yu. T.; et al. (2002). "Results from the first 249Cf+48Ca experiment" (PDF). JINR Communication (dalam bahasa Inggris). JINR, Dubna.
- ^ Oganessian, Yu. T.; et al. (2002). "Element 118: results from the first Cf + Ca experiment" (dalam bahasa Inggris). Communication of the Joint Institute for Nuclear Research. Diarsipkan dari versi asli tanggal 22 Juli 2011.
- ^ "Livermore scientists team with Russia to discover element 118". Livermore press release. 3 Desember 2006. Diarsipkan dari versi asli tanggal 2011-10-17. Diakses tanggal 18 Januari 2008.
- ^ Oganessian, Yu. T. (2006). "Synthesis and decay properties of superheavy elements". Pure Appl. Chem. (dalam bahasa Inggris). 78 (5): 889–904. doi:10.1351/pac200678050889.
- ^ Sanderson, K. (2006). "Heaviest element made – again". Nature News (dalam bahasa Inggris). Nature. doi:10.1038/news061016-4.
- ^ Schewe, P. & Stein, B. (17 Oktober 2006). "Elements 116 and 118 Are Discovered". Physics News Update (dalam bahasa Inggris). American Institute of Physics. Archived from the original on 1 Januari 2012. Diakses tanggal 18 Januari 2008.
- ^ Weiss, R. (17 Oktober 2006). "Scientists Announce Creation of Atomic Element, the Heaviest Yet" (dalam bahasa Inggris). Washington Post. Diakses tanggal 18 Januari 2008.
- ^ Barber, Robert C.; Karol, Paul J.; Nakahara, Hiromichi; Vardaci, Emanuele; Vogt, Erich W. (2011). "Discovery of the elements with atomic numbers greater than or equal to 113 (IUPAC Technical Report)". Pure and Applied Chemistry (dalam bahasa Inggris). 83 (7): 1. doi:10.1351/PAC-REP-10-05-01.
- ^ "Ununoctium" (dalam bahasa Inggris). WebElements Periodic Table. Diakses tanggal 9 Desember 2007.
- ^ Jacoby, Mitch (17 Oktober 2006). "Element 118 Detected, With Confidence". Chemical & Engineering News (dalam bahasa Inggris). Diakses tanggal 18 Januari 2008.
I would say we're very confident.
- ^ a b c d Chowdhury, Roy P.; Samanta, C.; Basu, D. N. (2006). "α decay half-lives of new superheavy elements". Phys. Rev. C (dalam bahasa Inggris). 73: 014612. arXiv:nucl-th/0507054
 . Bibcode:2006PhRvC..73a4612C. doi:10.1103/PhysRevC.73.014612.
. Bibcode:2006PhRvC..73a4612C. doi:10.1103/PhysRevC.73.014612.
- ^ Oganessian, Yu. Ts.; Utyonkov, V.; Lobanov, Yu.; Abdullin, F.; Polyakov, A.; Shirokovsky, I.; Tsyganov, Yu.; Gulbekian, G.; Bogomolov, S.; Gikal, B. N.; et al. (2004). "Measurements of cross sections and decay properties of the isotopes of elements 112, 114, and 116 produced in the fusion reactions 233,238U, 242Pu, and 248Cm+48Ca". Physical Review C (dalam bahasa Inggris). 70 (6): 064609. Bibcode:2004PhRvC..70f4609O. doi:10.1103/PhysRevC.70.064609.
- ^ Samanta, C.; Chowdhury, R. P.; Basu, D.N. (2007). "Predictions of alpha decay half-lives of heavy and superheavy elements". Nucl. Phys. A (dalam bahasa Inggris). 789: 142–154. arXiv:nucl-th/0703086
 . Bibcode:2007NuPhA.789..142S. doi:10.1016/j.nuclphysa.2007.04.001.
. Bibcode:2007NuPhA.789..142S. doi:10.1016/j.nuclphysa.2007.04.001.
- ^ Discovery and Assignment of Elements with Atomic Numbers 113, 115, 117 and 118 Diarsipkan 2015-12-31 di Wayback Machine.. IUPAC (30 Desember 2015)
- ^ Karol, Paul J.; Barber, Robert C.; Sherrill, Bradley M.; Vardaci, Emanuele; Yamazaki, Toshimitsu (29 Desember 2015). "Discovery of the element with atomic number Z = 118 completing the 7th row of the periodic table (IUPAC Technical Report)" (PDF). Pure Appl. Chem. (dalam bahasa Inggris). 88 (1–2): 155–160. doi:10.1515/pac-2015-0501. Diakses tanggal 2 April 2016.
- ^ a b Voinov, A. A.; Oganessian, Yu. Ts; Abdullin, F. Sh.; Brewer, N. T.; Dmitriev, S. N.; Grzywacz, R. K.; Hamilton, J. H.; Itkis, M. G.; Miernik, K.; Polyakov, A. N.; Roberto, J. B.; Rykaczewski, K. P.; Sabelnikov, A. V.; Sagaidak, R. N.; Shriokovsky, I. V.; Shumeiko, M. V.; Stoyer, M. A.; Subbotin, V. G.; Sukhov, A. M.; Tsyganov, Yu. S.; Utyonkov, V. K.; Vostokin, G. K. (2016). "Results from the Recent Study of the 249–251Cf + 48Ca Reactions". Dalam Peninozhkevich, Yu. E.; Sobolev, Yu. G. Exotic Nuclei: EXON-2016 Proceedings of the International Symposium on Exotic Nuclei. Exotic Nuclei (dalam bahasa Inggris). hlm. 219–223. ISBN 9789813226555.
- ^ Chatt, J. (1979). "Recommendations for the Naming of Elements of Atomic Numbers Greater than 100". Pure Appl. Chem. 51 (2): 381–384. doi:10.1351/pac197951020381.
- ^ Wieser, M.E. (2006). "Atomic weights of the elements 2005 (IUPAC Technical Report)". Pure Appl. Chem. (dalam bahasa Inggris). 78 (11): 2051–2066. doi:10.1351/pac200678112051.
- ^ "Discovery of New Elements Makes Front Page News" (dalam bahasa Inggris). Berkeley Lab Research Review Summer 1999. 1999. Diakses tanggal 18 Januari 2008.
- ^ Koppenol, W. H. (2002). "Naming of new elements (IUPAC Recommendations 2002)" (PDF). Pure and Applied Chemistry (dalam bahasa Inggris). 74 (5): 787. doi:10.1351/pac200274050787.
- ^ "New chemical elements discovered in Russia`s Science City" (dalam bahasa Inggris). 12 Februari 2007. Diakses tanggal 9 Februari 2008.
- ^ Yemel'yanova, Asya (17 Desember 2006). "118-й элемент назовут по-русски (118th element will be named in Russian)" (dalam bahasa Rusia). vesti.ru. Diarsipkan dari versi asli tanggal 2008-12-25. Diakses tanggal 18 Januari 2008.
- ^ "Российские физики предложат назвать 116 химический элемент московием (Russian Physicians Will Suggest to Name Element 116 Moscovium)" (dalam bahasa Rusia). rian.ru. 2011. Diakses tanggal 8 Mei 2011.
- ^ "News: Start of the Name Approval Process for the Elements of Atomic Number 114 and 116". International Union of Pure and Applied Chemistry (dalam bahasa Inggris). Archived from the original on 23 Agustus 2014. Diakses tanggal 2 Desember 2011.
- ^ Koppenol, W. H. (2002). "Naming of new elements (IUPAC Recommendations 2002)" (PDF). Pure and Applied Chemistry. 74 (5): 787–791. doi:10.1351/pac200274050787.
- ^ Koppenol, Willem H.; Corish, John; García-Martínez, Javier; Meija, Juris; Reedijk, Jan (2016). "How to name new chemical elements (IUPAC Recommendations 2016)". Pure and Applied Chemistry (dalam bahasa Inggris). 88 (4). doi:10.1515/pac-2015-0802.
- ^ "What it takes to make a new element". Chemistry World (dalam bahasa Inggris). Diakses tanggal 3 Desember 2016.
- ^ a b Gray, Richard (11 April 2017). "Mr Element 118: The only living person on the periodic table". New Scientist (dalam bahasa Inggris). Diakses tanggal 26 April 2017.
- ^ Fedorova, Vera (3 Maret 2017). "At the inauguration ceremony of the new elements of the Periodic table of D.I. Mendeleev". jinr.ru (dalam bahasa Inggris). Joint Institute for Nuclear Research. Diakses tanggal 4 Februari 2018.
- ^ de Marcillac, Pierre; Coron, Noël; Dambier, Gérard; Leblanc, Jacques; Moalic, Jean-Pierre (April 2003). "Experimental detection of α-particles from the radioactive decay of natural bismuth". Nature. 422 (6934): 876–878. Bibcode:2003Natur.422..876D. doi:10.1038/nature01541. PMID 12712201.
- ^ Oganessian, Yu. T. (2007). "Heaviest nuclei from 48Ca-induced reactions". Journal of Physics G: Nuclear and Particle Physics. 34 (4): R165–R242. Bibcode:2007JPhG...34..165O. doi:10.1088/0954-3899/34/4/R01.
- ^ "New Element Isolated Only Briefly" (dalam bahasa Inggris). The Daily Californian. 18 Oktober 2006. Diarsipkan dari versi asli tanggal 23 Agustus 2014. Diakses tanggal 18 Januari 2008.
- ^ Chowdhury, Roy P.; Samanta, C.; Basu, D. N. (2008). "Search for long lived heaviest nuclei beyond the valley of stability". Physical Review C (dalam bahasa Inggris). 77 (4): 044603. arXiv:0802.3837
 . Bibcode:2008PhRvC..77d4603C. doi:10.1103/PhysRevC.77.044603.
. Bibcode:2008PhRvC..77d4603C. doi:10.1103/PhysRevC.77.044603.
- ^ Chowdhury, R. P.; Samanta, C.; Basu, D.N. (2008). "Nuclear half-lives for α -radioactivity of elements with 100 ≤ Z ≤ 130". Atomic Data and Nuclear Data Tables (dalam bahasa Inggris). 94 (6): 781–806. arXiv:0802.4161
 . Bibcode:2008ADNDT..94..781C. doi:10.1016/j.adt.2008.01.003.
. Bibcode:2008ADNDT..94..781C. doi:10.1016/j.adt.2008.01.003.
- ^ a b Royer, G.; Zbiri, K.; Bonilla, C. (2004). "Entrance channels and alpha decay half-lives of the heaviest elements". Nuclear Physics A. 730 (3–4): 355–376. arXiv:nucl-th/0410048
 . Bibcode:2004NuPhA.730..355R. doi:10.1016/j.nuclphysa.2003.11.010.
. Bibcode:2004NuPhA.730..355R. doi:10.1016/j.nuclphysa.2003.11.010.
- ^ Duarte, S. B.; Tavares, O. A. P.; Gonçalves, M.; Rodríguez, O.; Guzmán, F.; Barbosa, T. N.; García, F.; Dimarco, A. (2004). "Half-life predictions for decay modes of superheavy nuclei" (PDF). Journal of Physics G: Nuclear and Particle Physics (dalam bahasa Inggris). 30 (10): 1487–1494. Bibcode:2004JPhG...30.1487D. doi:10.1088/0954-3899/30/10/014.
- ^ Sychev, Vladimir (8 Februari 2017). "Юрий Оганесян: мы хотим узнать, где кончается таблица Менделеева" [Yuri Oganessian: we want to know where the Mendeleev table ends]. RIA Novosti (dalam bahasa Rusia). Diakses tanggal 31 Maret 2017.
- ^ Roberto, J. B. (31 Maret 2015). "Actinide Targets for Super-Heavy Element Research" (PDF). cyclotron.tamu.edu (dalam bahasa Inggris). Texas A & M University. Diakses tanggal 28 April 2017.
- ^ Bader, Richard F.W. "An Introduction to the Electronic Structure of Atoms and Molecules" (dalam bahasa Inggris). McMaster University. Diakses tanggal 18 Januari 2008.
- ^ "Ununoctium (Uuo) – Chemical properties, Health and Environmental effects" (dalam bahasa Inggris). Lenntech. Diarsipkan dari versi asli tanggal 16 Januari 2008. Diakses tanggal 18 Januari 2008.
- ^ Goidenko, Igor; Labzowsky, Leonti; Eliav, Ephraim; Kaldor, Uzi; Pyykko¨, Pekka (2003). "QED corrections to the binding energy of the eka-radon (Z=118) negative ion". Physical Review A (dalam bahasa Inggris). 67 (2): 020102(R). Bibcode:2003PhRvA..67b0102G. doi:10.1103/PhysRevA.67.020102.
- ^ Eliav, Ephraim; Kaldor, Uzi; Ishikawa, Y.; Pyykkö, P. (1996). "Element 118: The First Rare Gas with an Electron Affinity". Physical Review Letters (dalam bahasa Inggris). 77 (27): 5350–5352. Bibcode:1996PhRvL..77.5350E. doi:10.1103/PhysRevLett.77.5350. PMID 10062781.
- ^ Landau, Arie; Eliav, Ephraim; Ishikawa, Yasuyuki; Kador, Uzi (25 Mei 2001). "Benchmark calculations of electron affinities of the alkali atoms sodium to eka-francium (element 119)" (PDF). Journal of Chemical Physics (dalam bahasa Inggris). 115 (6): 2389–92. Bibcode:2001JChPh.115.2389L. doi:10.1063/1.1386413. Diakses tanggal 15 September 2015.
- ^ Seaborg, Glenn Theodore (1994). Modern Alchemy. World Scientific. hlm. 172. ISBN 981-02-1440-5.
- ^ Takahashi, N. (2002). "Boiling points of the superheavy elements 117 and 118". Journal of Radioanalytical and Nuclear Chemistry (dalam bahasa Inggris). 251 (2): 299–301. doi:10.1023/A:1014880730282.
- ^ Nash, Clinton S.; Bursten, Bruce E. (1999). "Spin-Orbit Effects, VSEPR Theory, and the Electronic Structures of Heavy and Superheavy Group IVA Hydrides and Group VIIIA Tetrafluorides. A Partial Role Reversal for Elements 114 and 118". Journal of Physical Chemistry A (dalam bahasa Inggris). 1999 (3): 402–410. Bibcode:1999JPCA..103..402N. doi:10.1021/jp982735k.
- ^ Jerabek, Paul; Schuetrumpf, Bastian; Schwerdtfeger, Peter; Nazarewicz, Witold (29 September 2017). "Electron and Nucleon Localization Functions of Oganesson: Approaching the Fermi-Gas Limit" (dalam bahasa en). arΧiv:1707.08710v2 [nucl-th].
- ^ "Ununoctium: Binary Compounds" (dalam bahasa Inggris). WebElements Periodic Table. Diakses tanggal 18 Januari 2008.
- ^ Han, Young-Kyu; Lee, Yoon Sup (1999). "Structures of RgFn (Rg = Xe, Rn, and Element 118. n = 2, 4.) Calculated by Two-component Spin-Orbit Methods. A Spin-Orbit Induced Isomer of (118)F4". Journal of Physical Chemistry A (dalam bahasa Inggris). 103 (8): 1104–1108. Bibcode:1999JPCA..103.1104H. doi:10.1021/jp983665k.
- ^ Pitzer, Kenneth S. (1975). "Fluorides of radon and element 118". Journal of the Chemical Society, Chemical Communications (18): 760–761. doi:10.1039/C3975000760b.
- ^ a b Seaborg, Glenn Theodore (sktr. 2006). "transuranium element (chemical element)" (dalam bahasa Inggris). Encyclopædia Britannica. Diakses tanggal 16 Maret 2010.
- ^ 张青莲 (November 1991). 《无机化学丛书》第一卷:稀有气体、氢、碱金属 (dalam bahasa Tionghoa). Beijing: Science Press. hlm. P72. ISBN 7-03-002238-6.
- ^ Proserpio, Davide M.; Hoffmann, Roald; Janda, Kenneth C. (1991). "The xenon-chlorine conundrum: van der Waals complex or linear molecule?". Journal of the American Chemical Society (dalam bahasa Inggris). 113 (19): 7184. doi:10.1021/ja00019a014.
Bacaan lebih lanjut
[sunting | sunting sumber]- Scerri, Eric (2007). The Periodic Table, Its Story and Its Significance (dalam bahasa Inggris). New York: Oxford University Press. ISBN 978-0-19-530573-9.
Pranala luar
[sunting | sunting sumber]- Element 118: experiments on discovery, archive of discoverers' official web page
- It's Elemental: Oganesson
- Oganesson di The Periodic Table of Videos (University of Nottingham)
- On the Claims for Discovery of Elements 110, 111, 112, 114, 116, and 118 (IUPAC Technical Report)
- "Element 118, Heaviest Ever, Reported for 1,000th of a Second", NYTimes.com.
- WebElements: Oganesson
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||






