Inosinmonophosphat
Inosinmonophosphat (IMP) ist ein Nukleotid und der Phosphorsäureester des Nukleosids Inosin. IMP ist ein zentrales Intermediat des Purinstoffwechsels in allen Lebewesen.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
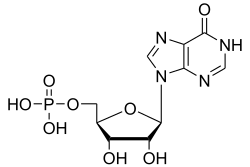
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Inosinmonophosphat | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C10H13N4O8P | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 348,21 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest[2] | |||||||||||||||||||||
| pKS-Wert |
2,4[3] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Eigenschaften
BearbeitenFarbloser Sirup mit angenehm fleischigem Geschmack (umami). Der Sirup geht bei Trocknung über Schwefelsäure in eine glasige Masse über.[4]
Physiologie
BearbeitenIMP ist zentrales Zwischenprodukt bei der Biosynthese der Purinnukleotide AMP und GMP sowie vollständig interkonvertibel mit beiden Stoffen.
Biosynthese
BearbeitenDie Biosynthese erfolgt entweder de-novo in 11 Schritten aus α-D-Ribose-5-phosphat – der letzte Reaktionsschritt ist hierbei die Formylierung und Cyclisierung von AICAR – oder wesentlich effizienter über den Salvage-Pathway direkt aus Hypoxanthin. Katalysierende Enzyme sind dabei die AICAR-Formyltransferase/IMP-Cyclase beziehungsweise die Hypoxanthin-Guanin-Phosphoribosyltransferase.[5][6]
Weiter entsteht IMP beim Abbau von AMP durch Desaminierung mithilfe der AMP-Desaminase und durch Reduktion von GMP mittels der GMP-Reduktase.[7]
Metabolismus
BearbeitenIMP ist Ausgangssubstanz für die Synthese von AMP (über Adenylosuccinat) und GMP (über Xanthosin-5'-monophosphat, XMP). Es wird bei Stickstoffüberschuss über Inosin in vier Schritten zu Harnsäure abgebaut und im Urin ausgeschieden.[8]
Verwendung
BearbeitenInosinmonophosphat wird wie auch das Dinatrium-, Dikalium- und Calciumsalz als Geschmacksverstärker (E 630, E 631, E 632 und E 633) eingesetzt. Trotz des geringen Eigengeschmacks besitzt Inosinmonophosphat eine ausgeprägte Wirkung als Geschmacksverstärker. Bei gemeinsamer Verwendung von Inosinmonophosphat mit Glutamat wird die geschmacksverstärkende Wirkung von Glutamat aufgrund synergistischer Effekte erheblich erhöht. Inosinmonophosphat findet als Geschmacksverstärker in Form des Natriumsalzes weit verbreitete Anwendung in der Nahrungsmittelindustrie, z. B. in Suppen- und Soßenprodukten sowie Fleischkonserven. Inosinmonophosphat wurde im Fleischextrakt bereits 1847 von Justus von Liebig nachgewiesen, der auch die geschmacksverstärkende Wirkung des Inosinmonophosphats erwähnte.[4]
Weblinks
BearbeitenEinzelnachweise
Bearbeiten- ↑ Eintrag zu E 630: Inosinic acid in der Europäischen Datenbank für Lebensmittelzusatzstoffe, abgerufen am 11. August 2020.
- ↑ a b c d Datenblatt Inosine 5′-monophosphate from Saccharomyces cerevisiae bei Sigma-Aldrich, abgerufen am 7. Februar 2021 (PDF).
- ↑ a b Eintrag zu Inosinic acid in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- ↑ a b Eintrag zu Inosin-5′-monophosphat. In: Römpp Online. Georg Thieme Verlag, abgerufen am 22. Dezember 2014.
- ↑ D'Eustachio / reactome: 5'-phosphoribosyl-5-aminoimidazole-4-carboxamide (AICAR) + 10-formyltetrahydrofolate ⇒ 5'-phosphoribosyl-5-formaminoimidazole-4-carboxamide (FAICAR) + tetrahydrofolate.
- ↑ Jassal / reactome: 5'-phosphoribosyl-5-formaminoimidazole-4-carboxamide (FAICAR) ⇔ inosine 5'-monophosphate + H2O.
- ↑ reactome: adenosine 5'-monophosphate (AMP) + H2O ⇒ inosine 5'-monophosphate (IMP) + NH4+ (L isoform).
- ↑ D'Eustachio / reactome: inosine 5'-monophosphate (IMP) + NAD+ + H2O ⇒ xanthosine 5'-monophosphate (XMP) + NADH + H+.