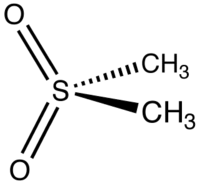
Méthyl-sulfonyl-méthane
| Méthyl-sulfonyl-méthane | |
| |
  |
|
| Identification | |
|---|---|
| Nom UICPA | méthyl-sulfonyl-méthane |
| Synonymes |
diméthylsulfone |
| No CAS | |
| No ECHA | 100.000.605 |
| No CE | 200-665-9 |
| No RTECS | PB2785000 |
| PubChem | 6213 |
| SMILES | |
| InChI | |
| Apparence | cristal incolore[1] |
| Propriétés chimiques | |
| Formule | C2H6O2S [Isomères] |
| Masse molaire[2] | 94,133 ± 0,008 g/mol C 25,52 %, H 6,42 %, O 33,99 %, S 34,06 %, |
| Propriétés physiques | |
| T° fusion | 107-110 °C[1] |
| T° ébullition | 238 °C[1],[3] |
| Solubilité | eau : 150 g·l-1[1],[3] |
| Masse volumique | 1,17 g·cm-3[4] |
| Précautions | |
| NFPA 704 | |
| Écotoxicologie | |
| DL50 | 5 000 mg·kg-1 (rat, oral)[5] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le méthyl-sulfonyl-méthane (MSM) ou la diméthylsulfone (DMSO2) est un composé organique de la famille des sulfones ; c'est un métabolite du diméthylsulfoxyde (DMSO). On le trouve dans de nombreux aliments et il est normalement présent dans le corps humain[6],[7];
Il est utilisé comme complément alimentaire dans l'alimentation animale, et chez l'Homme comme antalgique contre les douleurs articulaires d'origine inflammatoire (arthrose...)[8]. Il est supposé renforcer le collagène qui diminue avec l'âge. Son efficacité n'a pas été démontrée, mais des recherches émergentes semblent indiquer qu'il pourrait être utilisé dans le traitement d'appoint des inflammations osseuses[9]. C'est un composé dérivé du diméthylsulfoxyde, qui lui présente des applications médicales reconnues.
Synthèse et propriétés
[modifier | modifier le code]
Comme toutes les sulfones organiques, la diméthylsulfone est obtenue via l'oxydation de sulfure de diméthyle avec de l'eau oxygénée, H2O2 qui fournit également le produit intermédiaire, diméthylsulfoxyde, DMSO, O=S(CH3)2
Le MSM et le sulfoxyde correspond, le DMSO ont des propriétés physiques très différentes, la diméthylsufone est un solide cristallin incolore à température ambiante (p.f. 109 °C) tandis que le DMSO est un liquide (p.f. 19 °C) qui est un solvant aprotique très polaire, miscible à l'eau et qui est également un bon ligand. La diméthylsulfone est moins réactive que le DMSO car son atome de soufre est déjà dans son plus haut degré d'oxydation (IV). Ainsi, l'oxydation du sulfoxyde produit la sulfone aussi bien au laboratoire que métaboliquement[10].
Le MSM est trouvé dans de très nombreux organismes vivants (plantes et animaux, inclus les humains) et les produits qui en contiennent beaucoup inclus le lait de vache (3,3 ppm) ou le café (1,6 ppm).
Utilisation comme solvant
[modifier | modifier le code]En raison de sa polarité et de sa stabilité thermique, le MSM est utilisé industriellement comme solvant à haute température de substances inorganiques et organiques. Il est utilisé comme moyen de synthèse organique.
Par exemple, le déplacement de chlorures d'aryle par le fluorure de potassium peut être réalisé dans du MSM fondu[11].
Avec un pKa de 31, il peut être déprotoné avec de l'amidure de sodium, et la base conjuguée est un nucléophile efficace.
Pharmacologie et toxicité
[modifier | modifier le code]La DL50 du MSM est supérieure à 17,5 grammes par kilogramme de poids corporel.
Chez le rat, aucun événement indésirable n'a été observé après des doses quotidiennes de 2 g de MSM par kg de poids corporel. Dans une étude de suivi de 90 jours, les rats ont reçu des doses quotidiennes de MSM de 1,5 g/kg, et aucun changement n'a été observé en termes de symptômes, de chimie sanguine ou de pathologie macroscopique[12].
Des études de résonance magnétique nucléaire (RMN) ont démontré que les doses orales de MSM sont absorbées dans le sang et traversent la barrière hémato-encéphalique[13],[14]. Une étude RMN a également trouvé des niveaux détectables de MSM normalement présents dans le sang et le liquide céphalo-rachidien, suggérant qu'il provient de l'alimentation, du métabolisme du microbiote intestinal et du métabolisme endogène du méthanethiol du corps[15].
Les essais cliniques publiés sur le MSM n'ont pas signalé d'effet secondaire grave, mais il n'y a pas de données évaluées par les pairs sur les effets de son utilisation à long terme chez l'homme.
Usage comme complément alimentaire
[modifier | modifier le code]Chez l'animal
[modifier | modifier le code]Le MSM est utilisé dans l'alimentation animale[16]. La FDA le reconnait comme source de soufre bio assimilable[17].
- Chez le porc, de manière significative, il diminue les teneurs de la viande en Na, Mg et Ca (par rapport aux régimes sans supplément), mais augmente les teneurs en Fe, Cu et Zn tout en augmentant la teneur en soufre de la viande (ce qui lui donnerait un gout plus persillé), sans modifier la teneur en acides aminés, mais en augmentant les acides gras saturés et en diminuant les acides gras insaturés dans le muscle.
- Il a aussi été testé chez le cheval (par le dépositaire d'un brevet) [18]
- chez le poulet, il accélère la croissance, améliore le profil sanguin et la qualité de la viande, et semble favorable au microbiote[16].
- chez le canard, il améliore la qualité de la viande (alors plus protéique et plus riche en soufre, avec une meilleure capacité de rétention d'eau, et diminuant la perte d'humidité et de substances réactives à l'acide thiobarbiturique lors du stockage à froid)[19].
Chez l'Homme
[modifier | modifier le code]Dans les années 1980, il est considéré comme une bonne source de soufre (élément notamment nécessaire à la synthèse de 2 acides aminés essentiels : la cystéine et de la méthionine[20],[21].
Un usage thérapeutique du MSM a été envisagé à la fin des années 1970, en raison de sa proximité avec le DMSO. Des brevets (déposés par le Dr Robert Herschler dans les années 1980) lui ont attribué de multiples bénéfices pour la santé, bien que les preuves scientifiques se bornaient alors à une certaine efficacité comme anti-inflammatoire[9]. Son usage se répand aux États-Unis suite à la publication de deux livres[22], The Miracle of MSM: The Natural Solution for Pain en 1999[23], et MSM: The Definitive Guide, en 2002[24]. Stanley Jacob, l'auteur, est aussi dépositaire d'un brevet pour l'usage du MSM contre le ronflement. Le marketing commercial qui présente le MSM moyen de traiter la douleur ostéoarthritique et la rhinite allergique[25],[26] a conduit la FDA à avertir qu'elle ne lui a trouvé ni preuve d'efficacité, ni d'innocuité à long terme[27].
En 2012, l'EFSA, après avoir examiné les allégations de bénéfices sur la santé à la lumière des études scientifiques publiées, estime qu'aucun bénéfice n'a été prouvé de manière satisfaisante et interdit que les compléments alimentaires au MSM se prévalent d'effets thérapeutiques en Europe[28]. Il reste utilisé en médecine vétérinaire, dans les traitements contre l'arthrite pour les chevaux et les chiens.
Références
[modifier | modifier le code]- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Methylsulfonylmethane » (voir la liste des auteurs).
- Entrée « Dimethylsulfone » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 16 octobre 2016 (JavaScript nécessaire)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Fiche Dimethylsulfone », Merck [PDF] (consulté le ).
- (de) « Dimethylsulfon », sur Römpp Online, Georg Thieme Verlag (consulté le )
- (en) « Méthyl-sulfonyl-méthane », sur ChemIDplus
- A.C. Silva Ferreira, P. Rodrigues, T. Hogg, P. Guedes de Pinho Influence of some technological parameters on the formation of dimethyl sulfide, 2-mercaptoethanol, methionol, and dimethyl sulfone in port wines J. Agric. Food Chem., 51 (2003), p. 727-732
- U.F. Engelke, A. Tangerman, M.A. Willemsen, D. Moskau, S. Loss, S.H. Mudd, R.A. Wevers Dimethyl sulfone in human cerebrospinal fluid and blood plasma confirmed by one-dimensional 1 H and two-dimensional 1 H-13 C NMR. Biome., 18 (2005), p. 331-336
- « Msm (Methylsulfonylmethane): Uses, Side Effects, Interactions, Dosage, and Warning », sur webmd.com (consulté le ).
- Matthew Butawan, Rodney L. Benjamin et Richard J. Bloomer, « Methylsulfonylmethane: Applications and Safety of a Novel Dietary Supplement », Nutrients, vol. 9, no 3, (ISSN 2072-6643, PMID 28300758, PMCID PMC5372953, DOI 10.3390/nu9030290, lire en ligne, consulté le )
- X. He, C. M. Slupsky, Metabolic fingerprint of dimethyl sulfone (DMSO2) in microbial-mammalian co-metabolism, Journal of Proteome Research, 2014, vol. 13(12), p. 5281–5292. DOI 10.1021/pr500629t, .
- Georges Hareau et Philip Kocienski, Encyclopedia of Reagents for Organic Synthesis, (ISBN 978-0-471-93623-7, DOI 10.1002/047084289X.rd371), « Dimethyl Sulfone »
- Horváth K, Noker PE, Somfai-Relle S, Glávits R, Financsek I, Schauss AG, « Toxicity of methylsulfonylmethane in rats », Food and Chemical Toxicology, vol. 40, no 10, , p. 1459–62 (PMID 12387309, DOI 10.1016/S0278-6915(02)00086-8)
- Rose SE, Chalk JB, Galloway GJ, Doddrell DM, « Detection of dimethyl sulfone in the human brain by in vivo proton magnetic resonance spectroscopy », Magnetic Resonance Imaging, vol. 18, no 1, , p. 95–8 (PMID 10642107, DOI 10.1016/S0730-725X(99)00110-1)
- Lin A, Nguy CH, Shic F, Ross BD, « Accumulation of methylsulfonylmethane in the human brain: identification by multinuclear magnetic resonance spectroscopy », Toxicology Letters, vol. 123, nos 2–3, , p. 169–77 (PMID 11641045, DOI 10.1016/S0378-4274(01)00396-4)
- Engelke UF, Tangerman A, Willemsen MA, Moskau D, Loss S, Mudd SH, Wevers RA, « Dimethyl sulfone in human cerebrospinal fluid and blood plasma confirmed by one-dimensional (1)H and two-dimensional (1)H-(13)C NMR », NMR in Biomedicine, vol. 18, no 5, , p. 331–6 (PMID 15996001, DOI 10.1002/nbm.966)
- Jiao, Y., Park, J. H., Kim, Y. M., & Kim, I. H. (2017). Effects of dietary methyl sulfonyl methane (MSM) supplementation on growth performance, nutrient digestibility, meat quality, excreta microbiota, excreta gas emission, and blood profiles in broilers. Poultry science, 96(7), 2168-2175.
- U.S. Food and Drug Administration (2004) Guidance for Industry: Botanical Drug Products., http://www.fda.gov/downloads/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/ucm070491.pdf
- Herschler R.J (1986) MSM: a Nutrient for the Horse. Eq. Vet. Data, 7(7)268
- Hwang, J. W., Cheong, S. H., Kim, Y. S., Lee, J. W., You, B. I., Moon, S. H., ... & Park, P. J. (2017). Effects of dietary supplementation of oriental herbal medicine residue and methyl sulfonyl methane on the growth performance and meat quality of ducks. Animal production science, 57(5), 948-957 (résumé).
- V.L. Richmond (1986) Incorporation of methylsulfonylmethane sulfur into guinea pig serum proteins ; Life Sci, 39, p. 263-268 (résumé)
- Jacob, S. W (1983) The Current Status of MSM in Medicine. Am. Acad. Med. Prev
- « MSM - Sources naturelles, Bienfaits, Mensonges, Avis », sur passeportsante.net, (consulté le ).
- (en) Jacob S, Lawrence RM et Zucker M, The Miracle of MSM : The Natural Solution for Pain, États-Unis, Penguin-Putnam,
- (en) Jacob SW, et Appleton J, MSM : The Definitive Guide, États-Unis, Freedom Press,
- S. Brien, P. Prescott, N. Bashir, H. Lewith, G. Lewith (2008) Systematic review of the nutritional supplements dimethyl sulfoxide (DMSO) and methylsulfonylmethane (MSM) in the treatment of osteoarthritis Osteoarthr. Cartilage, 16 , p. 1277-1288
- L.S. Kim, L.J. Axelrod, P. Howar, N. Buratovich, R.F. Waters (2006) Efficacy of methylsulfonylmethane (MSM) in osteoarthritis pain of the knee: a pilot clinical trial Osteoarthr. Cartilage, 14 , p. 286-294
- « Methylsulfonylmethane (MSM) », sur quackwatch.org (consulté le ).
- « Méthyl sulfonyle méthane (MSM) », sur eurekasante.vidal.fr (consulté le ).
Voir aussi
[modifier | modifier le code]Bibliographie
[modifier | modifier le code]- Usha, P, R. & Naidum M, U. (2004). Randomised, Double-Blind, Parallel, Placebo-Controlled Study of Oral Glucosamine, Methylsulfonylmethane and their Combination in Osteoarthritis. Clinical Drug Investigation, 24(6):353-63
- Lim, E. J., Hong, D. Y., Park, J. H., Joung, Y. H., Darvin, P., Kim, S. Y. et al. (2012). Methylsulfonylmethane suppresses breast cancer growth by down-regulating STAT3 and STAT5b pathways. PloS one, 7(4):e33361, doi: 10.1371/journal.pone.0033361
- v. d. Merwe, M. & Bloomer, R. J. (2016, October). The Influence of Methylsulfonylmethane on Inflammation-Associated Cytokine Release before and following Strenuous Exercise. Journal of Sports Medicine, 2016: 7498359, doi: 10.1155/2016/7498359
- Sp, N., Kang, D. Y., Kim, D. H., Lee, H. G., Park, Y. M., Kim, I. H., ... & Yang, Y. M. (2020). [vhttps://www.spandidos-publications.com/10.3892/etm.2019.8196/download Methylsulfonylmethane inhibits cortisol‑induced stress through p53‑mediated SDHA/HPRT1 expression in racehorse skeletal muscle cells: A primary step against exercise stress]. Experimental and Therapeutic Medicine, 19(1), 214-222.
Lien externe
[modifier | modifier le code]- Fiche Sigma-Aldrich du composé Dimethyl sulfone, 98%, consultée le 13 décembre 2013.

