Acid cinamic
| Acid cinamic | |
 | |
 | |
| Nume IUPAC | acid (E)-3-fenil-2-propenoic |
|---|---|
| Alte denumiri | Acid benzenpropenoic |
| Identificare | |
| Număr CAS | 140-10-3 |
| ChEMBL | CHEMBL27246 |
| PubChem CID | 444539 |
| Informații generale | |
| Formulă chimică | C9H8O2 |
| Aspect | cristale albe monoclinice |
| Masă molară | 148,16 g/mol |
| Proprietăți | |
| Densitate | 1,2475 g/cm3 |
| Punct de topire | 133 °C |
| Punct de fierbere | 300 °C |
| Solubilitate în apă | |
| 500 mg/L | |
| Pericol | |
| Fraze R | R36 |
| Fraze S | S25 |
| NFPA 704 | |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Acidul cinamic este un compus organic din clasa acizilor monocarboxilici nesaturați, având formula structurală C6H5-CH=CH-COOH. Este un compus alb, cristalin, greu solubil în apă, dar solubil în majoritatea solvenților organici. [1] Este răspândit în natură în diverse plante. Fiind nesaturat, are o legătură dublă, ceea ce implică existența izomerilor cis și trans, dar cel din urmă este mai puțin comun. [2]
Răspândire
[modificare | modificare sursă]Acidul cinamic se obține, ca sursă naturală, din uleiul de scorțișoară, [3] și mai este întâlnit și în untul de shea. Compusul are un miros asemănător mierii, [4] iar acesta împreună cu esterul său etilic (cinamatul de etil, care este mult mai volatil) reprezintă componentele ce dau aromă din uleiul esențial de scorțișoară, în care aldehida sa, aldehida cinamică este componentul principal.
Obținere
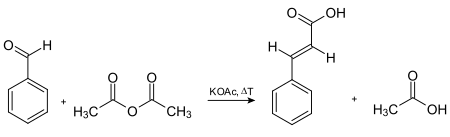
[modificare | modificare sursă]Sinteza originală a acidului cinamic are la bază o reacție Perkin, care implică condensarea în prezența unui catalizator bazic a anhidridei acetice cu benzaldehida. Rainer Ludwig Claisen (1851–1930) a descris sinteza esterilor acidului cinamic (numiți cinamați) prin reacția benzaldehidei cu esterii. Reacția este cunoscută sub numele de condensare aldolică. De asemenea, acidul poate fi preparat și prin reacția dintre aldehida cinamică (cinamaldehidă) și clorura de benziliden. [2]
Referințe
[modificare | modificare sursă]- ^ „Open Notebook Science Challenge: Solubilities of Organic Compounds in Organic Solvents”. Nature Precedings. . doi:10.1038/npre.2010.4243.3.[nefuncțională]
- ^ a b Dorothea Garbe "Cinnamic Acid" in Ullmann's Encyclopedia of Industrial Chemistry, 2000, Wiley-VCH, Weinheim. doi:10.1002/14356007.a07_099
- ^ Budavari, Susan, ed. (), The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (ed. a 12-a), Merck, ISBN 0911910123
- ^ Cinnamic acid, flavornet.org