氮族元素的氫化物
外觀
氮族元素的氫化物,又稱磷屬化氫[1](英語:hydrogen pnictides)是由氫原子與氮族元素原子(氮、磷、砷、銻、鉍或鏌)構成的化合物,是一種氫二元化合物。
氮族元素的三氫化物
[編輯]最簡單的氮族元素氫化物由三個氫原子與一個氮族元素原子化合而成,其化學式通常計為XH3,少數情況下會計做H3X,其中X表示任何一種氮族元素。這些分子的結構都是三角錐形分子構型(有別於硼族元素的三氫化物的平面三角形分子構型)且皆具有極性。
這些三氫化物最穩定的是氨,而位於週期表越下方的越不穩定,且具有毒性。
| 化合物 | 化學式 | 鍵長 | 空間填充模型 |
|---|---|---|---|
氨 胺 |
 [2] [2] |
 | |
膦 |
 |
 | |
胂 |
 |
 | |
䏲 |
 |
 | |
䏟 |
 |
 | |
氮族元素的三氫化物的性質如下[4]:
| 性質 | 氮化氫(氨) | 磷化氫(膦) | 砷化氫(胂) | 銻化氫(䏲) | 鉍化氫(䏟) |
|---|---|---|---|---|---|
| 化學式 | NH3 | PH3 | AsH3 | SbH3 | BiH3 |
| 熔點 (°C) | −77.8 | −133.5 | −116.3 | −88 | ? |
| 沸點 (°C) | −34.5 | −87.5 | −62.4 | −18.4 | 16.8 (推測) |
| 液體密度 (g/cm3) | 0.683 (−34 °C) | 0.746 (−90 °C) | 1.640 (−64 °C) | 2.204 (−18 °C) | ? |
| ΔH° f/kJ mol−1 |
−46.1 | +5[5] | +66.4 | +145.1 | +277.8 |
| 鍵長 (X–H)/pm | 101.7 | 141.9 | 151.9 | 170.7 | 177.59 |
| 鍵角 H–X–H | 107.8° | 93.6° | 91.8° | 91.3° | 90.48°[6] |
氮族元素四氫化物離子
[編輯]氮族元素三氫化物還可以再被質子化成化學式形如XH4+的鎓離子,且為四面體形分子:
| 離子 | 化學式 | 分子構型 | pka | 分子結構圖 | 球-棍模型 | 有機衍生物 |
|---|---|---|---|---|---|---|
銨 |
四面體型 | 9.25[7] |  |
 |
季銨鹽 | |
鏻 |
四面體型 |  |
 |
季鏻鹽 | ||
鉮 |
四面體型[8] |  |
 |
|||
四氫銻陽離子 |
四面體型[8] |
-2價氮族元素的氫化物
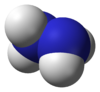
[編輯]另一種常見的氮族元素氫化物為2個氮族元素原子和四個氫原子化合而成,常見的比如由氮構成的聯氨,或稱肼。
| 化合物 | 化學式 | 分子結構圖 | 空間填充模型 | 質子化物種 |
|---|---|---|---|---|
肼 聯氨 (聯胺) |
 |
 |
N2H+ 5 N2H2+ 6 | |
聯膦 |
 |
 |
||
聯胂 |
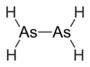 |
 |
參見
[編輯]參考文獻
[編輯]- ^ 磷屬化物 pnictide. 國家教育研究院. [2017-07-21]. (原始內容存檔於2017-08-10).
- ^ ammonia. pubchem. [2017-07-21]. (原始內容存檔於2017-06-20).
- ^ Fricke, Burkhard. Superheavy elements: a prediction of their chemical and physical properties. Recent Impact of Physics on Inorganic Chemistry. 1975, 21: 89–144 [2013-10-04]. doi:10.1007/BFb0116498. (原始內容存檔於2015-04-18).
- ^ 4.0 4.1 Greenwood, Norman Neill; Earnshaw, Alan. Chemistry of the elements. 2016. ISBN 978-0-7506-3365-9. OCLC 1040112384 (英語)., pp. 557–8
- ^ Zumdahl, Steven S. Chemical Principles 6th. Houghton Mifflin. 2009: A22. ISBN 978-0-618-94690-7.
- ^ W. Jerzembeck, H. Bürger, L. Constantin, L. Margulès, J. Demaison, J. Breidung, W. Thiel. Bismuthine BiH3: Fact or Fiction? High-Resolution Infrared, Millimeter-Wave, and Ab Initio Studies. Angew. Chem. Int. Ed. 2002, 41 (14): 2550–2552 [2017-08-10]. (原始內容存檔於2013-01-05).
- ^ Garrett, R.H. and Grisham, C.M. Biochemistry. Cengage Learning. 2016: 43 [2017-08-10]. ISBN 9781305886896. (原始內容存檔於2017-08-10).
- ^ 8.0 8.1 R. Minkwitz, R.; Kornath, A.; Sawodny, W.; Härtner, H. Über die Darstellung der Pnikogenoniumsalze AsH4+SbF6−, AsH4+AsF6−, SbH4+SbF6−. Zeitschrift für anorganische und allgemeine Chemie. 1994, 620 (4): 753–756. doi:10.1002/zaac.19946200429.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||



