Torium
90Th Torium | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Sampel torium di dalam ampul yang berisi gas argon | |||||||||||||||||||||||||||||||||||||||||
Garis spektrum torium | |||||||||||||||||||||||||||||||||||||||||
| Sifat umum | |||||||||||||||||||||||||||||||||||||||||
| Pengucapan | /torium/[1] | ||||||||||||||||||||||||||||||||||||||||
| Penampilan | keperakan, seringkali dengan noda hitam | ||||||||||||||||||||||||||||||||||||||||
| Torium dalam tabel periodik | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
| Nomor atom (Z) | 90 | ||||||||||||||||||||||||||||||||||||||||
| Golongan | golongan n/a | ||||||||||||||||||||||||||||||||||||||||
| Periode | periode 7 | ||||||||||||||||||||||||||||||||||||||||
| Blok | blok-f | ||||||||||||||||||||||||||||||||||||||||
| Kategori unsur | aktinida | ||||||||||||||||||||||||||||||||||||||||
| Berat atom standar (Ar) |
| ||||||||||||||||||||||||||||||||||||||||
| Konfigurasi elektron | [Rn] 6d2 7s2 | ||||||||||||||||||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 18, 32, 18, 10, 2 | ||||||||||||||||||||||||||||||||||||||||
| Sifat fisik | |||||||||||||||||||||||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | padat | ||||||||||||||||||||||||||||||||||||||||
| Titik lebur | 2115 K (1842 °C, 3348 °F) | ||||||||||||||||||||||||||||||||||||||||
| Titik didih | 5061 K (4788 °C, 8650 °F) | ||||||||||||||||||||||||||||||||||||||||
| Kepadatan mendekati s.k. | 11,7 g/cm3 | ||||||||||||||||||||||||||||||||||||||||
| Kalor peleburan | 13,81 kJ/mol | ||||||||||||||||||||||||||||||||||||||||
| Kalor penguapan | 514 kJ/mol | ||||||||||||||||||||||||||||||||||||||||
| Kapasitas kalor molar | 26,230 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||
Tekanan uap
| |||||||||||||||||||||||||||||||||||||||||
| Sifat atom | |||||||||||||||||||||||||||||||||||||||||
| Bilangan oksidasi | +1, +2, +3, +4 (oksida basa lemah) | ||||||||||||||||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 1,3 | ||||||||||||||||||||||||||||||||||||||||
| Energi ionisasi | ke-1: 587 kJ/mol ke-2: 1110 kJ/mol ke-3: 1930 kJ/mol | ||||||||||||||||||||||||||||||||||||||||
| Jari-jari atom | empiris: 179,8 pm | ||||||||||||||||||||||||||||||||||||||||
| Jari-jari kovalen | 206±6 pm | ||||||||||||||||||||||||||||||||||||||||
| Lain-lain | |||||||||||||||||||||||||||||||||||||||||
| Kelimpahan alami | primordial | ||||||||||||||||||||||||||||||||||||||||
| Struktur kristal | kubus berpusat muka (fcc) | ||||||||||||||||||||||||||||||||||||||||
| Kecepatan suara batang ringan | 2490 m/s (suhu 20 °C) | ||||||||||||||||||||||||||||||||||||||||
| Ekspansi kalor | 11,0 µm/(m·K) (suhu 25 °C) | ||||||||||||||||||||||||||||||||||||||||
| Konduktivitas termal | 54,0 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||
| Resistivitas listrik | 157 nΩ·m (suhu 0 °C) | ||||||||||||||||||||||||||||||||||||||||
| Arah magnet | paramagnetik[3] | ||||||||||||||||||||||||||||||||||||||||
| Suseptibilitas magnetik molar | 132,0×10−6 cm3/mol (293 K)[4] | ||||||||||||||||||||||||||||||||||||||||
| Modulus Young | 79 GPa | ||||||||||||||||||||||||||||||||||||||||
| Modulus Shear | 31 GPa | ||||||||||||||||||||||||||||||||||||||||
| Modulus curah | 54 GPa | ||||||||||||||||||||||||||||||||||||||||
| Rasio Poisson | 0,27 | ||||||||||||||||||||||||||||||||||||||||
| Skala Mohs | 3,0 | ||||||||||||||||||||||||||||||||||||||||
| Skala Vickers | 295–685 MPa | ||||||||||||||||||||||||||||||||||||||||
| Skala Brinell | 390–1500 MPa | ||||||||||||||||||||||||||||||||||||||||
| Nomor CAS | 7440-29-1 | ||||||||||||||||||||||||||||||||||||||||
| Sejarah | |||||||||||||||||||||||||||||||||||||||||
| Penamaan | dari Thor, dewa guntur Norse | ||||||||||||||||||||||||||||||||||||||||
| Penemuan | Jöns J. Berzelius (1829) | ||||||||||||||||||||||||||||||||||||||||
| Isotop torium yang utama | |||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||
Torium adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Th dan nomor atom 90. Logam torium berwarna keperakan dan bernoda hitam saat terkena udara, membentuk torium dioksida; logam ini cukup keras, mudah dibentuk, dan memiliki titik lebur yang tinggi. Torium adalah aktinida elektropositif yang sifat kimianya didominasi oleh keadaan oksidasi +4; unsur ini cukup reaktif dan bisa menyala di udara saat terbagi halus.
Semua isotop torium yang diketahui tidak stabil. Isotop yang paling stabil, 232Th, memiliki waktu paruh 14,05 miliar tahun, atau sekitar umur alam semesta; isotop ini meluruh sangat lambat melalui proses peluruhan alfa dan memulai rantai peluruhan yang dinamai "deret torium" yang berakhir pada 208Pb yang stabil. Di Bumi, torium, bismut dan uranium adalah tiga unsur radioaktif yang masih ada secara alami dalam jumlah banyak sebagai unsur primordial.[a] Diperkirakan torium tiga kali lebih berlimpah daripada uranium di kerak bumi. Logam torium terutama dimurnikan dari pasir monasit sebagai produk sampingan dari ekstraksi logam tanah jarang,
Torium ditemukan pada tahun 1828 oleh ahli mineral amatir Norwegia Morten Thrane Esmark dan diidentifikasi oleh ahli kimia Swedia Jöns Jacob Berzelius, yang menamainya dari Thor, dewa petir Nordik. Kegunaan pertamanya dikembangkan pada akhir abad ke-19. Radioaktivitas torium diketahui secara luas semasa awal dekade abad ke-20. Pada paruh kedua abad ini, torium telah digantikan penggunaannya dalam berbagai situasi karena muncul kekhawatiran mengenai sifat radioaktifnya.
Torium masih digunakan sebagai unsur paduan dalam elektrode pengelasan TIG, namun secara perlahan digantikan dengan bahan lainnya. Ia juga digunakan sebagai bahan dalam instrumen optik dan ilmiah canggih, dan sebagai sumber cahaya pada perangkat lampu gas, tapi penggunaannya sudah semakin jarang. Torium telah diusulkan digunakan sebagai pengganti uranium untuk bahan bakar reaktor nuklir dan beberapa reaktor torium telah dibangun.
Sifat umum
[sunting | sunting sumber]Torium merupakan logam aktinida radioaktif berwana keperakan terang, paramagnetik, dan agak lunak. Di dalam tabel periodik, torium berada di sebelah kanan aktinium, kiri protaktinium, dan di bawah serium. Torium murni sangat lunak, dan seperti logam pada umumnya, dapat dirolkan dalam keadaan dingin, ditempa, dan dibentuk.[5] Pada temperatur ruangan, logam torium memiliki struktur kristal kubus berpusat muka. Ia juga memiliki dua bentuk lain, satu pada temperatur tinggi (lebih dari 1360 °C), yaitu kubus berpusat badan dan satu lagi pada tekanan tinggi (sekitar 100 GPa), yaitu tetragonal berpusat badan.[5]
Logam torium memiliki modulus kompresi (ukuran ketahanan terhadap kompresi dari bahan) sebesar 54 GPa, hampir sama seperti timah (58,2 GPa). Sebagai perbandingan, modulus kompresi aluminium sebesar 75,2 GPa; tembaga 137,8 GPa; dan baja ringan sebesar 160-169 GPa.[6] Kekerasan torium adalah sama kerasnya dengan baja lunak, sehingga ketika dipanaskan torium dapat dirolkan menjadi lembaran dan ditarik menjadi kawat.[7]
Kepadatan torium mendekati setengah dari kepadatan uranium dan plutonium. Namun ia lebih keras dari kedua logam tersebut.[7] Torium menjadi superkonduktif di bawah suhu 1,4 K.[5] Titik lebur torium yang sebesar 1.750 °C berada di atas titik lebur aktinium (1.227 °C) dan protaktinium (1568 °C). Pada unsur-unsur permulaan periode 7, dari fransium sampai dengan torium, titik lebur unsur meningkat (seperti halnya unsur pada periode lain). Hal ini disebabkan jumlah elektron terdelokalisasi yang setiap atom kontribusikan meningkat dari satu elektron pada fransium menjadi empat elektron pada torium. Ini menyebabkan gaya tarik antara elektron-elektron dengan ion logam menjadi lebih besar seiring dengan muatan positif logam yang meningkat dari satu menjadi empat. Setelah torium, ada kecenderungan penurunan titik lebur yang berawal dari torium sampai dengan plutonium. Ini beriringan dengan meningkatnya jumlah elektron f dari sekitar 0,4 pada torium menjadi sekitar 6 pada polonium; kecenderungan ini disebabkan oleh peningkatan hibridisasi orbital 5f dan 6d pada atom dan pembentukan ikatan berarah yang mengakibatkan struktur kristal logam menjadi lebih kompleks dan melemahkan ikatan antar logam.[7][8] (Perhitungan elektron f untuk torium tidaklah bulat karena adanya tumpang tindih orbital 5f–6d).[8] Di antara unsur aktinida-aktinida hingga kalifornium, yang dapat dipelajari setidaknya dalam jumlah miligram, torium memiliki titik lebur dan titik didih yang tertinggi dan kepadatan yang terendah kedua; hanya unsur aktinium yang lebih lebih ringan daripada torium.[b] Titik didih torium adalah 4788 °C, merupakan titik didih yang tertinggi kelima di antara semua unsur yang telah diketahui titik didihnya.[c]
Sifat-sifat torium sangat bervariasi tergantung pada tingkat ketidakmurnian dalam sampel logam. Pengotor utama biasanya torium dioksida (ThO2); bahkan spesimen torium yang paling murni biasanya masih mengandung dioksida tersebut dalam takaran sekitar sepersepuluh persen (0,1 %).[5] Pengukuran-pengukuran eksperimental yang dilakukan untuk menentukan berat jenis torium memberikan nilai sebesar antara 11,5 sampai dengan 11,66 g/cm3: nilai tersebut sedikit lebih rendah dari nilai teoretis yang diharapkan, yaitu 11,7 g/cm3 (dihitung dari parameter kisi torium). Perbedaan ini mungkin disebabkan rongga-rongga mikroskopis yang terbentuk dalam logam ketika dicetak.[5] Nilai-nilai ini berada di antara nilai berat jenis unsur aktinium (10,1 g/cm3) dan protaktinium (15.4 g/cm3) yang bersebelahan dengan torium.[5]
Torium dapat dibentuk menjadi aloi dengan logam lainnya. Penambahan sebagian kecil torium pada magnesium akan meningkatkan kekuatan mekanik logam tersebut. Selain itu pemaduan torium-aluminium telah dipertimbangkan sebagai cara untuk menyimpan torium dalam reaktor nuklir torium usulan di masa depan. Torium membentuk campuran eutektik dengan kromium dan uranium. Selain itu, torium tercampur sepenuhnya dalam wujud padat maupun cair dengan unsur saudaranya yang lebih ringan, serium.[5]
Isotop
[sunting | sunting sumber]
Kecuali dua unsur, teknesium (unsur 43) dan prometium (unsur 61), semua unsur hingga bismut (unsur 83) memiliki satu isotop yang praktis stabil. Sedangkan polonium (unsur 84) dan semua unsur seterusnya bersifat radioaktif. 232Th merupakan salah satu dari tiga nuklida selain bismut (dua lainnya adalah 235U dan 238U) yang memiliki waktu paruh dalam ukuran milyaran tahun; waktu paruhnya 14,05 miliar tahun, sekitar tiga kali umur bumi dan sedikit lebih tua dari umur alam semesta. Sekitar delapan puluh persen torium yang ada pada saat pembentukan bumi masih bertahan hingga sekarang.[11][12][13] 232Th merupakan satu-satunya isotop torium yang ada dalam jumlah memadai di alam.[11] Stabilitasnya disebabkan oleh kulit inti tertutupnya yang ber-142 neutron.[14][15] Torium memiliki karakteristik komposisi isotop bumi, dengan berat atom sebesar 232,0377(4). Torium merupakan salah satu dari empat unsur radioaktif (bersama dengan bismut, protaktinium, dan uranium) yang kelimpahannya cukup besar di bumi untuk ditentukan berat atom standarnya.[16]
Inti torium rentan terhadap peluruhan alfa karena gaya nuklir kuatnya tidak dapat mengatasi tolakan elektromagnetik antar proton-protonnya.[17] Peluruhan alfa 232Th memulai rantai peluruhan 4n yang melibatkan isotop bernomor massa kelipatan 4 (disebut juga deret torium sesuai dengan nama unsur induknya). Rangkaian peluruhan alfa dan beta berturut-turut ini dimulai dari peluruhan 232Th menjadi 228Ra dan berakhir pada 208Pb.[11] Semua sampel logam torium maupun senyawa-senyawanya akan mengandung sekelumit anak-anak peluruhan ini, yaitu isotop-isotop talium, timbal, bismut, polonium, radon, radium, dan aktinium. Sampel torium alami dapat dimurnikan secara kimiawi untuk mengekstraksi berbagai nuklida anak yang berguna, seperti 212Pb, yang digunakan dalam kedokteran nuklir untuk terapi kanker.[18][19] 227Th (pemancar partikel alfa berwaktu paruh 18,68 hari) juga dapat digunakan dalam terapi kanker seperti terapi partikel alfa bertarget.[20][21][22] 232Th kadang-kadang juga mengalami fisi spontan daripada peluruhan alfa. Bukti-bukti peristiwa ini tertinggal dalam mineral-mineral torium (sebagai gas xenon yang terjebak dan terbentuk dari hasil fisi tersebut). Namun waktu paruh parsial dari proses ini sangat besar di atas 1021 tahun dan sebaliknya peluruhan alfa lah yang mendominasi.[23][24]
Terdapat tiga puluh radioisotop torium yang telah dikarakterisasi, dari yang bernomor massa 209[25] hingga 238.[23] Setelah 232Th, yang paling stabil (berdasarkan waktu paruhnya) adalah 230Th dengan waktu paruh 75.380 tahun, 229Th dengan waktu paruh 7.340 tahun, 228Th dengan waktu paruh 1,92 tahun, 234Th dengan waktu paruh 24,10 hari, dan 227Th dengan waktu paruh 18,68 hari. Semua isotop-isotop ini terdapat di alam sebagai radioisotop kelumit karena keberadaan mereka dalam rantai peluruhan 232Th, 235U, 238U, dan 237Np: yang terakhir ini telah lama punah di alam karena waktu paruhnya yang pendek (2,14 juta tahun), tetapi terus diproduksi dalam jumlah sekelumit akibat proses tangkapan neutron dalam bijih uranium. Isotop-isotop torium yang lain memiliki waktu paruh kurang dari 30 hari dan sebagian besarnya kurang dari 10 menit.[11]
Di laut dalam, isotop 230Th menduduki hingga 0,04% dari torium alami.[16] Ini disebabkan oleh induk 238U yang larut dalam air tetapi 230Th tak larut dan mengendap ke dalam sedimen. Bijih uranium dengan konsentrasi torium yang rendah dapat dimurnikan untuk menghasilkan sampel torium berukuran gram yang lebih dari seperempatnya berisotop 230Th, karena 230Th merupakan salah satu anak peluruhan dari 238U.[23] Persatuan Kimia Murni dan Terapan Internasional (IUPAC) menggolongkan kembali torium sebagai unsur binuklida pada tahun 2013; sebelumnya torium dianggap sebagai unsur mononuklida.[16]
Torium memiliki 3 isomer nuklir (atau keadaan metastabil), yaitu 216m1Th, 216m2Th, dan 229mTh.229mTh memiliki energi eksitasi terendah dari semua isomer tersebut,[26] yang terukur bernilai 7,6 ± 0,5 eV. Energi ini sebegitu rendahnya sehingga ketika menjalani transisi isomer, radiasi gama yang dipancarkan berada dalam kisaran ultraviolet.[27][28][d] Isotop-isotop torium yang berbeda memiliki sifat kimia yang sama tetapi sifat fisikanya yang sedikit berbeda: sebagai contoh, kepadatan dari 228Th, 229Th, 230Th, dan 232Th murni berturut-turut adalah 11,5, 11,6, 11,6, dan 11,7 g/cm3.[30] Isotop 229Th diprediksi dapat menjalani fisi dengan masa kritis polosnya 2839 kg, walaupun dengan reflektor baja nilai ini turun menjadi 994 kg.[30][e] 232Th tidak dapat berfisi, tetapi merupakan nuklida fertil karena dapat diubah menjadi bahan fisil 233U melalui tangkapan neutron yang diikuti peluruhan beta.[30][31]
Penanggalan radiometrik
[sunting | sunting sumber]Terdapat dua metode penanggalan radiometrik yang melibatkan isotop torium, yaitu penanggalan uranium–torium yang didasarkan pada peluruhan 234U menjadi 230Th, dan penanggalan ionium–torium yang mengukur rasio 232Th terhadap 230Th.[f] Kedua metode ini didasarkan pada fakta bahwa 232Th adalah radioisotop purba dan 230Th hanya muncul sebagai produk antara dalam rantai peluruhan 238U.[32] Penanggalan uranium–torium merupakan proses yang relatif berjangka pendek karena waktu paruh 234U dan 230Th yang relatif pendek terhadap usia Bumi. Proses ini juga dibarengi dengan proses yang melibatkan peluruhan alfa 235U menjadi 231Th, yang kemudian dengan cepat menjadi 231Pa yang berwaktu paruh panjang. Proses berbarengan ini sering digunakan untuk mengecek hasil penanggalan uranium–torium. Penanggalan uranium–torium umumnya digunakan untuk menentukan usia material kalsium karbonat seperti speleotem dan batu karang karena uranium lebih larut daripada torium dan protaktinium, sehingga kedua unsur ini secara selektif mengendap ke dalam sedimen laut. Dari sedimen inilah rasio kedua unsur tersebut diukur. Penanggalan ini memiliki kisaran waktu beberapa ratus tahunan.[32][33] Penanggalan ionium–torium merupakan proses yang mirip, yaitu dengan mengukur rasio 232Th terhadap 230Th di sedimen laut.[34][35] Kedua metode penanggalan ini memiliki asumsi dasar bahwa proporsi 230Th terhadap 232Th adalah konstan selama periode sewaktu lapisan sedimen tersebut terbentuk, bahwa sedimen tersebut belumlah mengandung torium sebelum uranium meluruh, dan bahwa torium tidak dapat bermigrasi dalam lapisan sedimen tersebut.[34][35]
Sifat kimia
[sunting | sunting sumber]Sebuah atom torium memiliki 90 elektron; 4 dari elektron tersebut merupakan elektron valensi. Terdapat tiga orbital atom yang secara teoretis tersedia bagi elektron valensi untuk diduduki, yakni orbital 5f, 6d, dan 7s.[36] Walaupun torium terletak pada blok-f tabel periodik, ia memiliki konfigurasi elektron dalam keadaan dasar yang tak lazim, yakni [Rn]6d27s2. Pada unsur aktinida awal, energi subkelopak 5f dan 6d unsur sangatlah dekat; pada torium subkelopak 6d-nya berenergi lebih rendah daripada subkelopak 5f-nya. Hal ini karena subkelopak 5f-nya terdestabilisasi dan tidak terperisai dengan baik oleh subkelopak 6s dan 6p yang terisi. Hal ini disebabkan oleh efek-efek relativitas yang semakin kuat pada unsur bagian bawah dalam tabel periodik, terutama efek interaksi spin–orbit. Kedekatan energi 5f, 6d, dan 7s pada torium menyebabkannya hampir selalu melepaskan keempat elektron valensinya dan sehingganya berwujud dalam keadaan oksidasi +4. Hal ini berbeda dengan serium, saudara lantanida torium, yang walaupun dapat berwujud dalam keadaan oksidasi +4, keadaan oksidasi +3-nya lah yang memainkan peran penting dan lebih stabil. Sifat-sifat kimiawi torium lebih mirip dengan logam-logam transisi seperti zirkonium dan hafnium daripada dengan serium dalam hal energi ionisasi dan potensial redoksnya. Perilaku bak-logam transisi ini merupakan kecenderungan yang normal pada separuh awal deret unsur aktinida.[37][38]

Walaupun konfigurasi elektron atom torium dalam wujud gas tidak lazim, torium dalam wujud logam menunjukkan keterlibatan orbital 5f yang signifikan. Sebuah keadaan metalik torium teoretis yang berkonfigurasi [Rn]6d27s2 dengan orbital 5f-nya di atas aras Fermi haruslah tersusun rapat heksagonal seperti pada unsur golongan 4 titanium, zirkonium dan hafnium. Namun, struktur torium yang terpantau sebenarnya adalah struktur kubus berpusat muka . Struktur kristal yang terpantau ini dapat dijelaskan apabila keadaan orbital 5f torium dilibatkan.[8]
Senyawa tetravalen torium biasanya tidak berwarna ataupun berwarna kuning. Ini karena ion Th4+ tidak memiliki elektron 5f atau 6d.[7] Sifat-sifat kimiawi torium oleh sebab itu didominasi oleh keelektropositifannya yang berbentuk ion diamagnetik berkonfigurasi gas mulia.[39][g] Torium dan uranium merupakan unsur radioaktif yang paling banyak dipelajari karena radioaktivitasnya cukup rendah sehingga tidak diperlukan penanganan yang khusus dalam laboratorium.[40]
Reaktivitas
[sunting | sunting sumber]Torium merupakan logam yang bereaktivitas tinggi dan elektropositif. Potensial reduksi standar torium adalah −1.90 V untuk pasangan Th4+/Th, Torium sedikit lebih elektropositif daripada zirkonium ataupun aluminium.[41] Logam torium yang terbagi halus bersifat piroforik dan dapat menyala spontan di udara bebas.[5] Ketika dipanaskan di udara bebas, remah torium menyala dan terbakar memancarkan cahaya putih yang terang, membentuk senyawa torium dioksida. Dalam bentuk bongkahan, torium murni bereaksi dengan lambat di udara bebas, walaupun korosi dapat terjadi setelah beberapa bulan. Kebanyakan sampel torium terkontaminasi sesedikit oleh torium dioksida. Kontaminasi ini mempercepat proses korosi.[5] Sampel torium seperti ini akan mengusam dengan perlahan; permukaannya menjadi abu-abu dan akhirnya menghitam.[5]
Pada suhu dan tekanan standar, torium dengan lambat diserang oleh air, tetapi akan dengan segera larut dalam kebanyakan asam, terkecuali dalam larutan asam klorida, yang meninggalkan residu tak larut ThO(OH,Cl)H.[5][42] Torium larut dalam asam nitrat pekat yang mengandung sejumlah kecil ion katalitik fluorida atau fluorosilikat;[5][43] apabila tidak terdapat kedua ion ini, proses pasivasi oleh nitrat akan terjadi, sebagaimana yang terjadi pada uranium dan plutonium.[5][44][45]
Senyawa anorganik
[sunting | sunting sumber]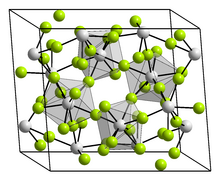
Kebanyakan senyawa biner torium dengan unsur nonlogam dapat dibuat melalui pemanasan kedua unsur tersebut.[46] Di udara bebas, torium terbakar menjadi ThO2 yang berstruktur fluorit.[47] Torium dioksida ini merupakan bahan refraktori yang bertitik lebur tertinggi (3390 °C) di antara semua senyawa oksida yang diketahui.[48] Torium dioksida sedikit bersifat higroskopik dan bereaksi dengan air dan berbagai gas;[49] ia larut dalam asam nitrat pekat apabila terdapat ion fluorida dalam larutan tersebut.[50]
Ketika dipanaskan di udara bebas, torium dioksida memancarkan cahaya biru yang terang. Cahaya ini berubah menjadi putih ketika torium dioksida dicampur dengan serium dioksida (CeO2). Kedua campuran senyawa ini dahulunya umumnya digunakan dalam kaus lampu untuk menghasilkan cahaya putih yang terang.[49] Kobaran api tidaklah diperlukan untuk mendapatkan cahaya terang ini. Pada tahun 1910, ditemukan bahwa kaus lampu Welsbach (terbuat dari ThO2 dengan 1% CeO2) yang panas tetap berpancar penuh ketika terpapar dengan campuran gas bakar dan udara.[51] Cahaya yang dipancarkan torium dioksida memiliki panjang gelombang yang lebih tinggi daripada yang diharapkan dari emisi benda hitam sebuah pijaran yang bertemperatur sama; efek ini disebut sebagai kandoluminesens. Ini terjadi karena ThO2 : Ce berperan sebagai katalis bagi rekombinasi radikal bebas yang muncul pada kobaran api bertemperatur tinggi. Deeksitasi radikal bebas ini menghasilkan energi yang besar. Penambahan 1% serium dioksida pada kaus lampu meningkatkan efek tersebut dengan meningkatkan emisivitas bahan pada daerah spektrum cahaya tampak; serium, tidak seperti torium, dapat berwujud dalam berbagai keadaan oksidasi yang bermacam-macam. Oleh karenanya, muatan beserta emisivitas cahaya tampak serium bergantung pada daerah di mana ia ditemukan dalam kobaran api.[51]
Beberapa senyawa torium kalkogenida dan oksikalkogenida yang diketahui meliputi persenyawaan dengan sulfur, selenium, and telurium.[52] Torium dapat bersenyawa dengan seluruh unsur golongan halogen sebagai torium tetrahalida.[53] Semua senyawa torium tetrahalida berkoordinasi 8 dan merupakan senyawa higroskopik yang larut dengan mudah dalam pelarut polar seperti air.[54] Senyawa torium tetrafluorida memiliki struktur kristal monoklinik seperti yang ditemukan pada zirkonium tetrafluorida dan hafnium tetrafluorida. Senyawa ini memilki geometri antiprisma persegi yang terdistorsi.[53] Sebaliknya, senyawa torium tetrahalida lainnya (klorida, bromida, dan iodida) memiliki geometri dodekahedral.[54] Selain itu, torium ditemukan juga dapat bersenyawa dalam valensi rendah dengan bromida (ThBr2 dan ThBr3) dan iodida (ThI2 dan ThI3).[53] Senyawa ThI3 (yang berwarna hitam) dan ThI2 (yang berwarna emas) dapat dibuat dari reduksi torium tetraiodida dengan logam torium. Senyawa torium iodida bervalensi rendah ini tidak mengandung Th3+ ataupun Th2+, melainkan mengandung Th4+ yang beranion elektron (Th4+ (I-)3 e- pada ThI3). Ini disebut sebagai senyawa elektrida.[53] Berbagai ion torium polihalida juga telah diketahui.[53] Sebagai contohnya, ketika kalium fluorida dan asam fluorida direaksikan dengan Th4+, kompleks anion ThF2−6 akan terbentuk dan mengendap menjadi garam K2ThF6 yang tak larut.[43]
Torium borida, karbida, silisida, dan nitrida adalah bahan-bahan refraktori. Oleh sebab itu, senyawa-senyawa ini mendapat perhatian khusus sebagai bahan bakar nuklir.[46] Keempat unsur pniktogen seperti fosforus, arsenik, antimon dan bismut juga bersenyawa dengan torium menjadi senyawa biner. Torium germanida juga telah diketahui keberadaannya.[55] Torium bereaksi dengan hidrogen, membentuk torium hidrida ThH2 dan Th4H15, Senyawa terakhir ini bersifat superkonduktif pada temperatur di bawah 7,5–8 K; pada temperatur dan tekanan standar, ia menghantarkan listrik seperti logam pada umumnya.[56] Senyawa torium hidrida secara termal tidak stabil dan terurai cepat seketika terpapar dengan udara bebas dan kelembaban.[57]
Senyawa koordinasi
[sunting | sunting sumber]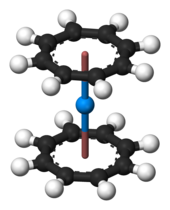
Dalam larutan air yang asam, ion torium berwujud sebagai ion akua tetrapositif [Th(H2O)9]4+ yang bergeometri prisma trigonal bertudung-tiga.[58][59] Pada pH < 3 larutan garam torium didominasi oleh kation tersebut.[58] Ion Th4+ merupakan ion unsur aktinida tetrapositif yang terbesar. Bergantung pada bilangan koordinasinya, ion ini berjari-jari antara 0,95 sampai dengan 1,14 Å.[58] Ion ini bersifat cukup asam karena muatannya yang tinggi. Keasamannya sedikit lebih kuat daripada asam sulfit, sehingga ia cenderung mengalami hidrolisis dan polimerisasi menjadi [Th2(OH)2]6+ dalam larutan ber-pH 3 atau kurang. Dalam larutan yang lebih basa, proses polimerisasi berlanjut sampai dengan terbentuknya Th(OH)4 yang bergelatin dan kemudian mengendap.[60] Sebagai asam Lewis keras, Th4+ lebih memfavoritkan ligan keras yang beratom oksigen sebagai donor. Senyawa kompleks dengan ligan beratom sulfur sebagai donor kurang stabil dan sehingganya lebih rentan terhidrolisis.[37]
Bilangan koordinasi yang tinggi sangatlah lazim bagi senyawa koordinasi torium karena ukuran torium yang besar. Torium nitrat pentahidrat merupakan contoh senyawa berbilangan koordinasi 11 yang pertama kali diketahui. Torium oksalat tetrahidrat berbilangan koordinasi 10 sedangkan torium borohidrida (pertama kali dibuat pada Proyek Manhattan) berbilangan koordinasi 14.[60] Garam-garam torium ini dikenal baik atas kelarutannya yang tinggi dalam air dan pelarut organik polar.[7]
Terdapat pula banyak senyawa torium anorganik beranion poliatomik yang diketahui. Contohnya torium perklorat, sulfat, sulfit, nitrat, karbonat, fosfat, vanadat, molibdat, dan kromat, beserta dengan bentuk-bentuk hidrat mereka.[61] Senyawa-senyawa ini sangatlah penting dalam proses pemurnian torium dan pembuangan limbah nuklir. Sebagian besar dari senyawa ini belumlah dikarakterisasi dengan penuh, terutama mengenai sifat-sifat strukturnya.[61] Senyawa kompleks torium dengan ligan organik seperti oksalat, sitrat, dan EDTA cenderung lebih stabil. Dalam perairan yang mengandung torium alami, senyawa torium organik biasanya ditemukan dalam konsentrasi yang beberapa pangkat orde lebih besar daripada senyawa torium anorganik. Hal ini berlaku bahkan apabila konsentrasi ligan anorganik lebih besar daripada konsentrasi ligan organik.[58]
Senyawa organotorium
[sunting | sunting sumber]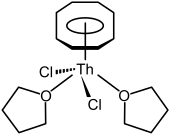
Kebanyakan hasil riset mengenai senyawa organotorium berfokus pada kompleks siklopentadienil dan siklooktatetraenil torium. Sama seperti dengan banyak unsur aktinida awal dan menengah (sampai dengan amerisium), torium dapat bersenyawa menjadi kompleks siklooktatetraenida Th(C8H8)2 (torosena) yang berwarna kuning. Kompleks ini isotipik dengan senyawa analog uranium, uranosena. yang lebih terkenal.[62] Torosena dapat dibuat dengan mereaksikan kalium siklooktatetraenida (K2C8H8) dengan torium tetraklorida dalam tetrahidrofuran (THF) pada temperatur es kering. Ia juga dapat dibuat dengan mereaksikan torium tetrafluorida dengan MgC8H8.[62] Torosena tidak stabil di udara bebas dan akan terurai dalam air atau pada suhu 190 °C.[62] Berbagai senyawa apit setengah torium juga telah diketahui, seperti misalnya (η8-C8H8)ThCl2(THF)2 yang berstruktur bangku piano. Senyawa ini dibuat dari reaksi antara torosena dengan torium tetraklorida dalam tetrahidrofuran.[37]
Senyawa siklopentadienil torium yang paling sederhana adalah Th(C5H5)3 dan Th(C5H5)4. Turunan-turunan dari senyawa ini juga banyak diketahui. Senyawa yang pertama (yang memiliki dua bentuk, bentuk berwarna ungu dan bentuk berwarna hijau) adalah contoh langka torium dalam keadaan oksidasi formal +3;[62][63] torium dalam keadaan oksidasi +2 juga berwujud pada turunan senyawa tersebut.[64] Turunan klorida [Th(C5H5)3Cl] dibuat dari pemanasan torium tetraklorida dengan K(C5H5) yang berjumlah terbatas. Turunan alkil dan aril senyawa torium siklopentadienil dapat dibuat dari turunan klorida tersebut dan telah digunakan untuk mempelajari ciri-ciri ikatan sigma Th–C.[63]
Senyawa organotorium yang lainnya kuranglah terkaji dengan baik. Senyawa tetrabenziltorium, Th(CH2C6H5) dan tetraaliltorium, Th(C3H5)4 telah diketahui keberadaannya, tetapi strukturnya belum berhasil ditentukan. Keduanya terurai dengan lambat pada suhu ruangan. Torium dapat membentuk anion prismatik trigonal bertudung tunggal [Th(CH3)7]3− heptametiltorat. Anion ini dapat bersenyawa menjadi garam [Li(tmeda)]3[ThMe7] (tmeda= Me2NCH2CH2NMe2). Walaupun satu gugus metil tersebut terikat hanya dengan atom torium (jarak Th–C 257,1 pm) dan enam gugus metil lainnya terikat menghubungkan litium dengan karbon (jarak Th–C 265,5–276,5 pm), ketujuh gugus metil tersebut berperilaku sama dalam larutan. Tetrametiltorium, Th(CH3)4, tidaklah diketahui keberadaannya, tetapi aduk senyawa ini distabilkan oleh ligan fosfina.[37]
Keberadaan
[sunting | sunting sumber]Pembentukan torium
[sunting | sunting sumber]232Th adalah nuklida purba yang telah berwujud dalam keadaan seperti sekarang sejak 10 milyar tahun yang lalu. Torium tercipta di dalam inti bintang sekarat melalui proses-r dan terhambur ke seluruh galaksi oleh supernova dan tabrakan bintang neutron.[65][66] Huruf "r" pada proses-r berasal dari frasa "rapid neutron capture" (tangkapan neutron yang cepat). Tangkapan ini terjadi di dalam supernova runtuh-inti, di mana inti benih yang berat seperti 56Fe dengan cepat menangkap neutron melawan garis tetesan neutron; neutron tertangkap dengan lebih cepat daripada kecepatan nuklida menjalani peluruhan beta menjadi nuklida stabil. Penangkapan neutron adalah satu-satunya cara bintang mensintesis unsur-unsur yang lebih berat daripada besi. Ini karena terdapat peningkatan sawar Coulomb yang membuat interaksi antar partikel bermuatan lebih sulit terjadi pada atom bernomor atom tinggi. Sebenarnya pula, reaksi fusi atom yang lebih berat dari 56Fe bersifat endotermik.[67] Karena stabilitas nuklida hilang dengan tiba-tiba ketika mencapai 209Bi, proses-r merupakan satu-satunya proses pada nukleosintesis bintang yang dapat menciptakan unsur torium dan uranium; proses-proses lainnya terlalu lambat dan inti antara yang terbentuk menjalani peluruhan alfa sebelum berhasil menangkap neutron yang cukup untuk menjadi unsur torium dan uranium.[65][68][69]

Dalam alam semesta, torium adalah salah satu dari unsur-unsur primordial yang paling langka, sebab torium adalah satu dari dua unsur (yang lainnya uranium) yang hanya dapat diciptakan dari proses-r. Selain itu, torium juga telah secara perlahan meluruh menjadi unsur lainnya sejak pertama kali diciptakan. Unsur-unsur primordial lainnya yang lebih langka daripada torium adalah tulium, lutesium, tantalum, renium, dan uranium.[65][67] Pada waktu yang lampau, kelimpahan torium dan uranium diperkaya oleh peluruhan isotop plutonium dan kurium. Torium diperkaya relatif terhadap uranium melalui peluruhan 236U menjadi 232Th dan deplesi alami 235U. Sekarang, hal ini tidaklah berkontribusi lagi kepada kelimpahan torium.[70]
Dalam kerak Bumi, torium lebih berlimpah dengan kelimpahan sebesar 8,1 bagian per juta (ppm). Torium merupakan salah satu unsur berat yang paling melimpah. Kelimpahannya menghampiri kelimpahan timbal (13 ppm) dan lebih berlimpah daripada timah (2,1 ppm).[71] Hal ini terjadi karena torium cenderung bersenyawa menjadi mineral oksida yang tidak tenggelam ke dalam inti Bumi; ia digolongkan sebagai litofil. Senyawa-senyawa torium umumnya juga kurang larut dalam air. Oleh karenanya, walaupun unsur-unsur logam refraktori memiliki kelimpahan relatif yang sama di Bumi maupun di Tata Surya, torium lebih terjangkau di kerak Bumi daripada logam-logam golongan platina berat lainnya.[72]
Di Bumi
[sunting | sunting sumber]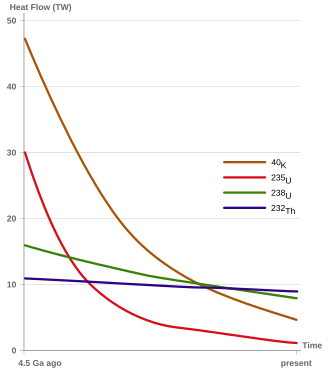
Hampir semua torium yang ditemukan di alam biasanya berisotop 232Th. Isotop ini merupakan isotop torium yang berumur paling panjang dan stabil. Waktu paruhnya sebanding dengan usia alam semesta.[23] Panas yang dihasilkan dari peluruhan radioaktif isotop ini berkontribusi terbesar terhadap panas internal bumi; kontributor panas bumi lainnya melibatkan radionuklida-radionuklida primordial yang berumur pendek, seperti 238U, 40K, dan 235U berturut-turut. (Pada saat Bumi terbentuk, 40K dan 235U berkontribusi lebih besar, tetapi keduanya meluruh dengan cepat. Karena itu, sekarang hanya 232Th dan 238U yang mendominasi.)[77]
Peluruhan isotop 232Th berkontribusi terhadap penurunan kandungan torium di Bumi secara perlahan-lahan. Kandungan torium di Bumi saat ini hanya sebesar 85% dari kandungan awal torium saat Bumi terbentuk.[48]
Isotop torium lainnya berumur pendek. Hanya 230Th yang biasanya dapat dideteksi. Torium ini berada dalam keadaan kesetimbangan sekuler dengan induk 238U. 230Th menduduki sekitar 0,04% torium alami.[23][h] Torium hanya ditemukan sebagai komponen minor dalam kebanyakan mineral. Karena itu, torium sebelumnya dianggap merupakan unsur yang langka.[79] Tanah biasanya mengandung sekitar 6 ppm torium.[80] Di alam, torium berwujud dalam keadaan oksidasi +4.[79] Karena keradiokatifannya, mineral-mineral yang mengandung torium sering kali berbentuk metamik (amorf). Ini disebabkan oleh perusakan struktur kristal oleh radiasi alfa yang dihasilkan torium.[81] Contoh ekstremnya adalah mineral ekanit (Ca,Fe,Pb)2(Th,U)Si8O20, yang hampir tidak pernah ditemukan dalam keadaan non-metamik karena kandungan toriumnya.[82]
Monasit (terdiri atas utamanya persenyawaan fosfat berbagai unsur tanah jarang) adalah sumber torium komersial yang penting karena ditemukan dalam endapan yang besar di seluruh dunia, utamanya di India, Afrika Selatan, Brazil, Australia, dan Malaysia. Monasit rata-ratanya mengandung sekitar 2,5% torium, walaupun kadang-kadang terdapat endapan monasit yang mengandung hingga 20% torium.[79][83] Monasit secara kimiawi relatif tidak reaktif dan ditemukan sebagai pasir yang berwarna kuning atau cokelat. Reaktivitasnya yang rendah membuatnya sulit untuk diekstraksi untuk mendapatkan torium.[79] Mineral alanit (komposisi utamanya berupa silikat-hidroksida berbagai logam) dapat mangandung 0,1–2% torium. Mineral zirkon (komposisi utamanya berupa zirkonium silikat, ZrSiO4) dapat mengandung paling banyak 0,4% torium.[79]
Torium dioksida ditemukan dalam mineral langka torianit. Karena senyawanya yang isotipik dengan uranium dioksida, kedua senyawa aktinida dioksida ini dapat saling larut dalam keadaan padat (membentuk larutan padat). Nama mineral yang mengandung kedua senyawa ini berbeda-beda bergantung pada kandungan ThO2 dalam mineral.[79][i] Torit (komposisi utamanya berupa torium silikat, ThSiO4), juga memiliki kandungan torium yang tinggi dan juga adalah mineral di mana torium pertama kali ditemukan.[79] Dalam mineral torium silikat , ion Th4+ dan SiO4−4 sering kali digantikan dengan ion M3+ (M= Sc, Y, or Ln) dan fosfat (PO3−4).[79] Karena torium dioksida sangat tidak larut, torium biasanya tidak menyebar dengan cepat ketika dilepaskan ke lingkungan sekitar. Ion Th4+ bersifat larut, terutama di tanah yang asam. Dalam kondisi tersebut, konsentrasi torium dapat mencapai 40 ppm.[48]
Sejarah
[sunting | sunting sumber]Laporan penemuan yang keliru
[sunting | sunting sumber]
Pada tahun 1815, seorang kimiawan Swedia Jöns Jacob Berzelius menganalisis sebuah sampel gadolinit yang berasal dari tambang tembaga di Falun, Swedia tengah. Ia mencermati adanya jejak-jejak mineral putih yang terkandung dalam sampel tersebut dan dengan berhati-hatinya berasumsi bahwa jejak tersebut merupakan oksida unsur baru yang belum diketahui. Berzelius sebelumnya telah menemukan dua unsur baru, yaitu serium dan selenium, tetapi ia juga pernah sekali melakukan kesalahan di depan umum dengan mengumumkan penemuan unsur baru "gahnium", yang ternyata merupakan seng oksida.[85] Berzelius pada tahun 1817 secara pribadi menamai unsur sangkaan tersebut sebagai "thorium"[86] dan oksida unsur tersebut sebagai "thorina". Nama ini berasal dari Thor, seorang dewa petir Nordik.[87] Pada tahun 1824, setelah endapan mineral yang sama ditemukan di Vest-Agder, Norwegia, Berzelius menarik penemuannya karena mineral tersebut (yang kemudian dinamai xenotim) ternyata mayoritas komposisinya adalah itrium ortofosfat.[31][85][88][89]
Penemuan torium
[sunting | sunting sumber]
Pada tahun 1828, Morten Thrane Esmark menemukan sebuah mineral hitam di pulau Løvøya, wilayah Telemark, Norwegia. Esmark adalah pendeta Norwegia dan juga seorang ahli mineralogi amatir yang mempelajari berbagai mineral yang ada di Telemark. Di sana, ia menjabat sebagai seorang vikep. Seringkali, dia mengirimkan berbagai spesimen yang menarik ke ayahnya, Jens Esmark, seorang ahli mineralogi ternama dan profesor mineralogi dan geologi di Universitas Kerajaan Frederick (sekarang Universitas Oslo) di Christiania (sekarang Oslo).[90] Jens Esmark menentukan bahwa spesimen yang dia terima dari anaknya merupakan mineral yang belum diketahui sebelumnya. Ia kemudian mengirim sampel tersebut kepada Berzelius untuk diperiksa lebih lanjut. Berzelius menentukan bahwa sampel tersebut mengandung unsur baru.[31] Ia mempublikasikan penemuannya pada tahun 1829 setelah mengisolasi sampel torium yang tak murni dari reduksi KThF5 menggunakan logam kalium.[91][92][93] Berzelius menggunakan kembali nama "Thorium" (torium) [91][94] untuk merujuk pada unsur baru tersebut, dan menamakan sumber mineral unsur tersebut sebagai "thorit" (torit).[31]
Berzelius melakukan beberapa karakterisasi awal logam baru tersebut beserta senyawa-senyawanya. Ia menentukan dengan benar bawah rasio massa torium dengan oksigen pada torium oksida adalah 7,5 (nilai yang aktual adalah 7,3). Namun ia mengasumsikan bahwa unsur baru tersebut bervalensi dua dan bukannya bervalensi empat, sehingga perhitungan massa atomnya menjadi 7,5 kali massa atom oksigen (120 amu); massa atom torium yang sebenarnya adalah 15 kali massa atom oksigen.[j] Ia menentukan bahwa torium adalah logam yang sangat elektropositif, melebihi elektropositivitas serium dan di bawah zirkonium.[95] Logam torium murni (99%) diisolasi pertama kalinya pada tahun 1914 oleh dua usahawan Belanda Dirk Lely Jr. dan Lodewijk Hamburger.[k]
Penggolongan dan kegunaan awal
[sunting | sunting sumber]Pada tabel periodik yang diterbitkan oleh Dmitri Mendeleev pada tahun 1869, torium dan unsur-unsur tanah jarang lainnya diletakkan di luar tabel utama di akhir ujung setiap periode setelah logam alkali tanah. Hal ini mencerminkan keyakinan pada saat itu bahwa torium dan unsur-unsur tanah jarang bervalensi dua. Setelah diketahui bahwa unsur-unsur tanah jarang kebanyakan bervalensi tiga dan torium bervalensi empat, Mendeleev memindahkan serium dan torium ke golongan IV pada tahun 1871. Golongan IV ini juga mengandung unsur-unsur golongan karbon (golongan 14) dan golongan titanium (golongan 4). Ini karena keadaan oksidasi semua unsur-unsur golongan tersebut maksimum adalah +4.[98][99] Serium kemudian dipindahkan dari tabel utama ke tabel terpisah yang mengandung deret lantanida, sedangkan torium tetap berada dalam golongan IV karena sifat-sifatnya yang dianggap mirip dengan unsur lain golongan tersebut, seperti titanium dan zirkonium.[100][l]
Walaupun telah ditemukan pada tahun 1828, torium pertama kali digunakan hanya sejak tahun 1885, ketika kimiawan Austria Carl Auer von Welsbach menciptakan kaus lampu, yakni sumber cahaya portabel yang mampu menghasilkan cahaya dari pijaran torium oksida ketika dipanaskan oleh bahan bakar gas.[31]
Radioaktivitas
[sunting | sunting sumber]
Torium pertama kali diamati bersifat radioaktif pada tahun 1898 oleh kimiawan Jerman Gerhard Carl Schmidt. Setelahnya pada tahun yang sama, secara terpisah, fisikawan Polandia-Prancis Marie Curie juga mengamati hal yang sama. Torium adalah unsur kedua yang ditemukan beradioaktivitas, setelah uranium yang radioaktivitasnya ditemukan oleh fisikawan Prancis Henri Becquerel pada tahun 1896.[101][102][103] Bermula dari tahun 1899, fisikawan Selandia Baru Ernest Rutherford dan insinyur listrik Amerika Robert Bowie Owens mulai mengkaji radiasi yang dihasilkan torium. Pengamatan awal menunjukkan bahwa radiasi torium bervariasi secara signifikan. Keduanya menentukan bahwa variasi ini disebabkan oleh anak inti torium yang berbentuk gas dan berumur pendek. Anak inti tersebut kemudian ditemukan sebagai unsur yang baru dan sekarang dinamakan radon. Radon adalah satu-satunya unsur radioaktif langka yang ditemukan di alam sebagai anak inti dari torium daripada dari uranium.[104]
Setelah mempertimbangkan kontribusi radon, Rutherford, yang setelahnya bekerja di bawah bimbingan fisikawan Britania Frederick Soddy, menunjukkan pada tahun 1900–1903 bagaimana torium meluruh dengan laju yang tetap seiring waktu menjadi sederetan unsur-unsur lain. Pengamatan ini berimbas pada identifikasi waktu paruh sebagai salah satu akibat dari peluruhan alfa.[105] Efek biologis radiasi tersebut kemudian ditemukan pada tahun 1903.[106] Penemuan fenomena radioaktivitas yang baru tersebut membangkitkan semangat para ilmuwan dan masyarakat umum. Pada tahun 1920-an, radiaktivitas torium dipromosikan sebagai obat untuk penyakit rematik, diabetes, dan impotensi seksual. Penggunaan torium untuk tujuan seperti ini kemudian dilarang di Amerika Serikat pada tahun 1932, setelah investigasi pemerintah federal Amerika mengenai efek-efek radioaktivitas terhadap kesehatan seseorang.[107] Sebelum dilarang, 10.000 orang di Amerika Serikat telah disuntik torium sewaktu menjalani diagnosis sinar-X; mereka kemudian ditemukan menderita masalah kesehatan seperti leukimia dan kromosom abnormal.[48] Ketertarikan publik dengan radioaktivitas menurun pada akhir tahun 1930-an.[107]
Penggolongan lebih lanjut
[sunting | sunting sumber]
Sampai dengan akhir abad ke-19, para kimiawan secara bulat setuju bahwa torium dan uranium memiliki sifat-sifat kimia yang beranalogi dengan hafnium dan wolfram; keberadaan unsur-unsur lantanida pada baris periode ke-6 tabel periodik dianggap hanya sebagai pengecualian saja. Pada tahun 1892, kimiawan Britania Henry Bassett mempostulatkan keberadaan baris periode tambahan di bawah lantanida untuk mengakomodasi baik unsur-unsur yang telah diketahui maupun yang belum ditemukan. Henry Bassett berpendapat bahwa torium dan uranium beranalogi dengan unsur-unsur lantanida. Pada tahun 1913, fisikawan Denmark Niels Bohr mempublikasikan suatu model teoretis atom beserta dengan orbital-orbital elektronnya. Model ini dengan cepat mendapat penerimaan yang luas. Berdasarkan model ini, unsur-unsur periode ke-7 pada tabel periodik haruslah kelopak-f-nya terisi penuh terlebih dahulu sebelum kelopak-d terisi, seperti pada unsur-unsur lantanida periode ke-6 yang mendahului logam-logam transisi 5d.[98] Keberadaan deret unsur transisi dalam kedua (unsur-unsur aktinida) ini tidaklah diterima luas sebelum ditentukannya struktur elektron unsur-unsur lantanida.[108] Bohr memberikan pendapat bahwa orbital 5f mungkin tidak terisi terlebih dahulu pada unsur-unsur setelah uranium.[98]
Hanya setelah penemuan unsur-unsur transuranium pertama, yang mayoritas berkeadaan oksidasi +3 dan +4 seperti pada lantanida, barulah disadari bahwa unsur-unsur aktinida semuanya sebenarnya mengisi orbital-f terlebih dahulu sebelum orbital-d. Kemiripan kimiawi unsur-unsur awal aktinida dengan logam transisi sekarang dianggap sebagai pengecualian daripada sebagai kecenderungan sifat yang berlanjut.[109] Pada tahun 1945, fisikawan Amerika Glenn T. Seaborg dan anggota tim risetnya menemukan unsur transuranium amerisium dan kurium. Seaborg mengagaskan konsep aktinida setelah menyadari bahwa torium adalah anggota ke-2 deret unsur aktinida blok-f, beranalogi dengan unsur-unsur lantanida daripada dengan unsur hafnium pada periode ke-4 blok-d.[100][m]
Penghentian penggunaan torium secara perlahan
[sunting | sunting sumber]Pada tahun 1990-an, kebanyakan penggunaan torium yang tidak memanfaatkan sifat-sifat radioaktivitasnya menurun drastis karena kekhawatiran akan keselamatan dan dampak lingkungan torum; hal ini juga diiringi oleh penemuan bahan pengganti torium yang lebih aman.[31][112] Walaupun radioaktif, torium masih digunakan pada pelbagai aplikasi yang pengganti alternatif toriumnya masih belum ditemukan. Dalam suatu kajian tahun 1981 oleh Laboratorium Nasional Oak Ridge Amerika Serikat, diperkirakan bahwa penggunaan kaus lampu torium setiap akhir minggu adalah aman bagi seseorang.[112] Namun, ini tidaklah aman bagi para pekerja manufaktur kaus tersebut maupun pada lingkungan tanah tempat pabrik kaus tersebut berada.[113] Beberapa produsen kaus lampu telah mengubah bahan materi kaus, misalnya dengan itrium.[114] Pada tahun 2007, beberapa perusahaan masih memproduksi dan menjual kaus lampu torium tanpa pemberitahuan informasi yang memadai tentang radioaktivitas produk tersebut. Beberapa perusahaan bahkan mengklaim palsu bahwa produk mereka tidak bersifat radioaktif.[112][115]
Tenaga nuklir
[sunting | sunting sumber]
Torium telah digunakan sebagai sumber energi pada skala purwarupa. Reaktor berbasis torium pertama kali didirikan di Indian Point Energy Center di Buchanan, New York, Amerika Serikat pada tahun 1962.[116] Salah satu sumber terbesar torium di dunia berada di India. Pada tahun 1950-an, pemerintah India menargetkan pencapaian swasembada energi melalui program tenaga nuklir tiga tahap India, yang tahap ketiganya adalah pembanguan reaktor nuklir torium.[117][118] Di kebanyakan negara, uranium secara relatif lebih berlimpah daripada torium, sehingga kemajuan pembangunan reaktor berbasis torium di negara lain berjalan lambat.[119] Riset berskala besar dimulai pada tahun 1996 oleh Badan Tenaga Atom Internasional untuk mengkaji penggunaan reaktor torium; setahun kemudian, Departemen Energi Amerika Serikat memulai riset mereka.
Pada abad ke-21, potensi torium dalam mengurangi proliferasi nuklir dan karakteristik limbahnya berujung pada ketertarikan kembali kepada siklus bahan bakar torium.[120][121][122] Pemerintah India memproyeksikan pencapaian pemenuhan 30% konsumsi listrik menggunakan torium pada tahun 2050. Pada bulan Februari 2014, Pusat Penelitian Atom Bhabha di Mumbai, India memamerkan desain "reaktor nuklir generasi mendatang" terbaru mereka yang menggunakan torium sebagai inti bahan bakar reaktor, dinamai "Advanced Heavy Water Reactor" (AWHR) atau Reaktor air berat tingkat lanjut. Kepala Komisi Energi Atom India pada tahun 2009 mengatakan bahwa India memiliki tujuan jangka panjang untuk berswasembada energi menggunakan sumber daya mineral India yang kaya akan torium."[123]
Senjata nuklir
[sunting | sunting sumber]Sewaktu sejumlah gram plutonium pertama kali diproduksi pada Proyek Manhattan, ditemukan bahwa isotop minor 240Pu menjalani fisi spontan yang signifikan. Hal ini menjadikan senjata nuklir jenis bedil berbahan bakar plutonium dipertanyakan kelayakannya. Untuk menghindari masalah tersebut, tim riset Los Alamos mulai mendesain senjata jenis implosi. Di saat yang bersamaan, tim riset Chicago juga mendiskuksikan penyelesaian masalah tersebut dengan menggunakan desain reaktor baru. Eugene Wigner mengusulkan penggunaan plutonium yang terkontaminasi 240Pu tersebut untuk mendorong transmutasi torium menjadi 233U dalam suatu reaktor konverter khusus. Dihipotesiskan bahwa 233U tersebut akan dapat digunakan pada senjata nuklir jenis bedil, walaupun terdapat pula kekhawatiran akan kontaminasi 232U. Kemajuan pada desain senjata jenis implosi Los Alamos membuat pengembangan reaktor konverter ini tidak dilanjutkan. Tetapi desain reaktor ini berpengaruh kuat terhadap pengembangan energi nuklir selanjutnya. Dalam rancangannya, terdapat deskripsi mendetail mengenai penggunaan reaktor berpendingin dan bermoderator air tingkat tinggi yang mirip dengan reaktor kapal laut dan reaktor pembangkit listrik di kemudian hari.[124]
Semasa Perang Dingin, Amerika Serikat mempertimbangkan kemungkinan penggunaan 232Th sebagai sumber 233U untuk kegunaan bom nuklir. Pemerintah Amerika meluncurkan sebuah bom uji pada tahun 1955.[125] Dari hasil pengujian bom tersebut, disimpulkan bahwa bom berbahan 233U cukup ampuh, tetapi tidak memiliki "keunggulan teknis" yang berkelanjutan dibandingkan dengan bom kontemporer berbahan uranium–plutonium.[126] Hal ini terutama karena 233U sulit diproduksi dalam keadaan berisotop murni.[125] Logam torium digunakan dalam hohlraum senjata nuklir W71 milik Amerika Serikat.[127]
Produksi
[sunting | sunting sumber]| Negara | Jumlah cadangan |
|---|---|
| 1070 | |
| 632 | |
| 595 | |
| 595 | |
| 380 | |
| 374 | |
| 300 | |
| 172 | |
| 155 | |
| 148 | |
| 100 | |
| 87 | |
| 86 | |
| 60.5 | |
| 50 | |
| 50 | |
| Negara lainnya | 1725 |
| Total seluruh dunia | 6579,5 |
Permintaan torium yang rendah membuat pembangunan tambang khusus ekstraksi torium tidak menguntungkan. Karena itu, torium hampir selalu diekstraksi bersamaan dengan logam-logam tanah jarang lainnya. Logam-logam tanah jarang ini pun dapat merupakan produk sampingan produksi mineral lain.[128] Kebanyakan torium di dunia diproduksi sebagai produk sampingan dari ekstraksi mineral monasit. Sumber mineral lainnya seperti torit mengandung lebih banyak torium dan dapat diekstraksi untuk mendapatkan torium apabila permintaan meningkat.[129] Distribusi sumber daya torium di dunia saat ini kurang diketahui karena permintaannya yang rendah membuat usaha eksplorasi torium jarang dilakukan.[130] Pada tahun 2014, produksi konsentrat monasit dunia, yang darinya torium dapat diekstraksi, mencapai 2700 ton.[131]
Lajur produksi torium pada umumnya melibatkan pengonsentrasian mineral bertorium, ekstraksi torium dari konsentrat tersebut, dan pemurnian torium. Jika diperlukan, torium dapat diubah setelahnya menjadi senyawa-senyawa turunannya, seperti torium dioksida.[132]
Pengonsentrasian dan ekstraksi
[sunting | sunting sumber]Terdapat dua kategori mineral pada proses pengonsentrasian torium, yakni mineral primer dan mineral sekunder. Endapan mineral primer terdapat pada magma asam granit dan pegmatit. Keduanya berkonsentrat monasit secara lokal, tetapi ukurannya kecil-kecil. Endapan mineral sekunder terdapat pada muara sungai daerah pegunungan bergranit. Pada endapan ini, torium diperkaya bersamaan dengan logam mineral berat lainnya.[41] Konsentrasi awal torium dalam mineral bervariasi tergantung pada jenis endapan.[132]
Untuk endapan primer, pegmatit, yang biasanya didapatkan dari penambangan, digiling menjadi bagian-bagian yang kecil, kemudian diflotasikan. Karbonat logam alkali tanah dalam mineral dipisahkan melalui reaksi dengan hidrogen klorida. Ini kemudian diikuti oleh proses pengentalan, penyaringan, dan kalsinasi. Hasilnya adalah konsentrat dengan kandungan logam tanah jarang yang dapat mencapai 90%.[132] Untuk endapan sekunder, pasir-pasir yang didapatkan pertama-tama dipisahkan terlebih dahulu melalui gravitasi, selanjutnya dipisahkan menggunakan magnet secara bertahap-tahap (dari magnet berkekuatan rendah sampai dengan magnet berkekuatan tinggi). Monasit yang dihasilkan dari metode ini kemurniannya dapat mencapai hingga 98%.[132]
Ekstraksi torium pada industri abad ke-20 mengandalkan perlakuan konsentrat monasit dengan asam sulfat pekat yang panas di dalam wadah yang terbuat dari besi cor. Ini kemudian diikuti oleh proses pengendapan selektif setelah pengenceran dengan air. Keberhasilan metode ini bergantung pada spesifikasi dan ukuran butir konsentrat. Oleh karenanya, terdapat pula banyak metode-metode alternatif lainnya yang telah diusulkan, tetapi hanya satu yang telah terbukti efektif dan ekonomis, yakni perlakuan konsentrat dengan larutan natrium hidroksida panas. Metode ini sedikit lebih mahal daripada metode perlakuan asam sulfat pekat panas, tetapi metode ini dapat menghasilkan logam torium berkemurnian lebih tinggi; terutamanya metode ini mampu memisahkan senyawa fosfat dari konsentrat.[132]
Ekstraksi menggunakan asam
[sunting | sunting sumber]Untuk mengekstraksi torium, konsentrat monasit dicerna terlebih dahulu menggunakan asam. Proses ini terdiri dari dua tahap dan melibatkan penggunaan asam sulfat berkepekatan hingga 93% pada suhu 210–230 °C. Pertama-tama, asal sulfat pekat dalam jumlah >60% massa konsentrat ditambahkan dan dipanaskan di dalam wadah, diikuti oleh penambahan pasir monasit. Oleh karena proses pelarutan konsentrat ini bersifat eksotermik, pasir monasit yang ditambahkan ke dalam asam haruslah dilakukan secara perlahan. Hal ini menyebabkan mengentalnya campuran reaksi menjadi seperti bubur dan kemudian memadat seiring dengan terbentuknya produk-produk reaksi. Pada tahap kedua, asam sulfat berasap yang berlebih kemudian ditambahkan ke dalam campuran tersebut dan suhu campuran dijaga tetap (210–230 °C) selama lebih dari 5 jam. Konsentrasi asam sulfat yang digunakan memengaruhi laju reaksi dan kekentalan campuran. Laju reaksi dan kekentalan meningkat seiring dengan meningkatnya konsentrasi asam sulfat yang digunakan. Namun, kekentalan campuran reaksi yang berlebihan dapat menghambat laju reaksi. Peningkatan suhu reaksi juga dapat digunakan untuk meningkatkan laju reaksi, tetapi suhu lebih dari 300 °C harus dihindari karena akan menyebabkan terbentuknya torium pirofosfat yang tak larut. Sebaliknya, apabila suhunya kurang dari 200 °C, reaksi berjalan dengan lambat dan menjadi tidak praktis. Untuk menghindari terbentuknya endapan-endapan yang menutupi permukaan pasir monasit, massa asam yang digunakan haruslah dua kali lipat lebih banyak daripada massa pasir.[132]
Setelah proses pencernaan selesai, campuran reaksi didinginkan ke suhu 70 °C dan diencerkan dengan air dingin sejumlah 10 kali lipat volume campuran. Garam-garam torium dan logam tanah jarang lain yang dihasilkan akan larut ke dalam air, sementara sisa-sisa pasir monasit yang tidak bereaksi mengendap ke bawah wadah. Torium kemudian dapat dipisahkan sebagai garam fosfat dengan mengatur pH larutan tersebut. Pada pH 1,3, garam fosfat torium akan secara selektif mengendap, sementara garam-garam logam tanah jarang lainnya hanya akan mengendap pada pH >2.[132]
Ekstraksi menggunakan basa
[sunting | sunting sumber]Dalam metode ini, ekstraksi dilakukan dengan larutan natrium hidroksida 30–45% pada suhu 140 °C selama tiga jam. Suhu yang terlalu tinggi harus dihindari karena akan menyebabkan pembentukan torium oksida dan uranium oksida yang tak larut dalam filtrat. Selain itu, konsentrasi basa yang terlalu rendah juga akan memperlambat laju reaksi. Oleh karena kondisi reaksi yang cukup lembut, pasir monasit yang digunakan dalam ekstraksi harus berukuran partikel di bawah 45 μm. Campuran reaksi kemudian disaring dan hasil saringan padat yang didapatkan mengandung campuran hidroksida logam-logam tanah jarang, torium hidroksida, dan natrium diuranat, sedangkan larutan filtrat yang didapatkan mengandung trinatrium fosfat. Trinatrium fosfat ini dapat mengkristal sebagai kristal dekahidrat ketika larutan didinginkan di bawah suhu 60 °C.[132]
Campuran padat hidroksida yang didapatkan kemudian dilarutkan ke dalam larutan asam klorida 37% pada suhu 80 °C. Bagian-bagian yang tak larut disaring keluar, dan filtrat yang didapatkan diendapkan menggunakan larutan natrium hidroksida 47%. Senyawa torium dan uranium akan mengendap pada pH 5,8, sedangkan senyawa logam-logam tanah jarang lainnya mengendap pada pH yang lebih tinggi. Endapatan senyawa torium dan uranium tersebut kemudian dilarutkan dalam asam nitrat untuk pemisahan lebih lanjut.[132]
Pemurnian
[sunting | sunting sumber]Hasil endapan baik dari ekstraksi menggunakan asam maupun basa haruslah dimurnikan lebih lanjut agar dapat digunakan dalam pelbagai aplikasi nuklir. Sebelumnya, pemurnian torium dicapai dengan melakukan pelarutan dan rekristalisasi secara berulang-ulang. Pada zaman sekarang, teknik tersebut telah digantikan dengan metode ekstraksi pelarut lawan arus berjenjang yang melibatkan kompleksasi Th4+. Ekstraksi ini menggunakan larutan tributil fosfat (TBP) dalam minyak tanah.[132] Proses Amex (amine extraction) yang menggunakan berbagai macam basa-basa amina juga dapat digunakan untuk memisahkan torium dari uranium dan logam-logam tanah jarang lainnya.[133]
Aplikasi modern
[sunting | sunting sumber]Kebanyakan penggunaan torium yang tidak berkaitan dengan radioaktivitasnya telah menurun sejak tahun 1950-an.[134] Hal ini disebabkan oleh kekhawatiran akan dampak lingkungan radioaktivitas torium beserta produk-produk peluruhannya.[31][112]
Torium mayoritas digunakan dalam bentuk torium dioksida daripada dalam bentuk logam murni. Senyawa torium dioksida memiliki titik lebur 3300 °C (6000 °F), merupakan yang tertinggi di antara semua senyawa oksida yang diketahui.[48] Hal ini menyebabkan senyawa ini tetap berwujud padat di dalam kobaran api. Selain itu, torium dioksida juga meningkatkan tingkat kecerahan api tersebut. Sifat-sifat inilah yang menjadi sebab digunakannya torium dioksida dalam kaus lampu.[135] Semua senyawa akan memancarkan energi (berpijar) pada suhu yang tinggi, tetapi sinar yang dipancarkan torium hampir semuanya termasuk dalam spektrum cahaya tampak, sehingga tampak lebih cerah.[51] Walaupun masih sering dijumpai, penggunaan torium dioksida dalam kaus lampu telah digantikan oleh itrium secara perlahan sejak akhir tahun 1990-an.[136]

Dalam produksi filamen lampu pijar berbahan wolfram, rekristalisasi wolfram dapat ditekan secara signifikan dengan penambahan sejumlah kecil torium dioksida ke dalam bubuk sinter wolfram.[134] Penambahan sejumlah kecil torium dioksida ke katode panas wolfram secara signifikan menurunkan fungsi kerja elektron. Sebagai akibatnya, elektron terpancarkan pada suhu yang jauh lebih rendah.[31] Torium membentuk lapisan berketebalan satu atom yang menyelimuti permukaan wolfram. Fungsi kerja dari permukaan torium menurun kemungkinan karena terbentuknya medan listrik pada antarmuka torium dan wolfram yang disebabkan oleh elektropositivitas torium yang lebih besar.[137] Sejak tahun 1920-an, kawat wolfram bertorium telah digunakan dalam tabung-tabung elektronik berserta katode dan antikatode pada tabung sinar-X dan penyearah. Oleh karena torium bereaksi dengan oksigen dan nitrogen dari atmosfer, torium juga berperan sebagai penangkap zat pengotor dalam tabung vakum. Penemuan transistor pada tahun 1950-an secara signifikan menyebabkan penurunan penggunaan torium untuk tujuan tersebut.[134] Torium dioksida juga digunakan dalam las busur wolfram gas (gas tungsten arc welding, disingkat GTAW) untuk meningkatkan kekuatan elektrode wolfram dan stabilitas busur pada suhu tinggi.[31] Penggunaan torium dioksida untuk tujuan ini secara perlahan telah digantikan dengan senyawa oksida lainnya, seperti oksida dari zirkonium, serium, dan lantanum.[138][139]
Torium dioksida digunakan juga dalam bahan keramik tahan panas, misalnya pada krus laboratorium. Torium dioksida dapat digunakan sebagai bahan utama keramik maupun sebagai zat tambahan ke dalam zirkonium dioksida.[31] Paduan 90% platina dan 10% torium adalah katalis yang efektif dalam pengoksidasian amonia menjadi berbagai senyawa oksida nitrogen. Namun, ia telah digantikan dengan logam paduan 95% platina dan 5% rodium karena sifat-sifat mekanik dan daya tahannya yang lebih baik.[134]
Ketika ditambahkan ke dalam kaca, torium dioksida membantu meningkatkan indeks refraksi dan menurunkan dispersi kaca. Kaca-kaca seperti ini digunakan sebagai lensa berkualitas tinggi pada kamera dan instrumen ilmiah.[42] Radiasi yang dihasilkan oleh lensa tersebut dapat menyebabkan lensa menjadi kuning secara perlahan, walaupun dampak kesehatannya minimal.[140] Lensa yang telah menguning tersebut dapat dikembalikan ke keadaan asalnya dengan memaparkan lensa tersebut dengan radiasi ultraviolet. Torium dioksida telah digantikan penggunaannya untuk tujuan seperti ini oleh senyawa oksida tanah jarang lainnya.[134]
Torium tetrafluorida digunakan sebagai bahan antirefleksi pada pelapis optik berlapis. Torium tetrafluorida transparan terhadap gelombang elektromagnetik yang berpanjang gelombang antara 0,35–12 µm. Rentang gelombang elektromagnetik ini meliputi sinar ultraviolet dekat, cahaya tampak, dan sinar inframerah. Radiasi yang disebabkan torium tetrafluorida utamanya adalah partikel alfa. Partikel ini dapat dihentikan dengan lapisan tipis bahan materi lain.[141] Penggantian torium tetrafluorida untuk tujuan ini telah dalam pengembangan sejak tahun 2010.[142]
Potensi kegunaan untuk energi nuklir
[sunting | sunting sumber]Sumber tenaga nuklir utama dalam sebuah reaktor nuklir adalah reaksi fisi sebuah nuklida yang diinduksi oleh neutron. Bahan fisil sintetik[e] seperti inti 233U dan 239Pu dapat dibiakkan melalui penangkapan neutron oleh nuklida 232Th dan 238U yang keduanya terdapat di alam. 235U yang terdapat di alam juga bersifat fisil.[143][144][n] Dalam siklus bahan bakar torium, isotop fertil 232Th dibombardir oleh neutron lambat dan menjalani penangkapan neutron menjadi 233Th. Isotop ini kemudian menjalani peluruhan beta dua kali menjadi 233Pa dan kemudian 233U:[31]
- 232
90Th + n → 233
90Th + γ 233
91Pa 233
92U
233U bersifat fisil dan dapat digunakan sebagai bahan bakar nuklir selayaknya 235U dan 239Pu. Ketika 233U menjalani fisi nuklir, neutron-neutron yang dipancarkannya dapat menumbuk inti 232Th lebih lanjut, sehingga siklus bersinambung.[31] Siklus ini berparalel dengan siklus bahan bakar uranium dalam reaktor pembiak cepat yang 238U-nya menjalani penangkapan neutron menjadi 239U. 239U kemudian meluruh beta menjadi 239Np dan selanjutnya menjadi 239Pu yang fisil.[145]
Keuntungan
[sunting | sunting sumber]| 237Np | ||||||||||||||
| ↑ | ||||||||||||||
| 231U | ← | 232U | ↔ | 233U | ↔ | 234U | ↔ | 235U | ↔ | 236U | → | 237U | ||
| ↓ | ↑ | ↑ | ↑ | |||||||||||
| 231Pa | → | 232Pa | ← | 233Pa | → | 234Pa | ||||||||
| ↑ | ↑ | |||||||||||||
| 230Th | → | 231Th | ← | 232Th | → | 233Th | ||||||||
| (Nuklida yang berwarna latar kuning memiliki waktu paruh di bawah 30 hari; nuklida yang ditebalkan memiliki waktu paruh lebih dari 1.000.000 tahun; nuklida yang dikotakmerahkan bersifat fisil) | ||||||||||||||
Keuntungan penggunaan torium ada pada kelimpahannya yang lebih besar daripada uranium, sehingga dapat memenuhi permintaan energi dunia dalam jangka waktu lebih lama.[146]
Selain itu, 232Th menyerap neutron lebih mudahnya daripada 238U. 233U yang dihasilkannya pun memiliki probabilitas menjalani fisi lebih besar (92%) daripada 235U (85.5%) ataupun 239Pu (73.5%) seketika tertumbuk neutron.[147] Neutron hasil fisi 233U juga secara rata-rata dihasilkan lebih banyak.[146] Sebuah penangkapan neutron oleh 238U menghasilkan limbah transuranium bersamaan dengan inti fisil 239Pu, tetapi penangkapan neutron yang sama oleh 232Th hanya akan menghasilkan limbah setelah lima kali penangkapan, menghasilkan limbah 237Np. Mayoritas 98–99% inti 232Th tidak akan menjalani penangkapan neutron sebanyak ini karena produk antaranya, yakni 233U dan 235U, akan menjalani fisi, sehingga sangat sedikit limbah transuranium berumur panjang yang dihasilkan. Oleh sebab inilah torium merupakan bahan bakar alternatif yang berpotensi menggantikan uranium dalam bahan bakar MOX (bahan bakar oksida campuran) untuk meminimalisasi penghasilan limbah inti transuranium dan memaksimalkan penghancuran plutonium.[148]
Penggunaan bahan bakar torium berdampak pada kinerja sekaligus keselamatan inti reaktor yang lebih baik karena torium dioksida memiliki titik lebur yang lebih tinggi, konduktivitas termal yang lebih tinggi, dan koefisien pemuaian termal yang lebih rendah.[31] Ia juga secara kimiawi lebih stabil daripada uranium dioksida yang sekarang umumnya dipakai. Ini karena uranium dioksida dapat teroksidasi menjadi triuranium oktoksida (U3O8) yang secara substansial berkurang kepadatannya.[149]
Kekurangan
[sunting | sunting sumber]Bahan bakar torium yang telah habis digunakan selain sulit juga berbahaya untuk diproses kembali karena menghasilkan banyak anak inti 232Th dan 233U yang merupakan pemancar gama yang kuat.[146] Semua metode produksi inti 233U akan menghasilkan ketidakmurnian 232U, baik dari reaksi pengguguran parasitik (n,2n) 232Th, 233Pa, dan 233U yang berakibat pada pelepasan sebuah neutron, ataupun dari penangkapan neutron ganda oleh 230Th yang merupakan ketidakmurnian yang dijumpai pada 232Th alami:[150]
- 230
90Th + n → 231
90Th + γ 231
91Pa 231
91Pa + n → 232
91Pa + γ 232
92U
232U itu sendiri tidaklah begitu berbahaya, tetapi ia dengan cepat meluruh menjadi inti 208Tl yang merupakan pemancar sinar gama yang kuat (232Th juga mengikuti rantai peluruhan yang sama, tetapi waktu paruhnya sangat panjang, sehingga jumlah 208Tl yang dihasilkan dapat diabaikan).[151] Ketidakmurnian yang berupa 232U ini membuat 233U mudah terdeteksi sekaligus berbahaya untuk ditangani. Selain itu, tidaklah praktis untuk memisahkan keduanya. Ini berdampak pada terbatasnya penggunaan 233U sebagai bahan fisil.[150] 233Pa memiliki waktu paruh yang relatif lebih panjang (27 hari) dan penampang lintang neutron yang tinggi. Karenanya, 233Pa adalah racun neutron. Alih-alih 233Pa meluruh cepat menjadi 233U yang berguna, sebagian besarnya mengonsumsi neutron dan berubah menjadi 234U. Sebagai akibatnya, efisiensi reaktor berkurang. Untuk menghindari hal tersebut, 233Pa diekstraksi keluar dari zona aktif reaktor garam cair torium semasa pengoperasiannya, sehingga tiada kesempatan bagi 233Pa untuk menangkap neutron dan sebaliknya hanya akan meluruh menjadi 233U.[152]
Sebelum keuntungan-keuntungan penggunaan torium dapat direalisasikan, teknologi proses iradiasi 232Th dengan neutron beserta pemrosesan lanjutannya perlu dikembangkan lebih jauh.[31] Hal ini memerlukan kemajuan teknologi yang lebih lanjut daripada teknologi dalam siklus bahan bakar uranium dan plutonium. Penelitian-penelitian masih terus dilakukan untuk mengembangkan teknologi tersebut. Selain itu, terdapat pula pendapat bahwa siklus bahan bakar torium tidak memiliki keekonomian yang layak.[153][154][155] Asosiasi Nuklir Dunia memprediksikan bahwa siklus bahan bakar torium tidak akan berkeekonomian layak selama uranium masih tersedia dalam jumlah yang berlimpah.[156]
Bahaya
[sunting | sunting sumber]Bahaya radiologis
[sunting | sunting sumber]
Torium alami meluruh dengan sangat lambat dibandingkan dengan bahan-bahan radioaktif lainnya. Ia memancarkan radiasi alfa yang tidak dapat menembus kulit manusia. Oleh karenanya, penanganan sejumlah kecil torium, seperti pada kaus lampu, dianggap aman, walaupun penggunaannya kemungkinan berisiko.[157] Pemaparan terhadap torium aerosol, seperti pada debu yang terkontaminasi torium, dapat berdampak pada peningkatan risiko kanker paru-paru, pankreas, dan darah. Hal ini disebabkan oleh radiasi alfa yang mampu menembus organ dalam.[157] Paparan internal torium juga dapat meningkatkan risiko penyakit pada hati.[158]
Produk-produk peluruhan 232Th sebagian adalah radium dan radon. Keduanya adalah radionuklida yang lebih berbahaya. Walaupun produk peluruhan torium dihasilkan dalam jumlah yang kecil karena peluruhannya yang sangat lambat, penaksiran keracunan radiologis 232Th haruslah memasukkan kontribusi anak-anak intinya. Beberapa anak intinya merupakan pemancar radiasi gama yang kuat[159] dan dapat berakumulasi dengan cepat setelah peluruhan 232Th bermula.[160] Karena anak-anak inti torium yang berbahaya memiliki titik lebur yang lebih rendah daripada torium dioksida, anak-anak inti tersebut akan menguap dengan mudah setiap kali kaus lampu dipanaskan. Dalam jangka waktu satu jam pertama penggunaan kaus lampu bertorium, anak-anak inti seperti 224Ra, 228Ra, 212Pb, dan 212Bi dilepaskan ke udara bebas.[161] Kebanyakan radiasi yang terpapar kepada konsumen berasal dari penghirupan radium. Diperkirakan dosis radiasinya adalah 0,2 milisievert setiap penggunaan. Nilai ini adalah sekitar sepertiga dosis pemaparan yang diterima dalam pemeriksaan mamografi.[162]
Walaupun dosis radiasi dari satu kaus lampu tidaklah bermasalah, hal ini akan menjadi bermasalah apabila kaus-kaus lampu dikumpulkan bersama dalam jumlah besar, seperti yang terjadi di pabrik pembuatan kaus lampu maupun di tempat pembuangan sampah.[158]
Bahaya biologis
[sunting | sunting sumber]Torium tidak berbau dan tidak berasa.[163] Toksisitas kimiawi torium rendah karena torium dan kebanyakan senyawa-senyawa turunannya (seperti dioksida) tidaklah larut dengan baik dalam air.[164] Ia akan mengendap dari larutan sebagai torium hidroksida sebelum masuk ke dalam tubuh.[165] Beberapa senyawa torium memiliki sifat racun yang menengah, terutama apabila terdapat ion pembentuk kompleks yang kuat seperti sitrat yang mampu membawa torium ke dalam tubuh dalam bentuk terlarut.[160] Apabila kaus lampu bertorium terkunyah ataupun terhisap, sekitar 0,4% torium dan 90% anak-anak intinya akan terlepas dari kaus.[115] Tiga per empat torium yang telah masuk ke dalam tubuh akan terakumulasi ke dalam tulang. Penyerapan torium melalui kulit adalah dimungkinkan, tetapi bukanlah jalur paparan yang utama.[157] Kelarutan senyawa torium yang rendah dalam air juga berarti bahwa ekskresi senyawa torium oleh ginjal dan dalam feses berjalan lambat.[160]
Pengujian yang dilakukan terhadap para pekerja pemrosesan monasit menunjukkan bahwa tingkat torium yang terdapat dalam tubuh pekerja melebihi batas rekomendasi. Namun, tiada dampak buruk yang ditemukan dari tingkat paparan menengah rendah tersebut. Sampai sekarang, tidak ditemukan adanya dampak buruk kimiawi terhadap saluran napas dan paru-paru dari paparan torium, walaupun dampak radiologisnya telah diketahui.[165]
Bahaya kimiawi
[sunting | sunting sumber]Debu logam torium bersifat piroforik, yakni ia akan terbakar secara spontan di udara bebas.[5] Titik nyala torium dalam bentuk debu adalah 270 °C (520 °F) sedangkan dalam bentuk lapisan tipis adalah 280 °C (535 °F). Konsentrasi ledak minimum torium adalah 0,075 oz/cu ft (0,075 kg/m3), sedangkan energi ledak minimum untuk debu torium adalah 5 mJ.[166]
Pada tahun 1956, terjadi ledakan di laboratorium Sylvania Electric Products semasa pemrosesan ulang dan pembakaran lumpur torium di kota New York, Amerika Serikat. Sembilan orang terluka; satu di antaranya meninggal karena komplikasi luka bakar derajat tiga.[167][168][169]
Lajur paparan
[sunting | sunting sumber]Torium terdapat di mana-mana di Bumi dalam jumlah kecil, walaupun terdapat pula sejumlah besar torium di bagian tertentu Bumi. Manusia rata-ratanya mengandung 40 mikrogram torium dan umumnya mengonsumsi 3 mikrogram torium setiap hari.[48] Kebanyakan paparan torium terjadi melalui penghirupan debu; beberapa jenis torium juga masuk lewat makanan dan minuman. Karena kelarutannya yang rendah dalam air, paparan lewat makanan dan minuman dapat diabaikan.[160]
Tingkat paparan meningkat bagi orang-orang yang tinggal dekat endapan torium, tempat pembuangan limbah nuklir, pabrik pemrosesan uranium, fosfat, dan timah, dan bagi orang-orang yang bekerja di pabrik kaus lampu bertorium.[170] Torium terutama sangatlah umum ditemukan di daerah pesisir Tamil Nadu di India. Penduduk daerah tersebut terpapar dosis radiasi alami yang 10 kali lipat lebih tinggi daripada dosis radiasi rata-rata dunia.[171]
Lajur paparan lainnya yang dimungkinkan adalah melalui debu torium yang dihasilkan dalam pengujian senjata rudal, karena torium digunakan dalam sistem kendali beberapa jenis rudal. Hal ini disalahkan sebagai sebab tingginya insiden kelainan bawaan dan kanker di Salto di Quirra di pulau Sardinia Italia.[172]
Catatan kaki
[sunting | sunting sumber]- ^ Bismut hanya sedikit radioaktif. Waktu paruhnya yang bernilai 1,9×1019 tahun adalah sangat panjang sedemikiannya peluruhannya dapat diabaikan bahkan dalam jangka waktu geologis.
- ^ Manakala einsteinium telah terukur memiliki kepadatan yang lebih rendah, pengukuran ini dilakukan pada sampel kecil bermassa mikrogram. Kemungkinan besar hasil pengukuran dipengaruhi oleh penghancuran diri kristal logam einsteinium yang disebabkan oleh radioaktivitasnya yang ekstrem.[9]
- ^ Titik didih torium di bawah titik didih osmium, tantalum, wolfram, dan renium;[5] titik didih yang lebih tinggi dispekulasikan ditemukan pada logam-logam transisi 6d. Namun, logam-logam ini belumlah diproduksi dalam jumlah yang cukup besar untuk menguji prediksi ini.[10]
- ^ Sinar gama ditentukan dari asal usulnya yang berasal dari inti atom, bukan dari panjang gelombangnya. Oleh karena itu, tiada batas bawah bagi energi gama yang dihasilkan oleh peluruhan radioaktif.[29]
- ^ a b Sebuah nuklida dapat menjalani fisi (bahkan dengan probabilitas yang kecil) setelah menangkap neutron berenergi tinggi. Beberapa nuklida ini dapat dipancing untuk menjalani fisi dengan neutron termal berenergi rendah dengan probabilitas tinggi; nuklida jenis ini disebut sebagai "fisil". Nuklida yang "fertil" adalah nuklida yang dapat dibombardir neutron untuk menghasilkan produk nuklida fisil. Massa kritis adalah massa sebuah bahan berbentuk bola yang dapat menjalani reaksi rantai nuklir berkelanjutan.
- ^ Nama ionium untuk 230Th adalah nama yang dulunya diberikan sewaktu unsur-unsur berisotop berbeda tidak dikenali sebagai unsur yang sama dan mempunyai nama yang berbeda.
- ^ Tidak seperti kemiripan antara aktinida dan logam transisi, kemiripan antara aktinida dengan unsur golongan utama berakhir di torium, sebelum kemudian berlanjut di paruh kedua deret aktinida. Hal ini karena kontribusi yang meningkat dari orbital 5f terhadap ikatan kovalen. Unsur aktinida uranium masih memiliki sedikit kemiripan dengan unsur golongan utama, yakni keadaan oksidasi umumnya yang berupa uranium(VI) dan uranium (IV). Keduanya berselisih dua dan keadaan oksidasi +6 menandakan hilangnya semua elektron valensi unsur secara formal. Perilaku ini mirip dengan unsur-unsur berat golongan utama pada blok-p.[39]
- ^ Berbagai isotop lainnya juga dapat terbentuk bersama-sama dengan 232Th, tetapi hanya dalam jumlah sekelumit. Apabila tidak terkandung uranium, isotop lain yang hanya dapat ditemukan adalah 228Th, yang berasal dari rantai peluruhan 232Th (deret torium); rasio 228Th terhadap 232Th bernilai di bawah 10−10.[23] Apabila terkandung uranium, sekelumit isotop-isotop lainnya juga dapat ditemukan, yakni 231Th dan 227Th yang berasal dari rantai peluruhan 235U (deret aktinium), dan 234Th dan 230Th yang berasal dari rantai peluruhan 238U (deret uranium).[23] 229Th juga dapat dihasilkan dari rantai peluruhan 237Np (deret neptunium); semua isotop primordial 237Np telah punah, tetapi masih dihasilkan sebagai hasil reaksi nuklir dalam bijih uranium.[78] 229Th kebanyakan diproduksi dari peluruhan 233U buatan yang dibuat dari iradiasi neutron 232Th. 233U sangatlah langka di alam.[23]
- ^ Torianit merujuk pada mineral yang mengandung 75–100 mol% ThO2; uranotorianit, 25–75 mol% ThO2; torian uraninit, 15–25 mol% ThO2; uraninit, 0–15 mol% ThO2.[79]
- ^ Pada saat itu, unsur-unsur tanah jarang, termasuk torium, dianggap sebagai unsur bervalensi dua; sehingganya massa atom unsur tanah jarang pada saat itu bernilai dua per tiga dari massa sebenarnya dan torium dan uranium bernilai setengah dari massa sebenarnya.
- ^ Kesulitan utama isolasi logam torium bukan pada sifat elektropositifnya, melainkan pada asosiasi torium di alam dengan unsur-unsur tanah jarang lainnya dan uranium yang membuatnya sulit dipisahkan satu sama lainnya. Kimiawan Swedia Lars Fredrik Nilson sebelumnya pernah mencoba mengisolasi logam torium pada tahun 1882, tetapi tidak berhasil mendapatkan logam dengan kemurnian yang tinggi.[96] Lely dan Hamburger mendapatkan logam torium 99% murni dengan mereduksi torium klorida dengan logam natrium.[97] Metode yang lebih sederhana dan menghasilkan logam berkemurnian lebih tinggi ditemukan pada tahun 1927 oleh dua insinyur Amerika John Marden dan Harvey Rentschler. Metode ini melibatkan reduksi torium oksida dengan kalsium dan keberadaan kalsium klorida.[97]
- ^ Torium juga muncul pada tabel yang dibuat oleh kimiawan Britania John Newlands pada tahun 1864 sebagai unsur yang terakhir dan terberat. Ini karena awalnya uranium dianggap sebagai unsur bervalensi tiga dengan massa atom sekitar 120; nilai ini adalah setengah kali nilai sebenarnya, karena uranium sebenarnya kebanyakan bervalensi enam. Torium juga muncul sebagai unsur terberat pada tabel tahun 1864 ciptaan kimiawan Britania William Odling, di bawah titanium, zirkonium, dan tantalum. Torium tidak muncul pada tabel periodik tahun 1862 yang diterbikan oleh ahli geologi Prancis Alexandre-Émile Béguyer de Chancourtois, tabel tahun 1867 yang diterbitkan oleh pemusik Jerman-Amerika Gustav Hinrichs, ataupun tabel tahun 1870 yang diterbitkan oleh kimiawan Jerman Julius Lothar Meyer; kesemuaan tabel tersebut juga tidak memasukkan unsur-unsur tanah jarang.[98]
- ^ Pengisian orbital subkelopak 5f yang berawal dari deret aktinida dikonfirmasi pada tahun 1964 ketika ruterfordium pertama kali disintesis dan diamati berperilaku seperti hafnium. Ini sesuai dengan prediksi perilaku unsur yang telah terisi penuh orbital 5f-nya.[110] Pada zaman sekarang, kemiripan torium dengan hafnium kadang-kadang masih diakui dan disebut sebagai "unsur golongan 4 semu".[111]
- ^ Ketigabelas isotop aktinida fisil yang berwaktu paruh lebih dari satu tahun ialah 229Th, 233U, 235U, 236Np, 239Pu, 241Pu, 242mAm, 243Cm, 245Cm, 247Cm, 249Cf, 251Cf, and 252Es. Dari ketigabelas isotop ini, hanya 235U yang terdapat di alam dan hanya 233U dan 239Pu yang dapat dibiakkan dari inti alami melalui penangkapan neutron tunggal.[144]
Referensi
[sunting | sunting sumber]- ^ (Indonesia) "Torium". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ Meija, J.; et al. (2016). "Atomic weights of the elements 2013 (IUPAC Technical Report)". Pure Appl. Chem. 88 (3): 265–91. doi:10.1515/pac-2015-0305.
- ^ Lide, D. R., ed. (2005). "Magnetic susceptibility of the elements and inorganic compounds". CRC Handbook of Chemistry and Physics (PDF) (edisi ke-86). CRC Press. hlm. 4–135. ISBN 978-0-8493-0486-6.
- ^ Weast, R. (1984). CRC, Handbook of Chemistry and Physics. Chemical Rubber Company Publishing. hlm. E110. ISBN 978-0-8493-0464-4.
- ^ a b c d e f g h i j k l m n o Wickleder, Fourest & Dorhout 2006, hlm. 61–63.
- ^ Gale, W. F.; Totemeier, T. C. (2003). Smithells Metals Reference Book (dalam bahasa Inggris). Butterworth-Heinemann. hlm. 15–2–15–3. ISBN 978-0-08-048096-1.
- ^ a b c d e Tretyakov, Yu. D., ed. (2007). Non-organic chemistry in three volumes. Chemistry of transition elements. 3. Academy. ISBN 978-5-7695-2533-9.
- ^ a b c Johansson, B.; Abuja, R.; Eriksson, O.; et al. (1995). "Anomalous fcc crystal structure of thorium metal". Physical Review Letters. 75 (2): 280–283. Bibcode:1995PhRvL..75..280J. doi:10.1103/PhysRevLett.75.280. PMID 10059654.
- ^ Haire, R. G.; Baybarz, R. D. (1979). "Studies of einsteinium metal" (PDF). Le Journal de Physique. 40: C4–101. doi:10.1051/jphyscol:1979431.
- ^ Fricke, Burkhard (1975). Superheavy elements: a prediction of their chemical and physical properties. Recent Impact of Physics on Inorganic Chemistry. Structure and Bonding. 21. hlm. 89–144. doi:10.1007/BFb0116498. ISBN 978-3-540-07109-9. Diakses tanggal 4 October 2013.
- ^ a b c d Audi, G.; Bersillon, O.; Blachot, J.; et al. (2003). "The NUBASE evaluation of nuclear and decay properties" (PDF). Nuclear Physics A. 729 (1): 3–128. Bibcode:2003NuPhA.729....3A. CiteSeerX 10.1.1.692.8504
 . doi:10.1016/j.nuclphysa.2003.11.001. Diarsipkan dari versi asli (PDF) tanggal 24 July 2013.
. doi:10.1016/j.nuclphysa.2003.11.001. Diarsipkan dari versi asli (PDF) tanggal 24 July 2013.
- ^ de Laeter, John Robert; Böhlke, John Karl; De Bièvre, Paul; Hidaka, Hiroshi; Peiser, H. Steffen; Rosman, Kevin J. R.; Taylor, Philip D. P. (2003). "Atomic weights of the elements. Review 2000 (IUPAC Technical Report)". Pure and Applied Chemistry. 75 (6): 683–800. doi:10.1351/pac200375060683
 .
.
- ^ International Union of Pure and Applied Chemistry (2006). "Atomic weights of the elements 2005 (IUPAC Technical Report)" (PDF). Pure and Applied Chemistry. 78 (11): 2051–2066. doi:10.1351/pac200678112051. Diakses tanggal 27 July 2017.
- ^ Nagy, S. (2009). Radiochemistry and Nuclear Chemistry. 2. EOLSS Publications. hlm. 374. ISBN 978-1-84826-127-3.
- ^ Griffin, H. C. (2010). "Natural Radioactive Decay Chains". Dalam Vértes, A.; Nagy, S.; Klencsár, Z.; et al. Handbook of Nuclear Chemistry. Springer Science+Business Media. hlm. 668. ISBN 978-1-4419-0719-6.
- ^ a b c Meija, Juris; et al. (2016). "Atomic weights of the elements 2013 (IUPAC Technical Report)". Pure and Applied Chemistry. 88 (3): 265–91. doi:10.1515/pac-2015-0305
 .
.
- ^ Beiser, A. (2003). "Nuclear Transformations" (PDF). Concepts of Modern Physics (edisi ke-6). McGraw-Hill Education. hlm. 432–434. ISBN 978-0-07-244848-1. Diarsipkan dari versi asli (PDF) tanggal 2016-10-04. Diakses tanggal 2020-06-06.
- ^ "AREVA Med launches production of lead-212 at new facility" (Siaran pers). Areva. 2013. Diakses tanggal 1 January 2017.
- ^ "Mineral Yearbook 2012" (PDF). United States Geological Survey. Diakses tanggal 30 September 2017.
- ^ Ramdahl, Thomas; Bonge-Hansen, Hanne T.; Ryan, Olav B.; Larsen, Åsmund; Herstad, Gunnar; Sandberg, Marcel; Bjerke, Roger M.; Grant, Derek; Brevik, Ellen M. (2016-09-01). "An efficient chelator for complexation of thorium-227". Bioorganic & Medicinal Chemistry Letters. 26 (17): 4318–4321. doi:10.1016/j.bmcl.2016.07.034
 . ISSN 0960-894X. PMID 27476138.
. ISSN 0960-894X. PMID 27476138.
- ^ Deblonde, Gauthier J.-P.; Lohrey, Trevor D.; Booth, Corwin H.; Carter, Korey P.; Parker, Bernard F.; Larsen, Åsmund; Smeets, Roger; Ryan, Olav B.; Cuthbertson, Alan S. (2018-11-19). "Solution Thermodynamics and Kinetics of Metal Complexation with a Hydroxypyridinone Chelator Designed for Thorium-227 Targeted Alpha Therapy". Inorganic Chemistry. 57 (22): 14337–14346. doi:10.1021/acs.inorgchem.8b02430. ISSN 0020-1669. PMID 30372069.
- ^ Captain, Ilya; Deblonde, Gauthier J.-P.; Rupert, Peter B.; An, Dahlia D.; Illy, Marie-Claire; Rostan, Emeline; Ralston, Corie Y.; Strong, Roland K.; Abergel, Rebecca J. (2016-11-21). "Engineered Recognition of Tetravalent Zirconium and Thorium by Chelator–Protein Systems: Toward Flexible Radiotherapy and Imaging Platforms". Inorganic Chemistry. 55 (22): 11930–11936. doi:10.1021/acs.inorgchem.6b02041. ISSN 0020-1669. PMID 27802058.
- ^ a b c d e f g h Wickleder, Fourest & Dorhout 2006, hlm. 53–55.
- ^ Bonetti, R.; Chiesa, C.; Guglielmetti, A.; et al. (1995). "First observation of spontaneous fission and search for cluster decay of 232Th". Physical Review C. 51 (5): 2530–2533. Bibcode:1995PhRvC..51.2530B. doi:10.1103/PhysRevC.51.2530. PMID 9970335.
- ^ Ikezoe, H.; Ikuta, T.; Hamada, S.; et al. (1996). "alpha decay of a new isotope of 209Th". Physical Review C. 54 (4): 2043–2046. Bibcode:1996PhRvC..54.2043I. doi:10.1103/PhysRevC.54.2043. PMID 9971554.
- ^ Ruchowska, E.; Płóciennik, W. A.; Żylicz, J.; et al. (2006). "Nuclear structure of 229Th". Physical Review C. 73 (4): 044326. Bibcode:2006PhRvC..73d4326R. doi:10.1103/PhysRevC.73.044326. hdl:10261/12130.
- ^ Beck, B. R.; Becker, J. A.; Beiersdorfer, P.; et al. (2007). "Energy splitting in the ground state doublet in the nucleus 229Th". Physical Review Letters. 98 (14): 142501. Bibcode:2007PhRvL..98n2501B. doi:10.1103/PhysRevLett.98.142501. PMID 17501268.
- ^ von der Wense, L.; Seiferle, B.; Laatiaoui, M.; et al. (2016). "Direct detection of the 229Th nuclear clock transition". Nature. 533 (7601): 47–51. arXiv:1710.11398
 . Bibcode:2016Natur.533...47V. doi:10.1038/nature17669. PMID 27147026.
. Bibcode:2016Natur.533...47V. doi:10.1038/nature17669. PMID 27147026.
- ^ Feynman, R.; Leighton, R.; Sands, M. (1963). The Feynman Lectures on Physics. 1. Addison-Wesley. hlm. 2–5. ISBN 978-0-201-02116-5. Diakses tanggal 13 January 2018.
- ^ a b c "Evaluation of nuclear criticality safety data and limits for actinides in transport" (PDF). Institut de radioprotection et de sûreté nucléaire. hlm. 15. Diarsipkan dari versi asli (PDF) tanggal 10 July 2007. Diakses tanggal 20 December 2010.
- ^ a b c d e f g h i j k l m n Wickleder, Fourest & Dorhout 2006, hlm. 52–53.
- ^ a b "3–6: Uranium Thorium Dating" (PDF). Institute for Structure and Nuclear Astrophysics, University of Notre Dame. Diarsipkan dari versi asli (PDF) tanggal 2021-04-21. Diakses tanggal 7 October 2017.
- ^ Davis, O. "Uranium-Thorium Dating". Department of Geosciences, University of Arizona. Diarsipkan dari versi asli tanggal 28 March 2017. Diakses tanggal 7 October 2017.
- ^ a b Rafferty, J. P. (2010), Geochronology, Dating, and Precambrian Time: The Beginning of the World As We Know It, The Geologic History of Earth, Rosen Publishing, hlm. 150, ISBN 978-1-61530-125-6
- ^ a b Vértes, A. (2010), Nagy, S.; Klencsár, Z.; Lovas, R. G.; et al., ed., Handbook of Nuclear Chemistry, 5 (edisi ke-2nd), Springer Science+Business Media, hlm. 800, ISBN 978-1-4419-0719-6
- ^ Wickleder, Fourest & Dorhout 2006, hlm. 59–60.
- ^ a b c d Cotton, S. (2006). Lanthanide and Actinide Chemistry. John Wiley & Sons.
- ^ Martin, W. C.; Hagan, L.; Reader, J.; et al. (1974). "Ground Levels and Ionization Potentials for Lanthanide and Actinide Atoms and Ions" (PDF). J. Phys. Chem. Ref. Data. 3 (3): 771–779. Bibcode:1974JPCRD...3..771M. doi:10.1063/1.3253147. Diarsipkan dari versi asli (PDF) tanggal 4 March 2016. Diakses tanggal 19 October 2013.
- ^ a b King, R. Bruce (1995). Inorganic Chemistry of Main Group Elements. Wiley-VCH. ISBN 978-0-471-18602-1.
- ^ Greenwood & Earnshaw 1997, hlm. 1262.
- ^ a b Stoll 2005, hlm. 6.
- ^ a b Hammond, C. R. (2004). The Elements, in Handbook of Chemistry and Physics
 (edisi ke-81st). CRC Press. ISBN 978-0-8493-0485-9.
(edisi ke-81st). CRC Press. ISBN 978-0-8493-0485-9.
- ^ a b Hyde, E. K. (1960). The radiochemistry of thorium (PDF). National Academy of Sciences. Diakses tanggal 29 September 2017.
- ^ Greenwood & Earnshaw 1997, hlm. 1264.
- ^ Moore, Robert Lee; Goodall, C. A.; Hepworth, J. L.; Watts, R. A. (May 1957). "Nitric Acid Dissolution of Thorium. Kinetics of Fluoride-Catalyzed Reaction". Industrial & Engineering Chemistry. 49 (5): 885–887. doi:10.1021/ie50569a035.
- ^ a b Greenwood & Earnshaw 1997, hlm. 1267.
- ^ Yamashita, Toshiyuki; Nitani, Noriko; Tsuji, Toshihide; Inagaki, Hironitsu (1997). "Thermal expansions of NpO2 and some other actinide dioxides". J. Nucl. Mater. 245 (1): 72–78. Bibcode:1997JNuM..245...72Y. doi:10.1016/S0022-3115(96)00750-7.
- ^ a b c d e f Emsley, J. (2011). emsley blocks: an A–Z guide to the elements. Oxford University Press. hlm. 544–548. ISBN 978-0-19-960563-7.
- ^ a b Wickleder, Fourest & Dorhout 2006, hlm. 70–77.
- ^ Greenwood & Earnshaw 1997, hlm. 1269.
- ^ a b c Ivey, H. F. (1974). "Candoluminescence and radical-excited luminescence". Journal of Luminescence. 8 (4): 271–307. Bibcode:1974JLum....8..271I. doi:10.1016/0022-2313(74)90001-5.
- ^ Wickleder, Fourest & Dorhout 2006, hlm. 95–97.
- ^ a b c d e Wickleder, Fourest & Dorhout 2006, hlm. 78–94.
- ^ a b Greenwood & Earnshaw 1997, hlm. 1271.
- ^ Wickleder, Fourest & Dorhout 2006, hlm. 97–101.
- ^ Wickleder, Fourest & Dorhout 2006, hlm. 64–66.
- ^ Greenwood & Earnshaw 1997, hlm. 127.
- ^ a b c d Wickleder, Fourest & Dorhout 2006, hlm. 117–134.
- ^ Persson, I. (2010). "Hydrated metal ions in aqueous solution: How regular are their structures?". Pure and Applied Chemistry. 82 (10): 1901–1917. doi:10.1351/PAC-CON-09-10-22
 .
.
- ^ a b Greenwood & Earnshaw 1997, hlm. 1275–1277.
- ^ a b Wickleder, Fourest & Dorhout 2006, hlm. 101–115.
- ^ a b c d Wickleder, Fourest & Dorhout 2006, hlm. 116–117.
- ^ a b Greenwood & Earnshaw 1997, hlm. 1278–1280.
- ^ Langeslay, Ryan R.; Fieser, Megan E.; Ziller, Joseph W.; Furche, Philip; Evans, William J. (2015). "Synthesis, structure, and reactivity of crystalline molecular complexes of the {[C5H3(SiMe3)2]3Th}1− anion containing thorium in the formal +2 oxidation state". Chemical Science. 6 (6): 517–521. doi:10.1039/C4SC03033H. PMC 5811171
 . PMID 29560172.
. PMID 29560172.
- ^ a b c Cameron, A. G. W. (1973). "Abundance of the Elements in the Solar System" (PDF). Space Science Reviews. 15 (1): 121–146. Bibcode:1973SSRv...15..121C. doi:10.1007/BF00172440. Diarsipkan dari versi asli (PDF) tanggal 21 October 2011.
- ^ Frebel, Anna; Beers, Timothy C. (2018). "The formation of the heaviest elements". Physics Today. 71 (1): 30–37. arXiv:1801.01190
 . Bibcode:2018PhT....71a..30F. doi:10.1063/pt.3.3815. ISSN 0031-9228.
. Bibcode:2018PhT....71a..30F. doi:10.1063/pt.3.3815. ISSN 0031-9228.
- ^ a b Roederer, I. U.; Kratz, K.-L.; Frebel, A.; et al. (2009). "The End of Nucleosynthesis: Production of Lead and Thorium in the Early Galaxy". The Astrophysical Journal. 698 (2): 1963–1980. arXiv:0904.3105
 . Bibcode:2009ApJ...698.1963R. doi:10.1088/0004-637X/698/2/1963.
. Bibcode:2009ApJ...698.1963R. doi:10.1088/0004-637X/698/2/1963.
- ^ Burbidge, E. M.; Burbidge, G. R.; Fowler, W. A.; et al. (1957). "Synthesis of the Elements in Stars" (PDF). Reviews of Modern Physics. 29 (4): 547. Bibcode:1957RvMP...29..547B. doi:10.1103/RevModPhys.29.547. Diarsipkan dari versi asli (PDF) tanggal 2016-06-24. Diakses tanggal 2020-06-09.
- ^ Clayton, D. D. (1968). Principles of Stellar Evolution and Nucleosynthesis
 . McGraw-Hill Education. hlm. 577–591. ISBN 978-0-226-10953-4.
. McGraw-Hill Education. hlm. 577–591. ISBN 978-0-226-10953-4.
- ^ Stoll 2005, hlm. 2.
- ^ Greenwood & Earnshaw 1997, hlm. 1294.
- ^ Albarède, F. (2003). Geochemistry: an introduction. Cambridge University Press. hlm. 17. ISBN 978-0-521-89148-6.
- ^ Trenn, T. J. (1978). "Thoruranium (U-236) as the extinct natural parent of thorium: The premature falsification of an essentially correct theory". Annals of Science. 35 (6): 581–597. doi:10.1080/00033797800200441.
- ^ Diamond, H.; Friedman, A. M.; Gindler, J. E.; et al. (1956). "Possible Existence of Cm247 or Its Daughters in Nature". Physical Review. 105 (2): 679–680. Bibcode:1957PhRv..105..679D. doi:10.1103/PhysRev.105.679.
- ^ Rao, M. N.; Gopalan, K. (1973). "Curium-248 in the Early Solar System". Nature. 245 (5424): 304–307. Bibcode:1973Natur.245..304R. doi:10.1038/245304a0.
- ^ Rosenblatt, D. B. (1953). "Effects of a Primeval Endowment of U236". Physical Review. 91 (6): 1474–1475. Bibcode:1953PhRv...91.1474R. doi:10.1103/PhysRev.91.1474.
- ^ Gando, A.; Gando, Y.; Ichimura, K.; et al. (2011). "Partial radiogenic heat model for Earth revealed by geoneutrino measurements" (PDF). Nature Geoscience. 4 (9): 647–651. Bibcode:2011NatGe...4..647K. doi:10.1038/ngeo1205.
- ^ Peppard, D. F.; Mason, G. W.; Gray, P. R.; et al. (1952). "Occurrence of the (4n + 1) Series in Nature". Journal of the American Chemical Society. 74 (23): 6081–6084. doi:10.1021/ja01143a074.
- ^ a b c d e f g h i Wickleder, Fourest & Dorhout 2006, hlm. 55–56.
- ^ Agency for Toxic Substances and Disease Registry (2016). Thorium (PDF) (Laporan). Diakses tanggal 30 September 2017.
- ^ Woodhead, J. A. (1991). "The metamictization of zircon: Radiation dose-dependent structural characteristics" (PDF). American Mineralogist. 76: 74–82.
- ^ Szymański, J. T. (1982). "A mineralogical study and crystal-structure determination of nonmetamict ekanite, ThCa2Si8O20" (PDF). Canadian Mineralogist. 20: 65–75.
- ^ Greenwood & Earnshaw 1997, hlm. 1255.
- ^ "Tor's Fight with the Giants" (dalam bahasa Inggris). Google Arts & Culture. Diakses tanggal 26 June 2016.
- ^ a b Fontani, M.; Costa, M.; Orna, V. (2014). The Lost Elements: The Periodic Table's Shadow Side. Oxford University Press. hlm. 73. ISBN 978-0-19-938334-4.
- ^ Ryabchikov, D. I.; Gol'braikh, E. K. (2013). The Analytical Chemistry of Thorium: International Series of Monographs on Analytical Chemistry. Elsevier. hlm. 1. ISBN 978-1-4831-5659-0.
- ^ Thomson, T. (1831). A System of Chemistry of Inorganic Bodies. 1. Baldwin & Cradock and William Blackwood. hlm. 475.
- ^ Berzelius, J. J. (1824). "Undersökning af några Mineralier. 1. Phosphorsyrad Ytterjord" [Examining some minerals. 1st phosphoric yttria.]. Kungliga Svenska Vetenskapsakademiens Handlingar (dalam bahasa Swedia). 2: 334–338.
- ^ "Xenotime-(Y)". Mindat database. Diakses tanggal 7 October 2017.
- ^ Selbekk, R. S. (2007). "Morten Thrane Esmark". Store norske leksikon (dalam bahasa Norwegia). Kunnskapsforlaget. Diakses tanggal 16 May 2009.
- ^ a b Weeks, M. E. (1932). "The discovery of the elements. XI. Some elements isolated with the aid of potassium and sodium: Zirconium, titanium, cerium, and thorium". Journal of Chemical Education. 9 (7): 1231. Bibcode:1932JChEd...9.1231W. doi:10.1021/ed009p1231.
- ^ Berzelius, J. J. (1829). "Untersuchung eines neues Minerals und einer darin erhalten zuvor unbekannten Erde" [Investigasi suatu mineral baru beserta oksida tak diketahui yang terkandung di dalamnya]. Annalen der Physik und Chemie (dalam bahasa Jerman). 16 (7): 385–415. Bibcode:1829AnP....92..385B. doi:10.1002/andp.18290920702. (modern citation: Annalen der Physik, vol. 92, no. 7, pp. 385–415).
- ^ Berzelius, J. J. (1829). "Undersökning af ett nytt mineral (Thorit), som innehåller en förut obekant jord" [Investigasi suatu mineral baru (torit) yang terkandung dalam oksida yang sebelumnya tak diketahui]. Kungliga Svenska Vetenskaps Akademiens Handlingar (dalam bahasa Swedia): 1–30.
- ^ Schilling, J. (1902). "Die eigentlichen Thorit-Mineralien (Thorit und Orangit)" [The actual thoritic minerals (thorite and orangite)]. Zeitschrift für Angewandte Chemie (dalam bahasa Jerman). 15 (37): 921–929. doi:10.1002/ange.19020153703.
- ^ Leach, M. R. "The Internet Database of Periodic Tables: Berzelius' Electronegativity Table". Diakses tanggal 16 July 2016.
- ^ Nilson, L. F. (1882). "Über metallisches Thorium" [About metallic thorium]. Berichte der Deutschen Chemischen Gesellschaft (dalam bahasa Jerman). 15 (2): 2537–2547. doi:10.1002/cber.188201502213.
- ^ a b Meister, G. (1948). Production of Rarer Metals (PDF) (Laporan). United States Atomic Energy Commission. Diakses tanggal 22 September 2017.
- ^ a b c d Leach, M. R. "The Internet Database of Periodic Tables". Diakses tanggal 14 May 2012.
- ^ Jensen, William B. (2003). "The Place of Zinc, Cadmium, and Mercury in the Periodic Table" (PDF). Journal of Chemical Education. 80 (8): 952–961. Bibcode:2003JChEd..80..952J. doi:10.1021/ed080p952. Diarsipkan dari versi asli (PDF) tanggal 11 June 2010.
- ^ a b Masterton, W. L.; Hurley, C. N.; Neth, E. J. (2011). Chemistry: Principles and reactions (edisi ke-7th). Cengage Learning. hlm. 173. ISBN 978-1-111-42710-8.
- ^ Curie, M. (1898). "Rayons émis par les composés de l'uranium et du thorium" [Sinar yang dipancarkan senyawa-senyawa uranium dan torium]. Comptes Rendus (dalam bahasa Prancis). 126: 1101–1103. OL 24166254M.
- ^ Schmidt, G. C. (1898). "Über die vom Thorium und den Thoriumverbindungen ausgehende Strahlung" [Tentang radiasi yang dipancarkan oleh torium dan senyawa-senyawa torium]. Verhandlungen der Physikalischen Gesellschaft zu Berlin (Proceedings of the Physical Society in Berlin) (dalam bahasa Jerman). 17: 14–16.
- ^ Schmidt, G. C. (1898). "Über die von den Thorverbindungen und einigen anderen Substanzen ausgehende Strahlung" [Tentang radiasi yang dipancarkan oleh senyawa torium dan beberapa senyawa lainnya]. Annalen der Physik und Chemie (dalam bahasa Jerman). 65 (5): 141–151. Bibcode:1898AnP...301..141S. doi:10.1002/andp.18983010512. (modern citation: Annalen der Physik, vol. 301, pp. 141–151 (1898)).
- ^ Rutherford, E.; Owens, R. B. (1899). "Thorium and uranium radiation". Trans. R. Soc. Can. 2: 9–12.: "The radiation from thorium oxide was not constant, but varied in a most capricious manner", whereas "All the compounds of Uranium give out a radiation which is remarkably constant."
- ^ Simmons, J. G. (1996). The Scientific 100: A Ranking of the Most Influential Scientists, Past and Present
 . Carol. hlm. 19. ISBN 978-0-8065-2139-8.
. Carol. hlm. 19. ISBN 978-0-8065-2139-8.
- ^ Fröman, N. (1996). "Marie and Pierre Curie and the Discovery of Polonium and Radium". nobelprize.org. Nobel Media AB. Diakses tanggal 11 May 2017.
- ^ a b Burns, M. (1987). Low-Level Radioactive Waste Regulation-Science, Politics and Fear. CRC Press. hlm. 24–25. ISBN 978-0-87371-026-8.
- ^ van Spronsen, J. W. (1969). The periodic system of chemical elements. Elsevier. hlm. 315–316. ISBN 978-0-444-40776-4..
- ^ Rhodes, R. (2012). The Making of the Atomic Bomb (edisi ke-25th Anniversary). Simon & Schuster. hlm. 221–222, 349. ISBN 978-1-4516-7761-4.
- ^ Türler, A.; Buklanov, G. V.; Eichler, B.; et al. (1998). "Evidence for relativistic effects in the chemistry of element 104". Journal of Alloys and Compounds. 271–273: 287. doi:10.1016/S0925-8388(98)00072-3.
- ^ Kratz, J. V.; Nagame, Y. (2014). "Liquid-Phase Chemistry of Superheavy Elements". Dalam Schädel, M.; Shaughnessy, D. The Chemistry of Superheavy Elements (edisi ke-2nd). Springer-Verlag. hlm. 335. doi:10.1007/978-3-642-37466-1. ISBN 978-3-642-37465-4.
- ^ a b c d Furuta, E.; Yoshizawa, Y.; Aburai, T. (2000). "Comparisons between radioactive and non-radioactive gas lantern mantles". J. Radiol. Prot. 20 (4): 423–431. Bibcode:2000JRP....20..423F. doi:10.1088/0952-4746/20/4/305. PMID 11140713.
- ^ New Jersey Department of Health (1996). "Health and hazardous waste" (PDF). A Practitioner's Guide to Patients' Environmental Exposures. 1 (3): 1–8. Diarsipkan dari versi asli (PDF) tanggal 15 April 2016.
- ^ Toepker, Terrence P. (1996). "Thorium and yttrium in gas lantern mantles". American Journal of Physics. 64 (2): 109. Bibcode:1996AmJPh..64..109T. doi:10.1119/1.18463.
- ^ a b Poljanc, K.; Steinhauser, G.; Sterba, J. H.; et al. (2007). "Beyond low-level activity: on a "non-radioactive" gas mantle". Science of the Total Environment. 374 (1): 36–42. Bibcode:2007ScTEn.374...36P. doi:10.1016/j.scitotenv.2006.11.024. PMID 17270253.
- ^ Kazimi, M. (2003). "Thorium Fuel for Nuclear Energy". American Scientist. Diarsipkan dari versi asli tanggal 1 January 2017. Diakses tanggal 29 September 2017.
- ^ Majumdar, S.; Purushotham, D. S. C. (1999). "Experience of thorium fuel development in India". Thorium fuel utilization: Options and trends (PDF) (Laporan). International Atomic Energy Agency. Diakses tanggal 7 October 2017.
- ^ "Nuclear Power in India". World Nuclear Association. 2017. Diakses tanggal 29 September 2017.
- ^ "IAEA-TECDOC-1450 Thorium Fuel Cycle – Potential Benefits and Challenges" (PDF). International Atomic Energy Agency. 2005. Diakses tanggal 23 March 2009.
- ^ "IAEA-TECDOC-1349 Potential of thorium-based fuel cycles to constrain plutonium and to reduce the long-lived waste toxicity" (PDF). International Atomic Energy Agency. 2002. Diakses tanggal 24 March 2009.
- ^ Evans, B. (2006). "Scientist urges switch to thorium". ABC News. Diarsipkan dari versi asli tanggal 28 March 2010. Diakses tanggal 17 September 2011.
- ^ Martin, R. (2009). "Uranium is So Last Century – Enter Thorium, the New Green Nuke". Wired. Diakses tanggal 19 June 2010.
- ^ "Thorium-based nuclear power", Wikipedia (dalam bahasa Inggris), 2020-01-16, diakses tanggal 2020-01-30
- ^ Weinberg, Alvin (1994). The First Nuclear Era: The Life and Times of a Technological Fixer. New York: AIP Press. hlm. 36–38. ISBN 978-1-56396-358-2.
- ^ a b c "Thorium". World Nuclear Association. 2017. Diakses tanggal 21 June 2017.
- ^ Woods, W. K. (1966). LRL Interest in U-233 (PDF) (Laporan) (dalam bahasa English). Battelle Memorial Institute. doi:10.2172/79078. OSTI 79078.
- ^ "Classification Bulletin WNP-118" (PDF). U.S. Department of Energy. March 12, 2008.
- ^ Stoll 2005, hlm. 7.
- ^ United States Geological Survey (2012). "Thorium" (PDF). Diakses tanggal 12 May 2017.
- ^ Jayaram, K. M. V. (1987). An Overview of World Thorium Resources, Incentives for Further Exploration and Forecast for Thorium Requirements in the Near Future (PDF) (Laporan). Department of Atomic Energy. Diarsipkan dari versi asli (PDF) tanggal 28 June 2011.
- ^ Thorium. Statistics and Information (Laporan) (dalam bahasa Inggris). United States Geological Survey. 2017. Diakses tanggal 6 January 2018.
- ^ a b c d e f g h i j Stoll 2005, hlm. 8.
- ^ Crouse, David J.; Brown, Keith B. (1959-12-01). "The Amex Process for Extracting Thorium Ores with Alkyl Amines". Industrial & Engineering Chemistry. 51 (12): 1461–1464. doi:10.1021/ie50600a030. ISSN 0019-7866.
- ^ a b c d e Stoll 2005, hlm. 32.
- ^ Stoll 2005, hlm. 31.
- ^ Matson, Tim (2011). The Book of Non-electric Lighting: The Classic Guide to the Safe Use of Candles, Fuel Lamps, Lanterns, Gaslights & Fire-View Stoves. Countryman Press. hlm. 60. ISBN 978-1-58157-829-4.
- ^ Pridham, G. J. (2016). Electronic Devices and Circuits: The Commonwealth and International Library: Electrical Engineering Division (dalam bahasa Inggris). Elsevier. hlm. 105. ISBN 978-1-4831-3979-1.
- ^ Uttrachi, J. (2015). Weld Like a Pro: Beginning to Advanced Techniques. CarTech Inc. hlm. 42. ISBN 978-1-61325-221-5.
- ^ Jeffus, L. (2016). Welding: Principles and Applications. Cengage Learning. hlm. 393. ISBN 978-1-305-49469-5.
- ^ Oak Ridge Associated Universities (1999). "Thoriated Camera Lens (ca. 1970s)". Diakses tanggal 29 September 2017.
- ^ Rancourt, J. D. (1996). Optical thin films: user handbook. SPIE Press. hlm. 196. ISBN 978-0-8194-2285-9.
- ^ Kaiser, N.; Pulker, H. K. (2013). Optical Interference Coatings (dalam bahasa Inggris). Springer. hlm. 111. ISBN 978-3-540-36386-6.
- ^ Ronen, Y. (2006). "A rule for determining fissile isotopes". Nuclear Science and Engineering. 152 (3): 334–335. doi:10.13182/nse06-a2588. ISSN 0029-5639.
- ^ a b Ronen, Y. (2010). "Some remarks on the fissile isotopes". Annals of Nuclear Energy. 37 (12): 1783–1784. doi:10.1016/j.anucene.2010.07.006.
- ^ "Plutonium". World Nuclear Association. 2017. Diakses tanggal 29 September 2017.
- ^ a b c Greenwood & Earnshaw 1997, hlm. 1259.
- ^ "Interactive Chart of Nuclides". Brookhaven National Laboratory. Diarsipkan dari versi asli tanggal 2017-01-24. Diakses tanggal 12 August 2013.
- ^ "Thorium test begins". World Nuclear News. 2013. Diakses tanggal 21 July 2013.
- ^ "IAEA-TECDOC-1450 Thorium Fuel Cycle – Potential Benefits and Challenges" (PDF). International Atomic Energy Agency. 2005. Diakses tanggal 23 March 2009.
- ^ a b Langford, R. E. (2004). Introduction to Weapons of Mass Destruction: Radiological, Chemical, and Biological. John Wiley & Sons. hlm. 85. ISBN 978-0-471-46560-7.
- ^ Stoll 2005, hlm. 30.
- ^ Nakajima, Ts.; Groult, H. (2005). Fluorinated Materials for Energy Conversion. Elsevier. hlm. 562–565. ISBN 978-0-08-044472-7.
- ^ Rees, E. (2011). "Don't believe the spin on thorium being a greener nuclear option". The Guardian. Diakses tanggal 29 September 2017.
- ^ Sovacool, B. K.; Valentine, S. V. (2012). The National Politics of Nuclear Power: Economics, Security, and Governance. Routledge. hlm. 226. ISBN 978-1-136-29437-2.
- ^ "Nuclear Energy FAQs" (PDF). Argonne National Laboratory. 2014. Diakses tanggal 13 January 2018.
- ^ Findlay, T. (2011). Nuclear Energy and Global Governance: Ensuring Safety, Security and Non-proliferation. Routledge. hlm. 9. ISBN 978-1-136-84993-0.
- ^ a b c "Thorium: Radiation Protection". United States Environmental Protection Agency. Diarsipkan dari versi asli tanggal 1 October 2006. Diakses tanggal 27 February 2016.
- ^ a b "Radioactivity in Lantern Mantles". Australian Radiation Protection and Nuclear Safety Agency. Diarsipkan dari versi asli tanggal 14 October 2007. Diakses tanggal 29 September 2017.
- ^ "Natural Decay Series: Uranium, Radium, and Thorium" (PDF). Argonne National Laboratory. 2005. Diarsipkan dari versi asli (PDF) tanggal 17 August 2016. Diakses tanggal 30 September 2017.
- ^ a b c d Stoll 2005, hlm. 35.
- ^ Luetzelschwab, J. W.; Googins, S. W. (1984). "Radioactivity released from burning gas lantern mantles". Health Phys. 46 (4): 873–881. doi:10.1097/00004032-198404000-00013. PMID 6706595.
- ^ Huyskens, C. J.; Hemelaar, J. T.; Kicken, P. J. (1985). "Dose estimates for exposure to radioactivity in gas mantles". Sci. Total Environ. 45: 157–164. Bibcode:1985ScTEn..45..157H. doi:10.1016/0048-9697(85)90216-5. PMID 4081711.
- ^ "Toxicological Profile for Thorium" (PDF). Agency for Toxic Substances and Disease Registry U.S. Public Health Service. 1990. hlm. 4.
- ^ Merkel, B.; Dudel, G.; et al. (1988). Untersuchungen zur radiologischen Emission des Uran-Tailings Schneckenstein (PDF) (Laporan) (dalam bahasa Jerman). Sächsisches Staatsministerium für Umwelt und Landesentwicklung. Diarsipkan dari versi asli (PDF) tanggal 8 January 2013.
- ^ a b Stoll 2005, hlm. 34.
- ^ Jacobson, M.; Cooper, A. R.; Nagy, J. (1964). Explosibility of metal powders (PDF) (Laporan). United States Department of the Interior. Diarsipkan dari versi asli (PDF) tanggal 2017-03-05. Diakses tanggal 29 September 2017.
- ^ "Nine Injured In Atomic Lab Blasts". Pittsburgh Post-Gazette. Associated Press. 1956. hlm. 2. Diakses tanggal 29 September 2017.
- ^ "No Radiation Threat Seen In A-laboratory Blast". St. Petersburg Times. Associated Press. 1956. hlm. 2. Diakses tanggal 29 September 2017.
- ^ Harrington, M. (2003). "Sad Memories of '56 Sylvania Explosion". New York Newsday. Diarsipkan dari versi asli tanggal 4 February 2012. Diakses tanggal 29 September 2017.
- ^ "Thorium ToxFAQs" (PDF). Agency for Toxic Substances and Disease Registry. Diakses tanggal 29 September 2017.
- ^ "Compendium Of Policy And Statutory Provisions Relating To Exploitation Of Beach Sand Minerals". Department of Atomic Energy. Diarsipkan dari versi asli tanggal 4 December 2008. Diakses tanggal 19 December 2008.
- ^ Alberici, Emma (29 January 2019). "Italian military officials' trial ignites suspicions of links between weapon testing and birth defects in Sardinia". ABC News. Australian Broadcasting Corporation. Diakses tanggal 29 January 2019.
Daftar pustaka
[sunting | sunting sumber]- Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements (edisi ke-2nd). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- Stoll, W. (2005). "Thorium and Thorium Compounds". Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. doi:10.1002/14356007.a27_001. ISBN 978-3-527-31097-5.
- Wickleder, M. S.; Fourest, B.; Dorhout, P. K. (2006). "Thorium". Dalam Morss, L. R.; Edelstein, N. M.; Fuger, J. The Chemistry of the Actinide and Transactinide Elements (PDF). 3 (edisi ke-3rd). Springer-Verlag. hlm. 52–160. doi:10.1007/1-4020-3598-5_3. ISBN 978-1-4020-3598-2. Diarsipkan dari versi asli (PDF) tanggal 14 December 2017.
- https://en.wikipedia.org/wiki/Thorium
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||


