Acide caféique
| Acide caféique | |
| |
| Identification | |
|---|---|
| Nom UICPA | acide (E) 3-(3,4-dihydroxyphényl)prop-2-ènoïque |
| Synonymes |
acide 3,4-dihydroxycinnamique |
| No CAS | |
| No ECHA | 100.005.784 |
| No CE | 206-361-2 |
| DrugBank | DB01880 |
| PubChem | 689043 |
| ChEBI | 17395 |
| SMILES | |
| InChI | |
| Apparence | poudre cristalline jaune |
| Propriétés chimiques | |
| Formule | C9H8O4 [Isomères] |
| Masse molaire[2] | 180,157 4 ± 0,009 g/mol C 60 %, H 4,48 %, O 35,52 %, |
| pKa | 4.62[1] |
| Propriétés physiques | |
| T° fusion | 234 à 237 °C (décomposition)[3] |
| Solubilité | peu soluble dans l'eau[3] |
| Masse volumique | 1,478 g·cm-3 |
| Précautions | |
| Directive 67/548/EEC | |
| Écotoxicologie | |
| DL50 | > 721 mg·kg-1 (souris, i.p.)[4] |
| LogP | 1,15[1] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
L'acide caféique ou acide (E) 3-(3,4-dihydroxyphényl)prop-2-ènoïque est un composé organique naturellement présent dans toutes les plantes car c'est un intermédiaire clé dans la biosynthèse de la lignine. C'est un dérivé de l'acide cinnamique qui a une structure très proche de l'acide férulique et, comme lui, il appartient aux grandes familles des phénylpropanoïdes et des acides-phénols.
Il n'a aucun lien avec la caféine, mais est présent naturellement en petite quantité dans le café à l'état libre et en très grande quantité à l'état estérifié.
Histoire
[modifier | modifier le code]Le chimiste allemand Runge (1795-1867), extrait du café un composé acide à l'aide d'eau chaude. Pfaff trouva dans le précipité à l'acétate plombique de Runge, une espèce particulière de tanin et un acide qu'il nomma "acide caféique".
Structure
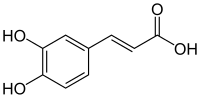
[modifier | modifier le code]L'acide caféique a une structure très proche de l'acide cinnamique dont il dérive. Comme lui il présente un groupe acrylique en bout de chaîne, mais s'en différencie par la présence de deux groupes hydroxy sur le phényle qui lui donne des propriétés propres aux polyphénols.
Répartition chez les plantes
[modifier | modifier le code]| Plantes alimentaires riches en acide caféique d'après Phenol Explorer[5] | ||
| Forme consommée | Nom scientifique de la plante | Teneur |
|---|---|---|
| Sauge officinale, séchée | Salvia officinalis | 26,4 mg/100g |
| Menthe douce, séchée | Mentha spicata | 25,00 mg/100g |
| Cannelle de Ceylan | Cinnamomum verum | 24,20 mg/100g |
| Thym commun, sec | Thymus vulgaris | 21,28 mg/100g |
| Airelle rouge | Vaccinium vitis-idaea | 6,34 mg/100g |
| Pruneau, jus à partir de concentré | Prunus domestica | 5,10 mg/100g |
| Endive, crue | Cichorium intybus L. var foliosum | 2,61 mg/100g |
| Datte, séchée | Phoenix dactylifera | 2,52 mg/100g |
| Olive noire, crue | Olea europaea | 2,10 mg/100g |
| Pomme de terre, crue | Solanum tuberosum | 1,62 mg/100g |
| Pomme, compote | Malus pumila | 1,14 mg/100g |
| Abricot | Prunus armeniaca | 0,66 mg/100g |
| Vin rouge | Vitis vinifera | 1,88 mg/100ml |
| Boisson de café, filtre | Coffea sp | 0,03 mg/100ml |
L'acide caféique et son dérivé, l'ester caféate de phénéthyle (caffeic acid phenetyl ester - CAPE, ester de l'acide caféique et du 2-phényléthanol), sont présents dans presque toutes les plantes[6],[7] et en particulier en grande quantité dans les grains de café, d'où il fut isolé pour la première fois au XIXe siècle et dont il tire son nom. En général, il est présent sous forme estérifiée[8], principalement avec l'acide quinique avec lequel il forme l'acide chlorogénique. On rencontre ce dernier particulièrement dans le café mais aussi dans la pomme. Parmi les autres formes estérifées courantes, on trouve l'acide caféoyltartrique (ou acide caftarique) formé avec l'acide tartrique présent dans le raisin, l'acide caféoylshikimique (formé avec l'acide shikimique) naturellement présent dans la datte, l'acide caféoylmalique (formé avec l'acide malique) naturellement présent dans le radis, ou encore estérifiée avec du glucose (caféoylglucose) ou sous forme d'amide avec la putrescine (caféoylputrescine).
Absorption
[modifier | modifier le code]L'acide caféique est extrêmement bien absorbé au niveau de l'intestin. Les mesures[9] ont été faites sur des patients ayant une iléostomie, dont les matières peuvent être récupérées avant l'entrée dans le côlon. Après avoir consommé 2,8 mmol d'acide caféique, seulement 5 % était retrouvé dans la poche, c'est-à-dire que 95 % était absorbé dans l'intestin grêle. On retrouve ensuite 11 % de cet acide caféique dans les urines. Une partie est méthylée dans le foie et une partie accessoire subit une glucuronidation et une sulfatation[10].
Biosynthèse
[modifier | modifier le code]Il est biosynthétisé par hydroxylation de l'acide paracoumarique (sous forme ester), lui-même obtenu par hydroxylation de l'acide cinnamique (éventuellement aussi obtenu via l'élimination du groupe amine de la tyrosine). C'est un précurseur de l'acide férulique, de l'alcool coniférylique et de l'alcool sinapylique, monomères de la lignine et de la lignane[11]. La transformation de l'acide caféique en acide férulique est catalysée par une enzyme spécifique l'acide caféique-O-méthyltransférase.

Dans les plantes, l'acide caféique (milieu) est formé par hydroxylation de l'acide paracoumarique (gauche) et transformé en acide férulique (droite).
Activités pharmacologiques
[modifier | modifier le code]- Activité antioxydante
L'acide caféique, comme tous les polyphénols, possèdent des groupes hydroxyles phénoliques -OH, capables de prévenir ou ralentir l'oxydation des lipides. Dans une étude comparative avec l'acide chlorogénique, l'effet de ces deux acides sur l'autoxydation du triacylglycérol a été étudié[12]. Il a été trouvé qu'à la concentration de 2,8 10-4 M, ces deux acides avaient pratiquement la même activité mais qu'à des concentrations plus élevées, l'acide caféique était plus efficace.
L'acide caféique, au même titre que le Trolox (une vitamine E hydrosoluble), est capable de protéger les cellules contre les dommages provoqués par les radicaux libres[13]. En présence de radicaux de monoxyde d'azote •NO, les cellules épithéliales (d'ouies de truites) meurent sauf si elles sont protégées par l'acide caféique ou le Trolox. Il a été montré in vitro que le traitement par l'acide caféique inhibe la voie de l'apoptose induite par •NO.[réf. nécessaire]
- Activité anti-inflammatoire, antimutagène[réf. nécessaire]
Application
[modifier | modifier le code]Kraft Foods a breveté en 1993 l'utilisation de l'acide caféique et de ses sels (de 0,001 % à 0,2 %) comme masqueur de l'arrière goût amer d'édulcorant artificiels tels que l'acésulfame potassium et la saccharine[14].
Notes et références
[modifier | modifier le code]- (en) « Acide caféique », sur ChemIDplus
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (de) Fiche Merck
- Yakugaku Zasshi. Journal of Pharmacy. Vol. 104, Pg. 793, 1984.
- Phenol Explorer INRA
- (en) Red Clover Flowers Herbal Information
- (en) « Dr. Duke's Phytochemical and Ethnobotanical Databases »
- Par sa fonction acide, avec les fonctions hydroxyle d'autres composés, y compris d'autres acides, hydroxylés
- Olthof MR, Hollman PC, Katan MB., « Chlorogenic Acid and Caffeic Acid are absorbed in humans », The Journal of Nurition, vol. 131, no 1, , p. 66-71
- Mateos R, Goya L, Bravo L., « Uptake and metabolism of hydroxycinnamic acids (chlorogenic, caffeic, and ferulic acids) by HepG2 cells as a model of the human liver. », J Agric Food Chem., vol. 54, no 23, , p. 8724-32
- Wout Boerjan, John Ralph, Marie Baucher Annual Reviews Plant Biology 2003, volume 54, 519–46. DOI 10.1146/annurev.arplant.54.031902.134938.
- Emma M.Marinova,A. Toneva, N. Yanishlieva, « Comparison of the antioxidative properties of caffeic and chlorogenic acids », Food Chemistry, vol. 114, , p. 1498-1502
- Chung MJ, Walker PA, Hogstrand C, « Dietary phenolic antioxidants, caffeic acid and Trolox, protect rainbow trout gill cells from nitric oxide-induced apoptosis », Aquatic Toxicology, vol. 80, , p. 321-328
- (en) JA Riemer. United States Patent 5,336,513

