Fosfora trifluorido
Etoso
| Fosfora trifluorido | ||||
 | ||||
| Plata kemia strukturo de la Fosfora trifluorido | ||||
 | ||||
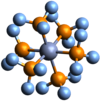
| Tridimensia kemia strukturo de la Fosfora trifluorido | ||||
| Alternativa(j) nomo(j) | ||||
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 7783-55-3 | |||
| ChemSpider kodo | 56416 | |||
| PubChem-kodo | 62665 | |||
| Merck Index | 15,7471 | |||
| Fizikaj proprecoj | ||||
| Aspekto | senkolora senodora volatila gaso | |||
| Molmaso | 87,969 g·mol−1 | |||
| Denseco | 3,907g cm−3 | |||
| Fandpunkto | -151,5 °C[1] | |||
| Bolpunkto | -101,8 °C | |||
| Solvebleco | Akvo:reakcias | |||
| Mortiga dozo (LD50) | 18 mg/kg (buŝe) | |||
| Sekurecaj Indikoj | ||||
| Riskoj | R14 R26/28 R35 R48/20 | |||
| Sekureco | S7/8 S26 S36/37/39 S45 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS Damaĝo Piktogramo |
| |||
| GHS Signalvorto | Damaĝa substanco | |||
| GHS Deklaroj pri damaĝoj | H280, H314, H330, H331 | |||
| GHS Deklaroj pri antaŭgardoj | P260, P261, P264, P271, P280, P284, P301+330+331, P303+361+353, P304+340, P305+351+338, P310, P311, P320, P321, P363, P403+233, P405, P410+403, P501[2] | |||
(25 °C kaj 100 kPa) | ||||
Fosfora trifluorido aŭ PF3 estas neorganika kombinaĵo de fosforo kaj fluoro, senkolora, senodora, volatila, kaj alte toksa gaso kiu reakcias kun la akvo. ��ia ĉefa uzo estas kiel liganto em metalkompleksaĵoj. Kiel liganto, ĝi similas al la karbona unuoksido kiu formas plurajn metalkarbonilaĵojn (=CO), kaj efektive ĝia tokseco kuŝas en la fakto ke ĝia molekulo ligiĝas al la fero de la hemoglobino laŭ simila maniero kiel la karbona unuoksido.
Sintezoj
[redakti | redakti fonton]Sintezo 1
[redakti | redakti fonton]- Preparado per duobla interŝanĝo de fosfora triklorido kaj arsena triklorido:
Sintezo 2
[redakti | redakti fonton]- Preparado per interagado de la fosfora triklorido kaj zinka fluorido:
Sintezo 3
[redakti | redakti fonton]- Sintezo per traktado de fosfora triklorido kaj fluorida acido:
Sintezo 4
[redakti | redakti fonton]Reakcioj
[redakti | redakti fonton]Reakcio 1
[redakti | redakti fonton]- Kromia heksafluoro-fosfino povas prepariĝi ekde la kromia dubenzeno:
Reakcio 2
[redakti | redakti fonton]- Trifluoro fosfano reakcias kun akvo donante fosfonatan acidon kaj fluoridan acidon:
Literaturo
[redakti | redakti fonton]- Nature
- Youtube
- The Chemistry of Phosphorus: Pergamon Texts in Inorganic Chemistry
- The Chemistry of Fluorine: Comprehensive Inorganic Chemistry
- General Chemistry: Media Enhanced Edition
- Transition Metal Complexes of Phosphorus, Arsenic & Antimony Ligands[rompita ligilo]






![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](http://178.128.105.246/host-https-wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)
![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](http://178.128.105.246/host-https-wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)