El Vikipedio, la libera enciklopedio
| Natria nitrato
|
|
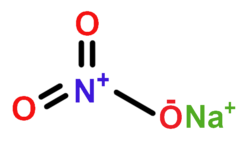
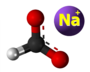
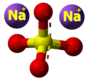
| Plata kemia strukturo de la Natria nitrato
|
|
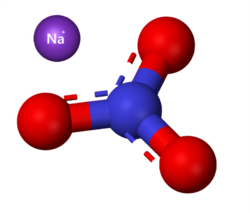
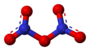
| Tridimensia kemia strukturo de la Natria nitrato
|

|
| Tridimensia strukturo de la Natria nitrato
|
| Alternativa(j) nomo(j)
|
|
|
| Kemia formulo |
NaNO3
|
| CAS-numero-kodo |
7631-99-4
|
| ChemSpider kodo |
22688
|
| PubChem-kodo |
24268
|
| Fizikaj proprecoj
|
| Aspekto |
blankaj kristaloj kun dolĉa odoro
|
| Molmaso |
84.9947 g·mol−1
|
| Denseco |
2.257 g cm−3
|
| Fandpunkto |
308 °C
|
| Bolpunkto |
380 °C (malkomponiĝas)
|
| Solvebleco |
Akvo:
- 73 g/100 ml (0 °C)
- 91.2 g/100 ml (25 °C)
- 180 g/100 ml (100 °C)
|
| Mortiga dozo (LD50) |
3236 mg/kg (buŝe)
|
| Sekurecaj Indikoj
|
| Risko |
R8 R22 S34 R36 R36/37/38 R36/38
|
| Sekureco |
S17 S26 S27 S36 S37/39 S36/37/39
|
| Pridanĝeraj indikoj
|
| Danĝero
|
| GHS etikedigo de kemiaĵoj
|
| GHS Damaĝo-piktogramo |
|
| GHS Signalvorto |
Damaĝa substanco
|
| GHS Deklaroj pri damaĝoj |
H272, H315, H319, H335, H350, H373
|
| GHS Deklaroj pri antaŭgardoj |
P201, P202, P210, P220, P221, P260, P264, P271, P280, P302+352, P304+340, P305+351+338, P308+313, P312, P332+313, P337+313, P362, P370+378, P403+233, P501
|
Escepte kiam indikitaj, datumoj estas prezentataj laŭ iliaj normaj kondiĉoj pri temperaturo kaj premo
(25 °C kaj 100 kPa)
|
Natri-salpetro, aŭ natria nitrato, estas klaso de nitrato kun formulo NaNO³, do ĝi enhavas Natrion, Nitrogenon kaj Oksigenon. Ĝi estas vitrece brila mineralo senkolora. Ĝi havas trigonan simetrion kaj estas ege durefrakta. Ties relativa maso estas 2,25 kaj ties dureco estas 1,5. Ĝi povas troviĝi kiel resto de dezerta forvaporiĝo. Antaŭ la invento de la sintezo de amoniako produktita el aero, ĝi estis ĉefa konsistaĵo de pulvo. Lastatempe ĝi utilas kiel konsistaĵo de minerala sterko por plibonigo de terkulturado.
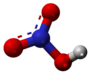
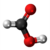
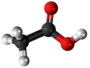
- Hidrolizo de la natria nitrato
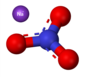
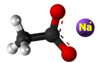
- Preparado de natria butanato per acida interŝanĝo inter natria nitrato kaj buterata acido:
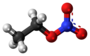
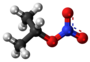
- Preparado de alila nitrato per alkohola interŝanĝo de natria nitrato kaj alila alkoholo en acida medio:
- Per varmigo, nitrata acido malkomponiĝas en dunitrogenan pentoksidon kaj akvon:
- Endre Dudich, "Ĉu vi konas la Teron? Ĉapitroj el la geologiaj sciencoj", Scienca Eldona Centro de UEA, Budapeŝto, 1983.










![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](http://178.128.105.246/host-https-wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)

![{\displaystyle {\mathsf {{\xrightarrow[{}]{OH}}\,}}}](http://178.128.105.246/host-https-wikimedia.org/api/rest_v1/media/math/render/svg/da9b8e5df7c63adcd478cc3011655595b79e288b)
![{\displaystyle {\mathsf {{\xrightarrow[{}]{+[H]}}\,}}}](http://178.128.105.246/host-https-wikimedia.org/api/rest_v1/media/math/render/svg/88fb0b03b975cfe42ff07b526c4bddf66812655c)
![{\displaystyle {\mathsf {{\xrightarrow[{}]{[OH]^{-}}}\,}}}](http://178.128.105.246/host-https-wikimedia.org/api/rest_v1/media/math/render/svg/258ce3c08df9dce17beda55311dbfb79464c8a40)
