Bariumcarbonat
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
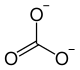
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Bariumcarbonat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | BaCO3 | ||||||||||||||||||
| Kurzbeschreibung |
weißer, geruchloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 197,34 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−1216 kJ·mol−1[4] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Bariumcarbonat ist das Carbonat des Erdalkalimetalls Barium. Es besitzt die Formel BaCO3 und kommt in der Natur als Mineral Witherit vor.
Es wird als Bestandteil von Rattengift sowie als Komponente von Zement und Backsteinen verwendet.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]
Das farblose Salz Bariumcarbonat zersetzt sich bei atmosphärischem Druck bei Temperaturen ab 1300 °C zu Bariumoxid und Kohlenstoffdioxid:[2]
Es kristallisiert orthorhombisch, Raumgruppe Pmcn (Raumgruppen-Nr. 62, Stellung 5) mit den Gitterparametern a = 5,313 Å, b = 8,896 Å und c =6,428 Å.[5] Es sind auch Hochtemperaturformen mit den Raumgruppen R3m (Nr. 166) und Fm3m (Nr. 225) bekannt.[6]
Herstellung
[Bearbeiten | Quelltext bearbeiten]Bariumcarbonat wird industriell durch die Reaktion von Bariumsulfid mit Kohlenstoffdioxid oder auch Natriumcarbonat bei 40–90 °C hergestellt:[7]
Es kann auch durch Einleiten von Kohlenstoffdioxid in eine Aufschlämmung aus Bariumhydroxid in Wasser dargestellt werden:[8]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Bariumcarbonat wird beispielsweise als Rohstoff für die Herstellung von Wirtschaftsglas und optischem Glas benutzt. Zudem ist es das Endprodukt beim Nachweis von Kohlenstoffdioxid mit Barytwasser. Dieser Nachweis ist nur möglich, weil Bariumcarbonat in Wasser schwer löslich ist. In geringen Mengen wird es in der Fahrzeugindustrie für Speicherkatalysatoren eingesetzt.
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Bariumcarbonat ist gesundheitsschädlich.[9] Es wirkt reizend auf Schleimhäute, führt zu Funktionsstörungen im zentralen und peripheren Nervensystem, Muskellähmung, gastrointestinalen Beschwerden sowie Herz-Kreislauf- und Lungenfunktionsstörungen.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g Eintrag zu Bariumcarbonat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Mai 2024. (JavaScript erforderlich)
- ↑ a b Eintrag zu Bariumcarbonat. In: Römpp Online. Georg Thieme Verlag, abgerufen am 15. Juli 2014.
- ↑ Eintrag zu Barium carbonate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ PAETEC Formelsammlung Ausgabe 2003, Seite 116.
- ↑ J.P.R. de Villiers: Crystal structures of aragonite, strontianite, and witherite. In: American Mineralogist, 56, 1971, S. 758–766.
- ↑ K.O. Strømme: On the Crystal Structures of the High-temperature Forms of Strontium and Barium Carbonate and Structurally Related Compounds. In: Acta Chemica Scandinavica, 29, 1975, S. 105–110, doi:10.3891/acta.chem.scand.29a-0105.
- ↑ Robert Kresse, Ulrich Baudis, Paul Jäger, H. Hermann Riechers, Heinz Wagner, Jochen Winkler, Hans Uwe Wolf: Barium and Barium Compounds. In: Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim 2007, ISBN 978-3-527-30673-2.
- ↑ Patent US2013316175A1: Method for preparing sodium ammonium hydrogen phosphate. Angemeldet am 27. November 1968, veröffentlicht am 9. November 1971, Anmelder: Sumitomo Chemical Co, Erfinder: Kozo Fukuba, Reiji Matsuda, Syozo Fujioka, Yasutomo Ogushi, Shigeru Nishibara.
- ↑ William Morton: Poisoning by barium carbonate, The Lancet, 1945,2:738–739 (doi:10.1016/S0140-6736(45)91071-3).



