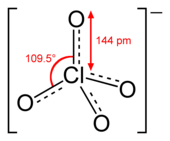
Perklorat
| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC sistematik
Perklorat[1] | |||
| Pengecam | |||
Imej model 3D Jmol
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.152.366 | ||
| 2136 | |||
| MeSH | 180053 | ||
PubChem CID
|
|||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| ClO− 4 | |||
| Jisim molar | 99.45 g·mol−1 | ||
| Asid konjugat | Asid perklorik | ||
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |||
| | |||
| Rujukan kotak info | |||
Perklorat ialah sebatian kimia yang mengandungi ion perklorat, ClO4, asas konjugat asid perklorik (perklorat ion). Sebagai ion pembalas, boleh ada kation logam, kation ammonium kuaterner atau ion lain, contohnya, kation nitronium (NO2+).
Istilah perklorat juga boleh menggambarkan ester perklorat atau perklorat kovalen.[2] Ini adalah sebatian organik yang merupakan alkil atau aril ester asid perklorik. Mereka dicirikan oleh ikatan kovalen antara atom oksigen bahagian ClO4 dan kumpulan organil.
Dalam kebanyakan perklorat ionik, kation tidak berkoordinasi. Majoriti perklorat ionik ialah garam yang dihasilkan secara komersial yang biasa digunakan sebagai pengoksida dalam peranti piroteknik dan keupayaannya mengawal elektrik statik dalam pembungkusan makanan.[3] Selain itu, ia telah digunakan dalam propelan roket, baja, dan sebagai agen peluntur dalam industri kertas dan tekstil.
Pencemaran perklorat terhadap makanan dan air membahayakan kesihatan manusia, terutamanya terhadap kelenjar tiroid.
Perklorat ionik biasanya pepejal tidak berwarna yang menunjukkan keterlarutan yang baik dalam air. Ion perklorat terbentuk apabila ia larut dalam air lalu tercerai menjadi ion. Banyak garam perklorat juga menunjukkan keterlarutan yang baik dalam pelarut bukan akueus.[4] Empat perklorat memiliki kepentingan komersial utama: ammonium perklorat , asid perklorik , kalium perklorat dan natrium perklorat .
Pengeluaran
[sunting | sunting sumber]Garam perklorat biasanya dihasilkan melalui proses elektrolisis yang melibatkan pengoksidaan larutan akueus klorat yang sepadan. Teknik ini lazimnya digunakan dalam penghasilan natrium perklorat yang didapati digunakan secara meluas sebagai bahan utama dalam bahan api roket. Garam perklorat juga biasanya dihasilkan dengan bertindak balas asid perklorik dengan bes, seperti ammonium hidroksida atau natrium hidroksida. Ammonium perklorat yang sangat bernilai juga dihasilkan melalui proses elektrokimia.[5]
Ester perklorat terbentuk dengan kehadiran mangkin nukleofilik melalui penggantian nukleofilik garam perklorat terhadap agen pengalkilan.[6]
Kegunaan
[sunting | sunting sumber]- Penggunaan dominan perklorat adalah sebagai pengoksida dalam propelan untuk roket, bunga api dan suar lebuh raya. Satu kegunaan utama ialah propelan komposit ammonium perklorat sebagai komponen bahan api roket pepejal. Dalam aplikasi berkaitan tetapi lebih kecil, perklorat digunakan secara meluas dalam industri piroteknik dan amunisi tertentu serta mancis.
- Perklorat digunakan untuk mengawal elektrik statik dalam pembungkusan makanan. Ketika disembur pada bekas, ia menghentikan makanan yang dicas secara statik daripada melekat pada permukaan plastik atau kertas/kadbod.[7]
- Kegunaan khusus termasuk litium perklorat, yang terurai secara eksotermik untuk menghasilkan oksigen, berguna dalam "lilin" oksigen pada kapal angkasa, kapal selam, dan dalam situasi lain di mana bekalan oksigen sandaran yang boleh dipercayai diperlukan.[8]
- Kalium perklorat pada masa lalu telah digunakan secara terapeutik untuk membantu menguruskan penyakit Graves. Ia menghalang pengeluaran hormon tiroid yang mengandungi iodin.[9]
Sifat kimia
[sunting | sunting sumber]Ion perklorat adalah yang paling tidak reaktif daripada klorat kebiasaan. Perklorat mengandungi klorin dalam nombor pengoksidaan tertingginya. Jadual potensi penurunan empat klorat menunjukkan bahawa, bertentangan jangkaan, perklorat ialah pengoksida paling lemah antara empat klorat dalam air.
| Ion | Tindak balas asid | E° (V) | Tindak balas neutral/bes | E° (V) |
|---|---|---|---|---|
| Hipoklorit | 2 H+ + 2 HOCl + 2 e− → Cl 2(g) + 2 H 2O |
1.63 | ClO− + H 2O + 2 e− → Cl− + 2 OH− |
0.89 |
| Klorit | 6 H+ + 2 HOClO + 6 e− → Cl 2(g) + 4 H 2O |
1.64 | ClO− 2 + 2 H 2O + 4 e− → Cl− + 4 OH− |
0.78 |
| Klorat | 12 H+ + 2 ClO− 3 + 10 e− → Cl 2(g) + 6 H 2O |
1.47 | ClO− 3 + 3 H 2O + 6 e− → Cl− + 6 OH− |
0.63 |
| Perklorat | 16 H+ + 2 ClO− 4 + 14 e− → Cl 2(g) + 8 H 2O |
1.42 | ClO− 4 + 4 H 2O + 8 e− → Cl− + 8 OH− |
0.56 |
Data ini menunjukkan bahawa perklorat dan klorat ialah pengoksida yang lebih kuat dalam keadaan berasid berbanding dalam keadaan bes.
Pengukuran fasa gas haba tindak balas (yang membenarkan pengiraan ΔHf°) pelbagai oksida klorin mengikut arah aliran yang dijangkakan di mana diklorin heptoksida mempamerkan nilai endotermik terbesar ΔHf° (238.1 kJ/mol) manakala diklorin monoksida mempamerkan nilai endotermik terendah ΔHf° (80.3 kJ/mol).[10]
Klorin dalam anion perklorat ialah atom cengkerang tertutup dan dilindungi dengan baik oleh empat atom oksigen. Kebanyakan sebatian perklorat, terutamanya garam logam elektropositif seperti natrium perklorat atau kalium perklorat tidak mengoksidakan sebatian organik sehingga campuran dipanaskan. Sifat ini berguna dalam banyak aplikasi, seperti suar, di mana pencucuhan diperlukan untuk memulakan tindak balas. Ammonium perklorat adalah stabil apabila tulen tetapi boleh membentuk campuran yang berpotensi meletup dengan logam reaktif atau sebatian organik. Bencana PEPCON memusnahkan loji pengeluaran ammonium perklorat apabila kebakaran menyebabkan ammonium perchlorate yang disimpan di tapak bertindak balas dengan aluminium yang digunakan untuk membina tangki simpanan dan meletup.
Dalam larutan, Ru(II) boleh menurunkan ClO−
4 menjadi ClO−
3, manakala V(II), V(III), Mo(III), Cr(II) dan Ti(III) boleh menurunkan ClO−
4 menjadi Cl−
.[11]
Biologi
[sunting | sunting sumber]Lebih 40 mikroorganisma daripada pelbagai filogenetik dan metabolik yang mampu tumbuh melalui penurunan perklorat[12] telah diasingkan sejak 1996. Kebanyakannya berasal daripada Pseudomonadota, dengan spesies lain termasuk Bacillota, Moorella perchloratireducens dan Sporomusa sp., dan arkea Archaeoglobus fulgidus.[13][14] Kecuali A. fulgidus, semua mikrob yang diketahui tumbuh melalui penurunan perklorat menggunakan enzim perklorat reduktase dan klorit dismutase yang secara kolektif mengambil perklorat kepada klorida yang tidak berbahaya.[13] Dalam proses itu, oksigen bebas dihasilkan.[13]
Kelimpahan semula jadi
[sunting | sunting sumber]Perklorat dicipta oleh pelepasan kilat dengan kehadiran klorida. Perklorat telah dikesan dalam kajian sampel hujan dan salji dari Florida dan Lubbock, Texas.[15] Ia juga terdapat di tanah Marikh.
Perklorat yang terdapat secara semula jadi pada jumlah yang paling banyak boleh didapati bercampur dengan deposit natrium nitrat di Gurun Atacama di utara Chile. Mendapan ini telah banyak dilombong sebagai sumber baja nitrat. Jumlah nitrat di Chile dianggarkan kira-kira 81,000 tonne (89,000 ton) perklorat yang diimport ke AS (1909–1997). Hasil daripada tinjauan air bawah tanah, ais dan padang pasir yang agak tidak terganggu telah digunakan untuk menganggarkan 100,000 hingga 3,000,000 tonne (110,000 hingga 3,310,000 ton) "inventori global" perklorat semula jadi pada masa ini di Bumi.[16]
Pencemaran dalam persekitaran
[sunting | sunting sumber]Perklorat memiliki kebimbangan kerana ketidakpastian tentang keracunan dan kesan kesihatan pada tahap rendah dalam air minuman, kesan ke atas ekosistem, dan laluan pendedahan tidak langsung untuk manusia akibat pengumpulan dalam sayuran.[9] Ia larut dalam air, sangat mudah alih dalam sistem air, dan boleh bertahan selama beberapa dekad di bawah keadaan air bawah tanah dan air permukaan biasa.[17]
Asal perindustrian
[sunting | sunting sumber]Perklorat digunakan kebanyakannya dalam penujah roket, tetapi juga dalam pembasmi kuman, agen peluntur dan racun herba. Perklorat ialah hasil sampingan daripada pengeluaran penujah roket dan bunga api.[4] Bunga api juga merupakan sumber perklorat di tasik.[18] Kaedah penyingkiran dan pemulihan sebatian ini daripada bahan letupan dan propelan roket termasuk pencucian air bertekanan tinggi, yang menjana ammonium perklorat berair.
Dalam makanan
[sunting | sunting sumber]Pada tahun 2004, bahan kimia itu ditemui dalam susu lembu di California pada paras purata 1.3 bahagian per bilion (ppb, atau µg/L), yang mungkin telah memasuki lembu melalui pemakanan pada tanaman yang terdedah kepada air yang mengandungi perklorat.[19] Satu kajian 2005 mencadangkan susu ibu manusia mempunyai purata 10.5 µg/L perklorat.[20]
Mineral dan kejadian semula jadi lain
[sunting | sunting sumber]Di sesetengah tempat, tiada sumber perklorat yang jelas, dan ia mungkin wujud semula jadi. Perklorat semula jadi di Bumi pertama kali dikenal pasti dalam mendapan/baja nitrat daratan Gurun Atacama di Chile seawal tahun 1880-an,[21] dan untuk masa yang lama dianggap sebagai sumber perklorat yang unik. Perklorat yang dikeluarkan daripada penggunaan bersejarah baja berasaskan nitrat Chile yang diimport oleh AS sebanyak ratusan tan pada awal abad ke-19 masih boleh ditemui di beberapa sumber air bawah tanah di Amerika Syarikat seperti di Long Island, New York.[22] Penambahbaikan terkini dalam kepekaan analitik menggunakan teknik berasaskan kromatografi ion telah mendedahkan kehadiran perklorat semula jadi yang lebih meluas, terutamanya dalam tanah bawah Amerika Syarikat Barat Daya,[23] penyejatan garam di California dan Nevada,[24] air bawah tanah Pleistosen di New Mexico,[25] dan malah terdapat di tempat yang sangat terpencil seperti Antartika.[26] Data daripada kajian ini dan lain-lain menunjukkan bahawa perklorat semulajadi didepositkan secara global di Bumi dengan pengumpulan dan pengangkutan seterusnya dikawal oleh keadaan hidrologi tempatan.
Walaupun kepentingannya terhadap pencemaran alam sekitar, sumber dan proses khusus yang terlibat dalam pengeluaran perklorat semula jadi masih kurang difahami. Eksperimen makmal bersama dengan kajian isotop[27] telah membayangkan bahawa perklorat boleh dihasilkan di bumi melalui pengoksidaan spesies klorin melalui laluan yang melibatkan ozon atau produk fotokimianya.[28][29] Kajian lain telah mencadangkan bahawa perklorat juga boleh dicipta oleh pengoksidaan teraktif kilat bagi aerosol klorida (cth., klorida dalam semburan garam laut),[30] dan sinaran ultraungu atau pengoksidaan berhaba klorin (cth., larutan peluntur yang digunakan dalam kolam renang) dalam air.[31][32][33]
Baja
[sunting | sunting sumber]Walaupun perklorat sebagai bahan pencemar alam sekitar biasanya dikaitkan dengan penyimpanan, pembuatan, dan ujian motor roket pepejal,[34] pencemaran perklorat telah ditumpukan dalam penggunaan baja dan pelepasan perkloratnya ke dalam air tanah. Baja meninggalkan anion perklorat untuk bocor ke dalam air tanah dan mengancam bekalan air di banyak wilayah di AS.[34]
Salah satu sumber utama pencemaran perklorat daripada penggunaan baja didapati berasal daripada baja yang diperoleh daripada Chile (kalsium karbonat) kerana Chile mempunyai sumber yang kaya dengan anion perklorat semulajadi.[35] Kepekatan perklorat tertinggi adalah dalam nitrat Chile, antara 3.3 hingga 3.98%.[17] Perklorat dalam baja pepejal adalah antara 0.7 hingga 2.0 mg g−1, variasi kurang daripada faktor 3, dan dianggarkan baja natrium nitrat yang diperolehi daripada baja Chile mengandungi lebih kurang 0.5–2 mg g−1 anion perklorat.[35] Kesan ekologi langsung perklorat tidak diketahui; kesannya boleh dipengaruhi oleh faktor termasuk hujan dan pengairan, pencairan, pengecilan semula jadi, penjerapan tanah, dan bioketersediaan.[35] Kuantifikasi kepekatan perklorat dalam komponen baja melalui kromatografi ion mendedahkan bahawa dalam komponen baja hortikultur mengandungi perklorat antara 0.1 dan 0.46%.[17]
Pembersihan alam sekitar
[sunting | sunting sumber]Terdapat banyak percubaan untuk menghapuskan pencemaran perklorat. Teknologi pemulihan semasa untuk perklorat mempunyai kelemahan kos yang tinggi dan kesukaran dalam operasi.[36] Oleh itu, terdapat minat dalam pembangunan sistem alternatif ekonomi dan hijau.[36]
Rawatan ex situ dan in situ
[sunting | sunting sumber]Beberapa teknologi boleh membuang perklorat melalui rawatan ex situ (luar lokasi) dan in situ (di lokasi).
Rawatan ex situ termasuk pertukaran ion menggunakan resin khusus perklorat atau nitrit, bioremediasi menggunakan bioreaktor berbungkus atau bendalir, dan teknologi membran melalui elektrodialisis dan osmosis songsang.[37] Dalam rawatan ex situ melalui pertukaran ion, bahan cemar tertarik dan melekat pada resin penukar ion kerana resin dan ion bahan cemar tersebut mempunyai cas yang bertentangan.[38] Apabila ion bahan cemar melekat pada resin, satu lagi ion bercas dibuang ke dalam air yang dirawat, di mana ion kemudian ditukar dengan bahan cemar.[38] Teknologi pertukaran ion mempunyai kelebihan kerana ia sangat sesuai bagi rawatan perklorat dan pengeluaran volum tinggi, tetapi mempunyai kelemahan iaitu ia tidak merawat pelarut berklorin. Di samping itu, teknologi ex situ penjerapan karbon fasa cecair digunakan, di mana karbon aktif berbutir (GAC) digunakan untuk menghapuskan tahap perklorat yang rendah dan prarawatan mungkin diperlukan dalam mengatur GAC untuk penyingkiran perklorat.[37]
Rawatan in situ seperti bioremediasi melalui mikrob selektif perklorat dan penghalang reaktif telap juga digunakan untuk merawat perklorat.[37] Bioremediasi in situ mempunyai kelebihan infrastruktur atas tanah yang minimum dan keupayaannya untuk merawat pelarut berklorin, perklorat, nitrat dan RDX secara serentak. Walau bagaimanapun, ia mempunyai kelemahan yang boleh menjejaskan kualiti air sekunder secara negatif. Teknologi fitoremediasi in situ juga boleh digunakan, walaupun mekanisme fitoremediasi perklorat belum diasaskan sepenuhnya.[37]
Bioremediasi menggunakan bakteria penurun perklorat yang mengurangkan ion perklorat kepada klorida yang tidak berbahaya juga telah dicadangkan.[39]
Kesan kesihatan
[sunting | sunting sumber]Perencatan tiroid
[sunting | sunting sumber]Perklorat ialah perencat bersaingan yang kuat bagi simporter natrium-iodida di tiroid.[40] Oleh itu, ia telah digunakan untuk merawat hipertiroidisme sejak tahun 1950-an.[41] Dalam dos yang sangat tinggi (70,000–300,000 ppb), pemberian kalium perklorat dianggap sebagai standard penjagaan di Amerika Syarikat, dan kekal sebagai campur tangan farmakologi yang diluluskan di banyak negara.
Dalam jumlah yang banyak, perklorat mengganggu pengambilan iodin ke dalam kelenjar tiroid. Pada orang dewasa, kelenjar tiroid membantu mengawal metabolisme dengan melepaskan hormon, manakala pada kanak-kanak, tiroid membantu dalam perkembangan yang betul. NAS, dalam laporan 2005-nya, Implikasi Kesihatan Pengambilan Perklorat, menekankan bahawa kesan ini, juga dikenali sebagai Perencatan Serapan Iodida (IUI) bukanlah kesan kesihatan yang buruk. Walau bagaimanapun, pada Januari 2008, Jabatan Kawalan Bahan Toksik California menyatakan bahawa perklorat menjadi ancaman serius kepada kesihatan manusia dan sumber air.[42] Pada 2010, Pejabat Ketua Inspektor EPA menentukan bahawa dos rujukan perklorat agensi itu sendiri sebanyak 24.5 bahagian per bilion melindungi daripada semua kesan biologi manusia berdasarkan pendedahan kerana kerajaan persekutuan bertanggungjawab terhadap semua pencemaran air bawah tanah pangkalan tentera AS. Penemuan ini disebabkan oleh perubahan ketara dalam dasar di EPA dalam mengasaskan penilaian risikonya pada kesan bukan buruk seperti IUI dan bukannya kesan buruk. Pejabat Inspektor Negara juga mendapati bahawa oleh kerana dos rujukan perklorat EPA adalah konservatif dan melindungi kesihatan manusia, pengurangan pendedahan perklorat di bawah dos rujukan tidak mengurangkan risiko secara berkesan.
Oleh kerana kesan buruk ammonium perklorat terhadap kanak-kanak, Massachusetts menetapkan had maksimum sebatian itu dalam air minuman terhadap 2 bahagian per bilion atau 2 mikrogram seliter.[43]
Perklorat hanya menjejaskan hormon tiroid. Kerana ia tidak disimpan atau dimetabolismekan, kesan perklorat pada kelenjar tiroid boleh diterbalikkan, walaupun kesan pada perkembangan otak daripada kekurangan hormon tiroid pada janin, bayi baru lahir dan kanak-kanak pula tidak.[44]
Kesan toksik perklorat telah dikaji dalam tinjauan terhadap pekerja kilang industri yang terdedah kepada perklorat berbanding dengan kumpulan kawalan pekerja kilang industri lain yang tidak diketahui ada pendedahan. Selepas menjalani pelbagai ujian, pekerja yang terdedah kepada perklorat didapati mengalami peningkatan tekanan darah sistolik yang ketara berbanding pekerja yang tidak terdedah, serta penurunan fungsi tiroid yang ketara berbanding pekerja kawalan.[45]
Satu kajian yang melibatkan sukarelawan dewasa yang sihat menentukan bahawa pada tahap melebihi 0.007 miligram sekilogram sehari (mg/(kg·hari)), perklorat boleh menghalang sementara keupayaan kelenjar tiroid untuk menyerap iodin daripada aliran darah ("perencatan pengambilan iodida", dan dengan itu, perklorat ialah goitrogen yang diketahui).[46] EPA menukar dos ini menjadi dos rujukan 0.0007 mg/(kg·d) dengan membahagikan tahap ini dengan faktor ketidakpastian intraspesies piawai bernilai 10. Agensi itu kemudian mengira "paras setara air minuman" sebanyak 24.5 ppb dengan mengandaikan berat seseorang ialah 70 kg (150 lb), dan dia minum 2 L (0.44 imp gal; 0.53 US gal) air minuman setiap hari sepanjang hayat.[47]
Pada 2006, satu kajian melaporkan persatuan statistik antara tahap perklorat persekitaran dan perubahan dalam hormon tiroid wanita dengan iodin rendah. Penulis kajian berhati-hati untuk menunjukkan bahawa tahap hormon dalam semua subjek kajian kekal dalam julat normal. Penulis juga menunjukkan bahawa mereka pada asalnya tidak menormalkan penemuan mereka bagi kreatinina yang pada asasnya menyumbang turun naik dalam kepekatan sampel air kencing sekali seperti yang digunakan dalam kajian ini.[48] Apabila penyelidikan Blount dianalisis semula dengan pelarasan kreatinina yang dibuat, populasi kajian terhad kepada wanita umur reproduktif, dan keputusan yang tidak ditunjukkan dalam analisis asal, sebarang perkaitan yang tinggal antara keputusan dan pengambilan perklorat hilang.[49] Tidak lama selepas kajian Blount yang disemak dikeluarkan, Robert Utiger, seorang doktor dengan Institut Perubatan Harvard, memberi keterangan di hadapan Kongres AS dan menyatakan: "Saya terus percaya bahawa dos rujukan itu, 0.007 miligram sekilo (24.5). ppb), yang merangkumi faktor 10 untuk melindungi mereka yang mungkin lebih terdedah, cukup memadai."[50]
Pada tahun 2014 satu kajian telah diterbitkan, menunjukkan bahawa pendedahan alam sekitar kepada perklorat pada wanita hamil dengan hipotiroidisme dikaitkan dengan risiko ketara perendahan IQ pada anak-anak mereka.[51]
Keracunan paru-paru
[sunting | sunting sumber]Sesetengah kajian mencadangkan bahawa perklorat mempunyai kesan racun pulmonari juga. Kajian telah dijalankan ke atas arnab di mana perklorat telah disuntik ke dalam trakea. Tisu paru-paru telah dikeluarkan dan dianalisis, dan didapati bahawa tisu paru-paru yang disuntik perklorat menunjukkan beberapa kesan buruk jika dibandingkan dengan kumpulan kawalan yang telah disuntik secara intratrakea dengan garam. Kesan buruk termasuk pencerobohan keradangan, keruntuhan alveolar, penebalan subpleural dan percambahan limfosit.[52]
Anemia aplastik
[sunting | sunting sumber]Pada awal 1960-an, kalium perklorat yang digunakan untuk merawat penyakit Graves telah terlibat dalam perkembangan anemia aplastik - keadaan di mana sumsum tulang gagal menghasilkan sel darah baharu dalam kuantiti yang mencukupi; dalam 13 orang pesakit, tujuh daripadanya meninggal dunia.[53] Penyiasatan seterusnya telah menunjukkan hubungan antara pemberian kalium perklorat dan perkembangan anemia aplastik adalah "sebaik-baiknya disamarkan", yang bermaksud bahawa manfaat rawatan, jika ia adalah satu-satunya rawatan yang diketahui, melebihi risiko, dan sebaliknya, ditemui bahawa suatu bahan pencemar lain yang menyebabkan keracunan 13 orang pesakit di atas.[54]
Perklorat kovalen
[sunting | sunting sumber]Walaupun biasanya ditemui sebagai anion tak berkoordinat, beberapa kompleks logam diketahui. Heksaperkloratoaluminat dan tetraperkloratoaluminat ialah agen pengoksidaan yang kuat.
Beberapa ester perklorat diketahui.[2] Sebagai contoh, metil perklorat ialah bahan tenaga tinggi yang merupakan agen pengalkilan yang kuat. Klorin perklorat ialah sejenis analog tak organik kovalen.
Rujukan
[sunting | sunting sumber]- ^ "Perchlorate – PubChem Public Chemical Database". The PubChem Project. USA: National Center for Biotechnology Information.
- ^ a b Markov, P. O.; Yashin, N. V.; Averina, E. B. (2022). "Covalent Organic Perchlorates: Synthesis and Properties". Reviews and Advances in Chemistry (dalam bahasa Inggeris). 12 (3): 178–193. doi:10.1134/S2634827622600153. ISSN 2634-8276.
- ^ Draft Toxicological Profile for Perchlorates, Agency for Toxic Substances and Disease Registry, U.S. Department of Health and Human Services, September, 2005.
- ^ a b Kucharzyk, Katarzyna (2009). "Development of drinking water standards for perchlorate in the United States". Journal of Environmental Management. 91 (2): 303–310. doi:10.1016/j.jenvman.2009.09.023. PMID 19850401.
- ^ Dotson R.L. (1993). "A novel electrochemical process for the production of ammonium perchlorate". Journal of Applied Electrochemistry. 23 (9): 897–904. doi:10.1007/BF00251024.
- ^ Zefirov, N. S.; Zedankin, V. V.; Koz'min, A. S. (1988). "The synthesis and properties of covalent organic perchlorates". Russian Chemical Reviews. Turpion. 57 (11). doi:10.1070/RC1988v057n11ABEH003410.
- ^ McMullen Jenica, Ghassabian Akhgar, Kohn Brenda, Trasande Leonardo (2017). "Identifying Subpopulations Vulnerable to the Thyroid-Blocking Effects of Perchlorate and Thiocyanate". The Journal of Clinical Endocrinology & Metabolism. 102 (7): 2637–2645. doi:10.1210/jc.2017-00046. PMID 28430972.CS1 maint: multiple names: authors list (link)
- ^ Markowitz, M. M.; Boryta, D. A.; Stewart, Harvey (1964). "Lithium Perchlorate Oxygen Candle. Pyrochemical Source of Pure Oxygen". Industrial & Engineering Chemistry Product Research and Development. 3 (4): 321–330. doi:10.1021/i360012a016.
- ^ a b Susarla Sridhar; Collette C. W.; Garrison A. W.; Wolfe N. L.; McCutcheon S. C. (1999). "Perchlorate Identification in Fertilizers". Environmental Science and Technology. 33 (19): 3469–3472. Bibcode:1999EnST...33.3469S. doi:10.1021/es990577k.
- ^ Wagman, D. D.; Evans, W. H.; Parker, V. P.; Schumm, R. H.; Halow, I.; Bailey, S. M.; Churney, K. L.; Nuttall, R. L. J. Phys.
- ^ Edward T. Urbansky.
- ^ Thrash JC, Pollock J, Torok T, Coates JD (2010). "Description of the novel perchlorate-reducing bacteria Dechlorobacter hydrogenophilus gen. nov., sp. nov. and Propionivibrio militaris, sp. nov". Appl Microbiol Biotechnol. 86 (1): 335–43. doi:10.1007/s00253-009-2336-6. PMC 2822220. PMID 19921177.CS1 maint: multiple names: authors list (link)
- ^ a b c John D. Coates; Laurie A. Achenbach (2004). "Microbial perchlorate reduction: rocket-fuelled metabolism". Nature Reviews Microbiology. 2 (7): 569–580. doi:10.1038/nrmicro926. PMID 15197392.
- ^ Martin G. Liebensteiner, Martijn W. H. Pinkse, Peter J. Schaap, Alfons J. M. Stams, Bart P. Lomans (5 April 2013). "Archaeal (Per)Chlorate Reduction at High Temperature: An Interplay of Biotic and Abiotic Reactions". Science. 340 (6128): 85–87. Bibcode:2013Sci...340...85L. doi:10.1126/science.1233957. PMID 23559251.CS1 maint: multiple names: authors list (link)
- ^ Kathleen Sellers, Katherine Weeks, William R. Alsop, Stephen R. Clough, Marilyn Hoyt, Barbara Pugh, Joseph Robb.
- ^ DuBois, Jennifer L.; Ojha, Sunil (2015). "Chapter 3, Section 2.2 Natural Abundance of Perchlorate on Earth". Dalam Peter M.H. Kroneck and Martha E. Sosa Torres (penyunting). Sustaining Life on Planet Earth: Metalloenzymes Mastering Dioxygen and Other Chewy Gases. Metal Ions in Life Sciences. 15. Springer. m/s. 45–87. doi:10.1007/978-3-319-12415-5_3. ISBN 978-3-319-12414-8. PMC 5012666. PMID 25707466.
- ^ a b c Susarla Sridhar; Collette T. W.; Garrison A. W.; Wolfe N. L.; McCutcheon S. C. (1999). "Perchlorate Identification in Fertilizers". Environmental Science and Technology. 33 (19): 3469–3472. Bibcode:1999EnST...33.3469S. doi:10.1021/es990577k.
- ^ "Fireworks Displays Linked To Perchlorate Contamination In Lakes". Science Daily. Rockville, MD. 2007-05-28.
- ^ Associated Press.
- ^ McKee, Maggie.
- ^ Ericksen, G. E. "Geology and origin of the Chilean nitrate deposits"; U.S. Geological Survey Prof. Paper 1188; USGS: Reston, VA, 1981, 37 pp.
- ^ Böhlke J. K.; Hatzinger P. B.; Sturchio N. C.; Gu B.; Abbene I.; Mroczkowski S. J. (2009). "Atacama perchlorate as an agricultural contaminant in groundwater: Isotopic and chronologic evidence from Long Island, New York". Environmental Science & Technology. 43 (15): 5619–5625. Bibcode:2009EnST...43.5619B. doi:10.1021/es9006433. PMID 19731653.
- ^ Rao B.; Anderson T. A.; Orris G. J.; Rainwater K. A.; Rajagopalan S.; Sandvig R. M.; Scanlon B. R.; Stonestrom S. A.; Walvoord M. A. (2007). "Widespread NaturalPerchlorate in Unsaturated zones of the Southwest United States". Environ. Sci. Technol. 41 (13): 4522–4528. Bibcode:2007EnST...41.4522R. doi:10.1021/es062853i. PMID 17695891.
- ^ Orris, G. J.; Harvey, G. J.; Tsui, D. T.; Eldridge, J. E. Preliminaryanalyses for perchlorate in selected natural materials and theirderivative products; USGS Open File Report 03-314; USGS, U.S.Government Printing Office: Washington, DC, 2003.
- ^ Plummer L. N.; Bohlke J. K.; Doughten M. W. (2005). "Perchlorate in Pleistocene and Holocene groundwater in North-Central New Mexico". Environ. Sci. Technol. 40 (6): 1757–1763. Bibcode:2006EnST...40.1757P. doi:10.1021/es051739h. PMID 16570594.
- ^ Böhlke, Karl John, Sturchio Neil C., Gu Baohua, Horita Juske, Brown Gilbert M., Jackson W. Andrew, Batista Jacimaria, Hatzinger Paul B. (2005). "Perchlorate isotope forensics". Analytical Chemistry. 77 (23): 7838–7842. doi:10.1021/ac051360d. PMID 16316196.CS1 maint: multiple names: authors list (link)
- ^ Rao B., Anderson T. A., Redder A., Jackson W. A. (2010). "Perchlorate Formation by Ozone Oxidation of AqueousChlorine/Oxy-Chlorine Species: Role of ClxOy Radicals". Environ. Sci. Technol. 44 (8): 2961–2967. Bibcode:2010EnST...44.2961R. doi:10.1021/es903065f. PMID 20345093.CS1 maint: multiple names: authors list (link)
- ^ Catling, D. C., M. W. Claire, K. J. Zahnle, R. C. Quinn, B. C. Clark, M. H. Hecht, and S. Kounaves (2010). "Atmospheric origins of perchlorate on Mars and in the Atacama". J. Geophys. Res. 115 (E1): E00E11. Bibcode:2010JGRE..115.0E11C. doi:10.1029/2009JE003425. PMC 7265485. PMID 32487988.CS1 maint: multiple names: authors list (link)
- ^ Dasgupta P. K.; Martinelango P. K.; Jackson W. A.; Anderson T. A.; Tian K.; Tock R.W.; Rajagopalan S. (2005). "The origin of naturally occurring perchlorate: the role ofatmospheric processes". Environmental Science & Technology. 39 (6): 1569–1575. Bibcode:2005EnST...39.1569D. doi:10.1021/es048612x. PMID 15819211.
- ^ Rao B.; Estrada N; Mangold J.; Shelly M.; Gu B.; Jackson W. A. (2012). "Perchlorate production byphotodecomposition of aqueous chlorine". Environ. Sci. Technol. 46 (21): 11635–11643. Bibcode:2012EnST...4611635R. doi:10.1021/es3015277. PMID 22962844.
- ^ Stanford B. D.; Pisarenko A. N.; Snyder S. A.; Gordon G. (2011). "Perchlorate, bromate, and chlorate in hypochlorite solutions: Guidelines for utilities". Journal of the American Water Works Association. 103 (6): 71. doi:10.1002/j.1551-8833.2011.tb11474.x.
- ^ William E. Motzer (2001). "Perchlorate: Problems, Detection, and Solutions". Environmental Forensics. 2 (4): 301–311. doi:10.1006/enfo.2001.0059.
- ^ a b Magnuson Matthew L.; Urbansky Edward T.; Kelty Catherine A. (2000). "Determination of Perchlorate at Trace Levels in Drinking Water by Ion-Pair Extraction with Electrospray Ionization Mass Spectrometry". Analytical Chemistry. 72 (1): 25–29. doi:10.1021/ac9909204. PMID 10655630.
- ^ a b c Urbansky T.; Brown S.K.; Magnuson M.L.; Kelty C.A. (2001). "Perchlorate levels in samples of sodium nitrate fertilizer derived from Chilean caliche". Environmental Pollution. 112 (3): 299–302. doi:10.1016/s0269-7491(00)00132-9. PMID 11291435.
- ^ a b "Eliminating Water Contamination by Inorganic Disinfection Byproducts". Hazen and Sawyer. 19 July 2012. Diarkibkan daripada yang asal pada 29 April 2021. Dicapai pada 28 March 2014.
- ^ a b c d "Technical Fact Sheet – Perchlorate" (PDF). US EPA. 2013-04-23. Diarkibkan daripada yang asal (PDF) pada 7 June 2013.
- ^ a b "ARA Perchlorate Contamination Solutions". Applied Research Associates, Inc. Diarkibkan daripada yang asal pada 29 April 2014.
- ^ Bardiya, Nirmala; Bae, Jae-Ho (2011). "Dissimilatory perchlorate reduction: A review". Microbiological Research. 166 (4): 237–254. doi:10.1016/j.micres.2010.11.005. PMID 21242067.
- ^ Braverman, L. E.; He X.; Pino S. (2005). "The effect of perchlorate, thiocyanate, and nitrate on thyroid function in workers exposed to perchlorate long-term". J Clin Endocrinol Metab. 90 (2): 700–706. doi:10.1210/jc.2004-1821. PMID 15572417. Unknown parameter
|displayauthors=ignored (bantuan) - ^ Godley, A. F.; Stanbury, J. B. (1954). "Preliminary experience in the treatment of hyperthyroidism with potassium perchlorate". J Clin Endocrinol Metab. 14 (1): 70–78. doi:10.1210/jcem-14-1-70. PMID 13130654.
- ^ "Perchlorate". California Department of Toxic Substances Control. Jan 26, 2008. Diarkibkan daripada yang asal pada August 23, 2009. Dicapai pada January 27, 2008.
- ^ https://www.mass.gov/guides/perchlorate-frequently-asked-questions
- ^ J. Wolff (1998). "Perchlorate and the Thyroid Gland". Pharmacological Reviews. 50 (1): 89–105. PMID 9549759.
- ^ "[original title not given]" [Health survey of plant workers for an occupational exposure to ammonium perchlorate]. Zhonghua Lao Dong Wei Sheng Zhi Ye Bing Za Zhi. 31 (1): 45–7. Jan 2013. PMID 23433158.
- ^ Greer, M. A.; Goodman, G.; Pleuss, R. C.; Greer, S. E. (2002). "Health effect assessment for environmental perchlorate contamination: The dose response for inhibition of thyroidal radioiodide uptake in humans" (free online). Environmental Health Perspectives. 110 (9): 927–937. doi:10.1289/ehp.02110927. PMC 1240994. PMID 12204829.
- ^ "Perchlorate Guidance (Memorandum)" (PDF). EPA. January 26, 2006.
- ^ Benjamin C. Blount; James L. Pirkle; John D. Osterloh; Liza Valentin-Blasini; Kathleen L. Caldwell (2006). "Urinary Perchlorate and Thyroid Hormone Levels in Adolescent and Adult Men and Women Living in the United States". Environmental Health Perspectives. 114 (12): 1865–71. doi:10.1289/ehp.9466. PMC 1764147. PMID 17185277.
- ^ Tarone (2010). "The Epidemiology of Environmental Perchlorate Exposure and Thyroid Function: A Comprehensive Review". Journal of Occupational and Environmental Medicine. 52 (June): 653–60. doi:10.1097/JOM.0b013e3181e31955. PMID 20523234. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Perchlorate: Health and Environmental Impacts of Unregulated Exposure". United States Congress. Dicapai pada 15 April 2012.
- ^ Taylor, Peter N.; Okosieme, Onyebuchi E.; Murphy, Rhian; Hales, Charlotte; Chiusano, Elisabetta; Maina, Aldo; Joomun, Mohamed; Bestwick, Jonathan P.; Smyth, Peter (November 2014). "Maternal Perchlorate Levels in Women With Borderline Thyroid Function During Pregnancy and the Cognitive Development of Their Offspring: Data From the Controlled Antenatal Thyroid Study". The Journal of Clinical Endocrinology & Metabolism (dalam bahasa Inggeris). 99 (11): 4291–4298. doi:10.1210/jc.2014-1901. ISSN 0021-972X. PMID 23706508.
- ^ Wu F.; Chen H.; Zhou X.; Zhang R.; Ding M.; Liu Q.; Peng KL. (2013). "Pulmonary fibrosis effect of ammonium perchlorate exposure in rabbit". Arch Environ Occup Health. 68 (3): 161–5. doi:10.1080/19338244.2012.676105. PMID 23566323.
- ^ National Research Council (2005). "Perchlorate and the thyroid". Health implications of perchlorate ingestion. Washington, D.C: National Academies Press. m/s. 7. ISBN 978-0-309-09568-6.
- ^ Clark, J. J. J. (2000). "Toxicology of perchlorate". Dalam Urbansky ET (penyunting). Perchlorate in the environment. New York: Kluwer Academic/Plenum Publishers. m/s. 19–20. ISBN 978-0-306-46389-1.